研究ファイル形式 API
スタディファイルフォーマット (SFF)は、Veeva EDCおよびCDBシステムから臨床データをエクスポートするための標準化された方法です。(YNA comment: Need to be changed globally.)SFFはスタディファイルフォーマット API を通じてアクセスされ、試験データと試験定義という2つの主要部分を含む単一のZIPパッケージとして提供されます。(YNA comment: Need to be changed globally.)
SFFは、臨床および運用データの報告や、他のシステムとの統合に役立ちます。ZIPパッケージには、臨床データ、運用データ、および参照データを提供するマニフェストファイルとCSVが含まれています。マニフェストファイルには、試験定義と試験データの関係が詳細に記載されています。(YNA comment: Need to be changed globally.)
抽出タイプ:SFF抽出には、フルとインクリメンタルの2つのタイプがあります。SFFの完全抽出には、データ収集の開始から最新のSFF完全抽出まで、すべてのデータセットが含まれています。SFF のフル抽出 (パッケージ) は、24 時間ごとの午後 12 時 (UTC) に利用可能です。臨床および運用データは、最新のSFF抽出以降の変更を反映するように、段階的に生成することができます。リストパッケージ エンドポイントを使用する際には、フルまたはインクリメンタルを指定できます。
ライセンス: CDMS ライセンスには、フルおよびインクリメンタル SFF パッケージの両方が含まれます。フルパッケージは、EDC ツールのスタディから有効化できます。インクリメンタルパッケージを有効化するには、Veeva サポートに連絡してください。
バージョン管理: SFF では、API とパッケージで別々のバージョン管理を採用しています。当社は、2 つの有効な API バージョンと 2 つの有効なパッケージバージョンを維持しています。パッケージのバージョン管理については、既存の統合を破損させる可能性のあるスキーマの変更があった場合のみ、新しいバージョンを作成します。例えば、構造に影響を与えない列を CSV ファイルに追加するだけの場合、パッケージのバージョンは変更しません。マニフェストの属性が変更された場合は、新しいバージョンを作成します。
API のバージョン管理の詳細については、開発者ポータルをご覧ください。
SFFは OpenEDC 試験をサポートしていません。既存の EDC データを使用したサードパーティのスタディをサポートします。
前提条件
標準の CDMS スーパーユーザ治験の役割を持つユーザは、デフォルトで下記のアクションを実行することができます。組織がカスタムロールを使用する場合、そのロールには以下の権限を付与することが必要です:
| タイプ | 権限ラベル | 制御 |
|---|---|---|
| 機能権限 | 研究ファイル形式 API アクセス | 治験ファイル形式 API にアクセスし、使用する権限。 スタディファイルフォーマット APIアクセスは、デフォルトでAPIアクセスと制限付きデータアクセスを提供します。 (YNA comment: Need to be changed globally.) |
| 機能権限 | ワークベンチタブ* | ワークベンチ(Workbench)タブからデータワークベンチアプリケーションにアクセスする権限。 *[ワークベンチ]タブの権限は、インクリメンタルエクスポートを使用するワークベンチスタディでスタディファイルフォーマットAPIを使用する場合のみ必要です。 |
スタディファイルフォーマット API の有効化
SFFは、本番試験環境およびテスト試験環境の両方で有効化できます。
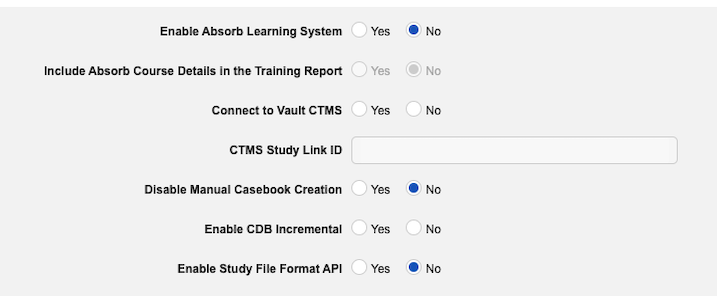
Vaultでスタディファイルフォーマット機能を有効にするには: (YNA comment: Need to be changed globally.)
CDB 増分インポート: CDB 増分インポートは、CDB スタディの前提条件です。データ vault が 24R2 リリース以降に作成された場合は、データ vault で増分インポートが有効になっています。データ vault が 24R2 リリースより前に作成された場合、この機能はまだ有効になっていない可能性があります。
SFFを初めて有効にする場合は、最初のSFFパッケージが完全に公開され、APIを通じて利用可能になるまで待ちます。この機能は、無効にした後に試験用に再度有効にした場合にも適用されます。 (YNA comment: Need to be changed globally.)
SFFテスト環境
テスト(TST)試験環境でSFFを有効にすると、SFF APIにアクセスしてテストするための30日間の期間が開始されます。これにより、開発およびテストのプロセス全体を通じて、スタディデザインを使用してSFFの機能をテストできます。テストはCDBライセンススタディでのみ利用可能です。Vaultに対して増分インジェストが有効になっている場合、CDBは増分パッケージを生成します。
SFFがテスト用に有効化されると、次の2つの条件下で自動的に無効化されます:
- 前回パッケージをダウンロードしてから30日が経過した場合
- ユーザが一度もパッケージをダウンロードしなかった場合
無効化後にSFFにアクセスしようとすると、エラーメッセージが表示されます。テスト期間が終了する前にSFFを無効にすると、CDBは期間の開始時刻をクリアします。
30日間のテスト期間を再開するには、 ツール > EDCツール > スタディ設定(Tools > EDC Tools > Study Settings)でこの機能を再度有効にする必要があります。再度有効にするには、CDBで新しい完全なSFFパッケージを生成する必要があります。
パッケージ内容 &構成
SFFパッケージはZIPファイル形式で提供されます。ZIPファイル内には、すべてのCSVファイルが格納された「data」というフォルダがあります。ZIPファイルのルートにある「manifest.json」ファイルには、パッケージの自己記述構造と試験デザイン情報が含まれています。 (YNA comment: Need to be changed globally.)
パッケージファイルのファイル名の形式は以下の通りです。
試験名_SFF_フル/増分_YYYY_MM_DD_HH_MM_SS (YNA comment: Need to be changed globally.)
例えば、Natevba_SFF_Incremental_2024_08_16_00_30_00
名前に含まれるタイムスタンプは、パッケージの公開時刻を示しています。
列ヘッダーの重複
アイテム定義をフォームで再利用すると、CSV 列ヘッダーが重複して表示されます。SFFでは、重複する列には"_n"を付加することで、重複に対処しています。 例:_1、_2。最初の列は元の名前を維持し、各列に接尾辞が追加されます。列名の重複排除では大文字と小文字が区別されます。例えば、「ColumnName」と「columnname」は異なる名前として扱われ、重複排除されません。
列の外観の各インスタンスは、マニフェストファイルのclinical_data セクションに表示されます。このセクションでは、重複排除された名前は name フィールドに表示され、元のアイテム定義名はlookup_name フィールドに表示されます。
重複排除により、itemgroups 配列は単一の属性となり、各列の単一のアイテムグループ定義を示します。これは、フォーム定義に複数のラボパネルが存在する場合、ローカルラボの列ヘッダにも適用されます。
パッケージバージョン 2.0 は重複列機能をサポートしています。
完全データ抽出
ZIPパッケージの完全な抽出は24時間ごとに利用可能であり、次のような状況で下流システムの更新を支援するように設計されています。
- 初めての試験でSFFを有効にする (YNA comment: Need to be changed globally.)
- 新しいスタディデザインの変更または展開中
- 完全な更新によるデータの置き換え(つまり、EDCから CDBへのデータの完全な取り込み)
- 再起動が必要な重大なエラーが発生しました。
完全な必須フィールド:SFF APIレスポンスのfull_requiredフィールドは、完全なデータ抽出が必要であることを示します。このフィールドは、 TrueとFalseの2つの値を受け入れます。スタディデザインに変更が生じたり、CDBのエラーにより完全な更新が必要になったりすると、システムはfull_requiredフィールドをTrueに設定します。
スタディデザインデータ
マニフェストファイル内のスタディデザインデータは、常に完全なデータセットとして抽出され、インクリメンタルには抽出されません。抽出のたびに、最新のスタディデザインデータが取得されます。
ラベルとラベルのオーバーライド
ラベルおよびオーバーライドラベルには、最新のスタディデザインバージョンのデータが含まれます。
増分データ抽出
インクリメンタル抽出は 15 分ごとに利用可能です。増分抽出を使用する場合、最後の抽出と現在の抽出に変更がない場合、列見出しのみの空白ファイルとして生成されます。
ファイルを削除します
増分抽出の参照データには、DELETES CSVファイルが含まれています。統合システムから削除すべき行を特定するために必要な、すべての削除済みデータが含まれています。
ROW ID列
ROW ID列は DELETESファイルを除くすべてのファイルに含まれており、更新および削除された行を特定するために使用できます。Row IDは、一意のデータ行を作成するために使用される基礎となる識別子です。Row IDの構造はファイルによって異なります。
データ変更の処理
増分抽出または ZIPパッケージへの変更は、挿入ではなくUpsertとして扱う必要があります。Upsertコマンドは、値がすでに存在する場合は既存の行を更新し、存在しない場合は新しい行を挿入します。これに対する唯一の例外は、削除された行を追跡するDeletesファイルです。
Manifestファイルの理解
JSONは、スタディデザインオブジェクトをスタディデータにマッピングするために使用できる構造化されたフォーマットです。Manifest.json ファイルにより、ユーザーはプログラムでデータを消費することができます。これは、スタディデータファイルの構造を定義し、スタディデザインを含みます。
マニフェストファイルのヘッダー情報は、以下の内容で構成されています。
- 試験名 (YNA comment: Need to be changed globally.)
- ドキュメントの URL
- SFF 版
- 名前を抽出
- 作成日時
- パッケージ内のファイル数
- 臨床データが徐々に生成されるかどうかに関わらず、
- マニフェストが参照しているスタディデザインのバージョンは何ですか。
SFF API バージョンは、SFF パッケージバージョンとは独立して動作します。例えば、SFF API バージョンはバージョン 23.2、24.3、25.2 が利用可能であり、SFF パッケージは 1. 0と 2.0 バージョンを提供しています。
データは4つのJSONコードブロックに分割されています。
- 運用データ
- 参照データ
- クリニカルデータ
- スタディデザイン
マニフェストファイル例
マニフェストファイルのサンプルをダウンロードします。
パッケージバージョン 1.0:
パッケージバージョン 2.0:
運用 &参照データ
運用データは、システムファイルを含む運用データファイルを定義し、参照データは、スタディに関連する参照データファイルを定義します。
クリニカルデータ
臨床データは、ファイル名、ソース、フォームおよび列ヘッダーで構成されています。
| フィールド | 説明 |
|---|---|
| ファイル名 | CSVファイルの名前(例:「prescreening.csv」) |
| ソース | 試験データファイルのソース(例:「EDC」) |
| フォーム | フォーム定義の名称 |
| 列 | ファイル列の配列には、定義済みのヘッダー列と臨床アイテム列の両方が含まれます。各アイテム列は、単一のアイテム定義を表します。 アイテム定義(Item Definition) メタデータは、EDC Studioから取得されます。 アイテムには追加の属性が備わっている場合があります。詳細については、以下の 追加のアイテム属性(Additional Item Attributes)セクションを参照してください。 |
追加のアイテム属性
以下は、マニフェストファイル内の試験データに関する追加のアイテム属性の例です。
- 名前:属性の名前
- External_id: 属性の外部ID
- SDTM_name: SDTM名
- データタイプV:EDCのデータタイプ(下記参照)に基づきます。
- 長さ:テキスト、数値、コードリスト、および単位のアイテムタイプ用に設定済み
- 精密さ:および単位のアイテムタイプ用に設定済み
- v不明:日付または日時形式で入力できます。不明な部分を許可するアイテム定義V
- マスク:通常、不明な日付と日時用に設定されています。
- Item_type: 例えば、edc__v、derived__v、read_only__v
- アイテムグループ:アイテムグループ定義名(複数可)
- アイテム定義がアイテムグループ定義間で再利用される場合、すべてのアイテムグループ定義はフォーム定義にリストされている順番で配列に表示されます。 (YNA comment: Need to be changed globally.)
- 制限付き:制限付きデータ、ブール値はtrueまたはfalseに等しい
- コードリスト:コードリスト定義名
- 単位:単位定義名
データタイプ
データタイプアイテムの属性は、以下のEDCデータタイプに基づいています:
- テキスト
- コードリスト
- url
- ラベル
- ブーリアン
- 数字
- 単位
- 日付
- 日時
- 時間
スタディデザイン
スタディデザイン(study_design)ブロックには、以下のセクションが含まれます。
- イベントグループ: スタディで構成されたすべての事象グループ定義を定義します。
- イベント: スタディで構成されたすべての事象定義を定義します。
- フォーム: スタディで構成されたすべてのフォーム定義を定義します。
- アイテムグループ: スタディで構成されたすべてのアイテムグループ定義を定義します。
- コードリスト: 試験データファイル(ラボ以外)で使用されるコードリスト定義をすべて定義します。
- 単位: 試験データファイル(ラボ以外)で使用される単位定義をすべて定義します。
- Subject_groups: スタディで構成されたすべての症例グループ定義を定義します。
試験データファイル(ラボ以外)で使用されるコードリスト定義をすべて定義します。各臨床ファイルには、イベントグループ、イベント、フォーム定義の名前への参照キーがあります。これにより、臨床ファイルとスタディデザインオブジェクトの関係をマッピングすることができます。
マニフェストファイル内の列は順序どおりであることが保証されていません。しかし、プログラムで各列を対応するCSV列ヘッダーにマッピングすることができます。これは順序通りに保存されます。
スタディデータファイル
SFFの試験データ部分も、試験データ、運用データ、参照データで構成されています。 (YNA comment: Need to be changed globally.) 試験データファイルには、各症例に関連する試験、サイト国、サイト、イベントグループ、イベント、フォームを示すヘッダー列が含まれています。 (YNA comment: Need to be changed globally.) フォーム上の各臨床アイテムには、主となる列の見出しの後に配置された、それぞれの列が設けられます。
試験データファイルは制限されたデータが含まれています。 (YNA comment: Need to be changed globally.) スタディファイルフォーマット API アクセス権限は、デフォルトで制限付きデータアクセス権限を付与します。 (YNA comment: Need to be changed globally.)
通常、イベントグループ、イベント、フォーム、アイテムグループ、アイテム定義、ステータスなどのオブジェクトには、ラベルではなく名前が使用されます。ラベルは、SFFの完全ZIPパッケージ内のLABELS CSVファイルに記載されています。IDは、データ行の一意の識別子であるRow IDとして以外は、SFFでは表示されません。
試験データファイル
試験データファイルは、各フォーム定義ごとに1つのCSVファイルで構成されています。ファイルのタイトルはフォーム定義名と同じです。同じ名前のフォーム定義が複数ある場合、追加のフォーム定義のファイル名には_2、_3などが付加されます。順序は、ソース名とフォーム定義名の両方のアルファベット順で決定されます。各ファイルには、特定のフォームインスタンスの試験データの行を表すレコードが含まれています。試験データには、ステータスが「提出済み」および「編集中(in_progress_post_submit__v)」のフォームが含まれます。
試験データヘッダー
試験データヘッダーは、フォーム内の試験データの階層を表す標準の列です。ヘッダーは、すべての試験データファイルで共通です。
列のリストは以下の通りです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| EGROUPNAME | テキスト | 事象グループ名 |
| EGSEQ | 数字 | 事象グループ順序 |
| EventName | テキスト | 事象名 |
| FORMNAME | テキスト | フォーム名 |
| FSEQ | 数字 | フォーム順序 |
| IGSEQ | 数字 | 項目グループ順序 |
| FORMSTATUS | テキスト | フォームステータス |
| CREATEDDT | 日時 | フォームが作成された日時 |
| FIRSTSUBMITDT | 日時 | フォームが最初に送信された日時 |
| LASTSUBMITDT | 日時 | フォームが最後に送信された日時 |
| FORMLASTMODDT | 日時 | フォームが最後に修正された日時 |
| アイテム列 | 異なる | アイテム列 (フォームのアイテム数に合わせて拡張) |
| ROWWRITEDT | 日時 | ファイルに書き込まれた行の日時 |
| ROWID | テキスト | 行 ID |
試験アイテムデータ
試験アイテムは、各臨床ファイルの上部に列挙されたヘッダー列の後に表示され、それぞれのアイテム定義名がそれぞれの列に表示されます。必要に応じて動的にデータを追加します。例えば、アイテムグループが非反復の場合、対応するアイテムグループのシーケンスは臨床フォームに表示されません。
データタイプ &フォーマット
| データタイプ | フォーマット | 説明 |
|---|---|---|
| テキスト | 文字列 | 試験データアイテムについては、テキストをコードリストまたはURLデータタイプとして表現することができます。ステータスは名前と値で表現されます。例えば:submitted__v |
| 数字 | 桁 | 定義された精度および/または長さ |
| 日付 | システム日付はYYYY-MM-DD形式で表示されます。各臨床データには、派生/ISO8601日付と入力された生の日付の2つの列があります。 | 各日付には2つの列があり、ISO8601形式とRAW形式が得られます。例えば: BIRTHDT: 1990-01-25 と BIRTHDT_RAW: 25-Jan-1990 |
| 日時 | システムのデータタイムは UTC タイムゾーンです。各臨床日時データには、派生/ISO8601日時と入力された生の日時という2つの列があります。 | 各データタイムには2つの列があり、ISO8601形式とRAW形式が得られます。例えば:LBDTC: 2021-01-01T12:00:00 および BIRTHDT_RAW: 01-Jan-2021 12:00:00: |
| Time | HH:mm:ss | 標準フォーマット、ISO8601 |
| 不明 | 日が不明な日付の場合、派生日付形式は2024-06-01、RAW日付形式はUN-Jun-2024です。 日が不明な日付時刻の場合、派生日付時刻形式は2024-06-01T00:00:00、RAW日付時刻形式はUN-Jun-2024 UN:UN:UNです。 月+日が不明な日付の場合、派生日付形式は2024-01-01、RAW日付形式はUN-UNK-2024です。 月+日が不明な日付時刻の場合、派生日付時刻形式は2024-01-01T00:00:00、RAW日付時刻形式は UN-UNK-2024 UN:UN:UNです。 時刻が不明な場合、派生日付時刻形式は2024-06-02T00:00:00となり、RAW日付時刻形式は02-Jun-2024 UN:UN:UNとなります。 | RAWデータと日時出力が未知の日付と日時を表現する方法。派生した日付と日時については、システムは不明な部分(月、日、または時刻)をUTCの1月1日00:00:00にデフォルト設定します。 |
| ブーリアン | True/False | |
| 単位 | (item)_UOM (item)_TRANSLATED (item)_UOM_TRANSLATED | 各ユニットアイテムには、ユニット値、翻訳値、翻訳されたユニット値があります。これらは、臨床項目名に接尾辞を付加することで示されます。測定単位(UOM)と翻訳された測定単位には、単位ラベルが表示されます。 |
| コードリスト | (item) (item)_DECODE | コード値はアイテム値です。DECODEまたはラベルは、アイテム名に接尾辞を追加して動的に追加される2番目の列です。例:ethnicity_DECODE |
運用 &システムデータセット
SFF ZIPパッケージには、試験データとともに、運用データを含む複数のシステムデータセットが含まれています。
システムデータセットは、特定の EDC オブジェクトに関連するデータを提供し、研究内のすべての対象の進捗状況を追跡します。ZIPパッケージには自動的に次のファイルが含まれます。
- SYS_EVENTS.csv
- SYS_FORMS.csv
- SYS_SUBJECTS.csv
- SYS_ILB.csv
- SYS_LINKS.csv
- SYS_SITES.csv
- SYS_PD.csv
- QUERIES.csv
- QUERY_MSGS.csv
SYS_EVENTS
SYS_EVENTSデータセットは、特定の症例に関連するイベントおよびイベントグループについて、現在のステータスと変更理由を記載しています。
次のイベントステータスが含まれています。
- blank__v (空白)
- submitted__v (提出済み)
- in_progress__v (進行中)
- planned__v (計画)
- did_not_occur__v (発生せず)
SYS_EVENTS列のリストは以下の通りです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| EGROUPNAME | テキスト | 事象グループ名 |
| EGROUPORDER | 数字 | イベントグループ順序 |
| EGSEQ | 数字 | 事象グループ順序 |
| EventName | テキスト | 事象名 |
| EVENTORDER | 数字 | イベント順序 |
| EVENTDT | 日付 | イベント日付 |
| VISMETHOD | テキスト | 訪問方法 |
| PLANNEDDT | 日付 | 予定日 |
| OVERDUEDT | 日付 | イベント期限日 |
| EVENTSTATUS | テキスト | イベントステータス |
| EVENTRESTRICTED | ブーリアン | イベント制限あり |
| CHANGEREASON | テキスト | イベント変更理由 |
| EXPFORMS | 数字 | Expected Number of Forms |
| 機能停止 | ブーリアン | イベントフリーズ済み |
| FROZENDT | 日時 | 日時イベントがフリーズしています。 |
| ロック済み | ブーリアン | イベントロック済み |
| LOCKEDDT | 日時 | 日時イベントがロックされています。 |
| SIGNED | ブーリアン | イベントが署名済み |
| SIGNEDDT | 日時 | 日時イベントに署名済み |
| EVENTDTLASTMODDT | 日時 | イベントの日付 最終更新日時 |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
SYS_FORMS
SYS_FORMSデータセットは、症例データを含むすべてのフォームの概要を提供します。これには、フォームのステータス、SDVおよびDMRのフォームレベルのレビューステータス、フォームレベルの意図的に空白にする(ILB)情報が含まれます。
次のフォームステータスが含まれています:
- blank__v (空白)
- submitted__v (提出済み)
- in_progress__v (進行中)
- in_progress_post_submit__v (編集中)
SYS_FORMS列のリストは以下の通りです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| EGROUPNAME | テキスト | 事象グループ名 |
| EGSEQ | 数字 | 事象グループ順序 |
| EventName | テキスト | 事象名 |
| FORMNAME | テキスト | フォーム名 |
| FSEQ | 数字 | フォーム順序 |
| FORMSTATUS | テキスト | フォームステータス |
| FORMRESTRICTED | ブーリアン | フォーム 制限 |
| CREATEDDT | 日時 | フォーム作成日 |
| FIRSTSUBMITDT | 日時 | フォーム 最初送信日 |
| LASTSUBMITDT | 日時 | フォーム 最終送信日 |
| NUMSUBMITS | 数字 | フォーム送信数 |
| OVERDUEDT | 日付 | フォーム 期限日 |
| CHANGEREASON | テキスト | フォーム変更理由 |
| SDVOVRPLAN | テキスト | SDV プランの上書き |
| SDVREQ | ブーリアン | 必須 SDV |
| SDVCOMP | ブーリアン | SDV 完了 |
| FIRSTSDVDT | 日時 | 初期 SDV 日付 |
| SDVCOMPDT | 日時 | SDV完了日時 |
| SDVUSERMODDT | 日時 | SDVユーザー 変更日 |
| DMROVRPLAN | テキスト | DMR プランの上書き |
| DMRREQ | ブーリアン | 必須 DMR |
| DMRCOMP | ブーリアン | DMR 完了 |
| FIRSTDMRDT | 日時 | 初期 DMR 日付 |
| DMRCOMPDT | 日時 | DMR完了日時 |
| DMRUSERMODDT | 日時 | DMRユーザー 変更日 |
| 機能停止 | ブーリアン | フォームフリーズ済み |
| FROZENDT | 日時 | 日時フォームがフリーズ |
| ロック済み | ブーリアン | フォームロック済み |
| LOCKEDDT | 日時 | 日時フォームがロックされています。 |
| SIGNED | ブーリアン | フォーム署名済み |
| SIGNEDDT | 日時 | 日時フォームに署名済み |
| ILB | ブーリアン | 意図的に空欄のままにしておくフォーム |
| ILBREASON | テキスト | フォームの意図的に空白のままにされている理由 |
| FORMLASTMODBY | テキスト | フォーム 最終更新者 |
| FORMLASTMODDT | 日時 | フォーム 最終変更日時 |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
SYS_SUBJECTS
SYS_SUBJECTSデータセットには、試験内の症例に関するデータが含まれています。 (YNA comment: Need to be changed globally.)
SYS_SUBJECTS列のリストは以下の通りです:
| 列 | データタイプ | 説明 |
|---|---|---|
| CASEBOOKVER | 数字 | 症例のケースブックバージョン番号 |
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| SUBSTATUS | テキスト | 症例ステータス |
| SUBRESTRICTED | ブーリアン | 被験者に制限あり |
| SDVPLAN | テキスト | 被験者に割り当てられた SDV 計画 |
| DMRPLAN | テキスト | 被験者に割り当てられた DMR 計画 |
| 機能停止 | ブーリアン | 被験者固定 |
| ロック済み | ブーリアン | 被験者ロック済み |
| SIGNED | ブーリアン | 被験者署名済み |
| LATESTARM | テキスト | 最新群 |
| LATESTCOHORT | テキスト | 最新コホート |
| LATESTSUBSTUDY | テキスト | 最新下位試験 |
| CNSNTDT | 日付 | 初回同意日 |
| SCRDDT | 日付 | スクリーニング実施日 |
| SCRFAILDT | 日付 | スクリーニング不合格日 |
| ENRDDT | 日付 | 登録日 |
| RDMDDT | 日付 | 無作為化日 |
| STARTTRTDT | 日付 | 治療開始日 |
| ENDTRTDT | 日付 | 治療終了日 |
| WTHDRWNDT | 日付 | 回収日 |
| STARTFLLWUPDT | 日付 | フォローアップ開始日 |
| LOSTFLLWUPDT | 日付 | フォローアップ喪失日 |
| CMPLTDT | 日付 | スタディ終了日 |
| SUBLASTMODBY | テキスト | 被験者最終更新者 |
| SUBLASTMODDT | 日時 | 被験者最終変更日時 |
| ROWWRITEDT | 日時 | ファイルに書き込まれた行の日時 |
| ROWID | テキスト | 行 ID |
SYS_ILB
SYS_ILBデータセットには、すべてのスタディ実施施設における各症例の特定のフォーム上の関連アイテムの「故意に未記入のままにされたデータ」が含まれています。提出済みステータスのデータが含まれています。
SYS_ILB列のリストは以下の通りです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| EGROUPNAME | テキスト | 事象グループ名 |
| EGSEQ | 数字 | 事象グループ順序 |
| EventName | テキスト | 事象名 |
| FORMNAME | テキスト | フォーム名 |
| FSEQ | 数字 | フォーム順序 |
| IGROUPNAME | テキスト | 項目グループ名 |
| IGSEQ | 数字 | 項目グループ順序 |
| ITEMNAME | テキスト | 項目名 |
| ILBREASON | テキスト | 未実施理由 |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
SYS_LINKS
SYS_LINKSデータセットには、フォーム間リンクのために試験データに追加されたリンクに関する情報が含まれています。
SYS_LINKS列のリストは以下の通りです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| EGROUPNAME | テキスト | 事象グループ名 |
| EGSEQ | 数字 | 事象グループ順序 |
| EventName | テキスト | 事象名 |
| FORMNAME | テキスト | フォーム名 |
| FSEQ | 数字 | フォーム順序 |
| LINKID | テキスト | リンク Vault ID |
| LINKCREATEDBY | テキスト | リンク作成者 |
| LINKCREATEDDT | 日時 | リンク作成日時 |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
SYS_SITES
このデータセットには、スタディ実施施設に関するデータが含まれています。
SYS_SITES列のリストは以下の通りです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SITENAME | テキスト | 施設名 |
| SITEPI | テキスト | 施設試験責任医師長 |
| SITESTATUS | テキスト | 施設ステータス |
| SITETIMEZONE | テキスト | 施設タイムゾーン |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
SYS_PD
SYS_PDデータセットは、特定の症例に関連するプロトコール逸脱について、現在のステータスと変更理由を記載しています。
SYS_PD列のリストは以下の通りです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ実施施設の3文字の国コード |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| EGROUPNAME | テキスト | 事象グループ名 |
| EGSEQ | 数字 | 事象グループ順序 |
| EventName | テキスト | 事象名 |
| FORMNAME | テキスト | フォーム名 |
| FSEQ | 数字 | フォーム順序 |
| IGROUPNAME | テキスト | 項目グループ名 |
| IGSEQ | 数字 | 項目グループ順序 |
| ITEMNAME | テキスト | 項目名 |
| PDNAME | テキスト | プロトコール逸脱ID(名前) |
| PDTYPE | テキスト | プロトコール逸脱(PDが件名、フォーム、または項目で作成された場合) |
| PDSUM | テキスト | プロトコール逸脱概要 |
| PDDT | 日付 | 逸脱日 |
| PDDTID | 日付 | 日付特定済み |
| PDCAT | テキスト | プロトコール逸脱カテゴリ(ラベルではなくコード) |
| PDSUBCAT | テキスト | プロトコール逸脱サブカテゴリ(ラベルではなくコード) |
| PDSEV | テキスト | プロトコール逸脱の重要度(ラベルではなくコード) |
| PDDESC | テキスト | プロトコール逸脱の説明 |
| PDSTATUS | テキスト | プロトコール逸脱ステータス(選択リスト) |
| PDRES | テキスト | プロトコール逸脱の解決策 |
| PDRULE | テキスト | プロトコル逸脱ルール名(IDではなく名前を表示) |
| PDRESTRICTED | ブーリアン | プロトコル逸脱制限あり |
| INACTBYSYS | ブーリアン | システムによって無効化 |
| LASTINACTDT | 日時 | 最後に無効化された日付 |
| LASTREASON | テキスト | 最終変更の理由 |
| PDCREATEDBY | テキスト | プロトコール逸脱の作成者(ユーザ名) |
| PDCREATEDDT | 日時 | プロトコール逸脱の作成日時 |
| USERMODBY | テキスト | プロトコール逸脱のユーザ変更者(ユーザ名) |
| USERMODDT | 日時 | プロトコール逸脱のユーザ変更日時 |
| PDLASTMODBY | テキスト | プロトコール逸脱の最終変更者(ユーザ名) |
| PDLASTMODDT | 日時 | プロトコール逸脱の最終変更日時 |
| ORIGINSYS | テキスト | プロトコル逸脱の起源システム |
| ORIGINID | テキスト | プロトコール逸脱の起源ID |
| ORIGINNAME | テキスト | プロトコール逸脱の起源の名前 |
| SYSID | テキスト | プロトコール逸脱ID |
| SOURCE | テキスト | PDのフォームのソース(EDC、eCOAなど) |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時(システム生成) |
| ROWID | テキスト | 行 ID |
クエリファイル
クエリファイルには、スタディで作成された各クエリの記録が含まれています。また、クエリがいつ開かれ、いつ閉じられ、誰が作成したかなどの運用指標も含まれています。このデータを使用して、下流のレポートや分析用の追加指標を計算することができます。
クエリファイル内の列のリストは次のとおりです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| EGROUPNAME | テキスト | 事象グループ名 |
| EGSEQ | 数字 | 事象グループ順序 |
| EventName | テキスト | 事象名 |
| EVENTDT | 日付 | イベント日付 |
| EVENTSTATUS | テキスト | イベントステータス |
| FORMNAME | テキスト | フォーム名 |
| FSEQ | 数字 | フォーム順序 |
| IGROUPNAME | テキスト | 項目グループ名 |
| IGSEQ | 数字 | 項目グループ順序 |
| ITEMNAME | テキスト | 項目名 |
| QUERYNAME | テキスト | クエリ名 |
| QUERYID | テキスト | クエリ ID |
| ORIGINSYS | テキスト | 元のシステム |
| ORIGINID | テキスト | IDの生成元 |
| ORIGINNAME | テキスト | 発案者名 |
| QUERYSTATUS | テキスト | クエリステータス |
| QUERYTYPE | テキスト | クエリタイプ |
| QUERYRESTRICTED | ブーリアン | 制限ありクエリ |
| MANUALQUERY | ブーリアン | 手動またはシステムクエリ |
| RULEDEF | テキスト | ルール 定義 名 |
| TRIGID | テキスト | トリガー名 |
| FIRSTQUERYMSG | テキスト | 最初のクエリメッセージ |
| QUERYTEAM | テキスト | クエリチーム |
| QUERYROWEXTERNALID | テキスト | クエリ行外部ID(Veeva EDC以外のデータに対するクエリで設定されている場合、入力されます) |
| QUERYCREATEDBY | テキスト | クエリ作成者 |
| QUERYCREATEDDT | 日時 | クエリ作成日時 |
| QUERYLASTCLOSEDDT | 日時 | クエリ 最後のクローズ日時 |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
クエリメッセージ
クエリメッセージファイルは、特定のクエリに関連する各メッセージを表示することで、クエリファイルを補完します。クエリIDをキーとして使用して、クエリファイルとクエリメッセージファイルの間の対応付けを行うことができます。
クエリメッセージファイル内の列のリストは次のとおりです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 試験名 (YNA comment: Need to be changed globally.) | テキスト | 試験名 (YNA comment: Need to be changed globally.) |
| SiteCountry | テキスト | スタディ施設の3文字の国コード (YNA comment: Need to be changed globally.) |
| SITENUM | テキスト | 施設番号 |
| SUBJID | テキスト | 患者名 (YNA comment: Need to be changed globally.) |
| QUERYNAME | テキスト | クエリ名 |
| QUERYID | テキスト | クエリ ID |
| QUERYMSGSTATUS | テキスト | メッセージステータスクエリ |
| RESTRICTEDMSG | ブーリアン | 制限付きクエリメッセージ |
| QUERYMSG | テキスト | クエリメッセージ |
| QUERYMSGBY | テキスト | メッセージ作成者 |
| QUERYMSGDT | 日時 | 問い合わせメッセージ日付 |
| QUERYTEAM | テキスト | メッセージを作成したチームに問い合わせる |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
参照データファイル
参照データには、ラベル、表示上書きラベル、削除、ローカルラボユニット定義、ローカルラボコードリスト定義のファイルが含まれています。
DELETESファイルに関する情報は、「増分抽出」を参照してください。
ラベル
ラベルファイルには、イベントグループ、イベント、フォーム、アイテムグループ、アイテムなどの試験定義オブジェクトに関連するラベルが表示されます。 (YNA comment: Need to be changed globally.) このファイルには最新のスタディデザインバージョンのラベルが含まれており、SFFのZIPパッケージのフルバージョンでのみ入手可能です。ラベルは、使用中のVaultで設定されている言語で表示されます。 (YNA comment: Need to be changed globally.)
ラベルファイル内の列のリストは次のとおりです:
| 列 | データタイプ | 説明 |
|---|---|---|
| 名前 | テキスト | オブジェクト名 |
| ラベル | テキスト | オブジェクトラベル |
| タイプ | テキスト | オブジェクトタイプ(イベントグループ、イベント、フォーム、アイテムグループ、アイテムなど) |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
ラベルファイルの例:
| 名前 | ラベル | タイプ | ROWWRITEDT | ROWID |
|---|---|---|---|---|
| 事前審査 | 事前審査 | 事象グループ | 2024-06-01T21:06:00Z | prescreening_eventgroup |
| visit1 | 来院 1 | 事象 | 2024-06-01T21:06:00Z | visit1_event |
| physical_exam | 身体所見 (YNA comment: Need to be changed globally.) | フォーム | 2024-06-01T21:06:00Z | physical_exam_form |
| ig_prescreen | 事前審査 | 項目グループ | 2024-06-01T21:06:00Z | ig_prescreen_itemgroup |
| dob | 生年月日 | 項目 | 2024-06-01T21:06:00Z | dob_item |
| in_progress__v | 進行中 | event_status | 2024-06-01T21:06:00Z | in_progress__v_event_status |
| submitted__v | 送信済み | event_status | 2024-06-01T21:06:00Z | submitted__v_event_status |
| blank__v | 空白 | event_status | 2024-06-01T21:06:00Z | blank__v_event_status |
| did_not_occur__v | 未実施 | event_status | 2024-06-01T21:06:00Z | did_not_occur__v_event_status |
| planned__v | 予定 | event_status | 2024-06-01T21:06:00Z | planned__v_event_status |
Row IDは、上記の例では連結された文字列である可能性があります。
ラベルを上書き
オーバーライドラベルファイル内の列のリストは次のとおりです:
| 列 | データタイプ | 説明 |
|---|---|---|
| SRCDEFINITION | テキスト | ソース(オブジェクト)定義名 |
| SRCLABELTYPE | テキスト | ソース(オブジェクト)ラベルタイプ:イベントグループなど |
| TARGETDEFINITION | テキスト | ターゲット(オブジェクト)定義名 |
| TARGETLABELTYPE | テキスト | 対象(オブジェクト)ラベルの種類:イベントなど |
| TARGETOVERRIDELABEL | テキスト | ターゲット(オブジェクト) オーバーライドラベル |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
ローカルラボユニット
ローカルラボユニットファイルは、ローカルラボモジュールに関連するユニット定義を表示します。
ラボユニットファイル内の列のリストは次のとおりです:
| 列 | データタイプ | 説明 |
|---|---|---|
| UNITNAME | テキスト | 単位 定義 名 |
| UNITEXTID | テキスト | 単位定義外部 ID |
| UNITTYPE | テキスト | 単位定義タイプ |
| UNITITEMCODE | テキスト | 単位項目定義コーダー |
| UNITITEMDECODE | テキスト | 単位アイテム定義コーダー |
| UNITITEMEXTID | テキスト | 単位アイテム定義外部 ID |
| UNITITEMABBR | テキスト | 単位アイテム定義略称 |
| UNITITEMSTANDARD | ブーリアン | 単位アイテム定義標準 |
| UNITITEMCONV | テキスト | 単位 項目 定義 変換式 |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
ローカルラボコードリスト
ローカルラボコードリストファイルは、ローカルラボモジュールに関連するコードリスト定義を表示します。
ローカルラボコードリストファイル内の列のリストは次のとおりです:
| 列 | データタイプ | 説明 |
|---|---|---|
| CODELISTNAME | テキスト | コードリスト 定義 名 |
| CODELISTEXTID | テキスト | コードリスト定義外部 ID |
| CODELISTITEMCODE | テキスト | コードリスト項目定義コーダー |
| CODELISTITEMDECODE | テキスト | デコードリスト項目定義コーダー |
| ROWWRITEDT | 日時 | 行がファイルに書き込まれた日時 |
| ROWID | テキスト | 行 ID |
エラー処理に関する情報は、CDMS開発者ポータルのCDB固有のエラーセクションを参照してください。
試験デザインの変更を理解する
EDC で試験デザインに変更が生じた場合、新しいケースブックが公開されます。デザイン変更がCDBに取り込まれCDBが適用されると、APIレスポンスはfull_requiredフィールドをtrueとしてフルおよび差分抽出パッケージの両方で返します。full_requiredがtrueの場合、パッケージは生成されるますが空です。これは、パッケージが 48 時間アクセス可能な状態にあるためです。例えば、この機能がオフになっていても、48 時間の制限時間に達していなければ、空のパッケージを返却できます。
API のレスポンスは、抽出が差分かフルかによって解釈が異なります:
- 差分パッケージの場合、true のレスポンスは、インクリメンタルな変更が停止したことを意味し、更新を再開するには次のフル SFF パッケージを待つ必要があります。
- フルパッケージの場合、true のレスポンスがあれば、パッケージが最新のフルセットでデータをリフレッシュするために使用できることを意味します。