创建研究填写指南
使用 Veeva EDC 工作室,你可以在设计过程中的任何时间点轻松生成研究文档。在当前版本中,有四种类型的研究规范可用:所有 CRF PDF、唯一 CRF PDF、SDS(研究设计规范)(Excel™)和 CDE(病例手册设计导出)。
所有 & 唯一 CRF
可以创建包含研究中所有病例报告表单(CRF)的 PDF 文件。可以选择在创建过程中包含注释。注释包括有关表单上条目字段的其他详细信息,例如编码值、最大长度或条目字段是否必填。
为所有 CRF PDF 和唯一 CRF PDF 生成的 PDF 反映了 EDC 应用程序的其他区域中提供的空白详细信息 PDF。
有两种类型的 PDF 可用:
- 所有 CRF PDF:表单按其在研究计划中的出现顺序排序,并针对其在计划中发生的每个事件重复出现。
- 唯一 CRF PDF:表单按字母顺序排序,即使在研究计划中被多次使用也不会重复。
注释
可以选择在 PDF 中包含常规注释和导出注释(如果可用)。还可以选择缩进渐进显示条目。
常规注释
在当前版本中,Vault 添加了下表中所述的注释。请注意,用大括号括起的值(例如,{最小值})是令牌,将替换为研究设计中的实际值。
| 注释 | 描述 |
|---|---|
| 外部 ID= | 显示每个设计组件的外部 ID(以前称为 OID)值。 |
| 编码列表: | 每个编码列表条目 注释都包含该选项的编码值。这表示规则评估所针对的存储值。 |
| 编码列表样式:单选按钮 – 横向 | 当编码列表类型的条目 使用水平单选按钮时显示。 |
| 编码列表样式:单选按钮 – 纵向 | 当编码列表类型的条目 使用垂直单选按钮时显示。 |
| 最大长度: | 为文本类型条目 字段设置的最大长度。 |
| 最大长度.精确度 | 为数字类型和单位类型条目 字段设置的最大长度 和精确度。 |
| 只读 | 此注释显示在任何只读 类型的条目 上。 |
| 编码的相关条目 | 此注释显示在标记为编码逐字记录相关条目 的任何条目 上。 |
| 受限 | 显示“是”或“否”,具体取决于表单 是否受限(设盲)。这基于表单定义 的受限(Restricted)属性。了解有关受限表单 数据的更多信息。 |
| 必填 | 此注释显示在选中了必填(Required)属性复选框的任何条目 上。 |
| 范围,{最小值} - {最大值} | 此注释显示在同时设置了最小和最大范围属性的任何条目 上。 |
| 范围必须为 > = {最小值} | 此注释显示在设置了最小值(Minimum Value)属性的任何条目 上。 |
| 范围必须为 < = {最大值} | 此注释显示在设置了最大值(Maximum Value)属性的任何条目 上。 |
| 用于编码的逐字记录(词典 = {词典名称}) | 此注释显示在用作编码逐字记录的任何条目 上。 |
| 为条目选择默认值:{Defaulted Value} | 此注释显示在成像条目上。 |
导出注释
此选项会向 PDF 中的每个条目添加一个注释,以指示主研究提取 CSV 中包含该条目 的位置。例如,出生日期 条目可能具有人口统计信息.DOB 的注释。在此示例中,条目位于人口统计信息 表单的视图中标记为“DOB”的列中。
导出注释仅在启用了“视图集”功能的 Vault 中可用。请联系 Veeva 服务代表了解详细信息。
缩进渐进显示条目
选择缩进渐进显示条目(Indent Progressive Display Items)将缩进已配置为渐进显示的条目,并在控制项 的正下方显示从属条目。了解有关渐进显示的更多信息。
如果未选中此复选框,则 Vault 不会在 PDF 中包含任何指示,表明条目 已配置为渐进显示。
Vault 在 PDF 中只能显示 10 个级别的渐进显示从属关系。如果超过 10 个,则 Vault 会停止缩进第 10 级之后的所有条目。
研究设计规范(SDS)
研究设计规范(SDS)是一个 Microsoft Excel™ 工作簿。该工作簿包含关键研究设计组件的工作表:
- 计划 - 网格:按研究计划中的显示顺序列出研究 中的所有表单定义。
- 计划 - 树:列出所有事件组定义、事件定义 和表单定义,按照研究计划中的显示顺序分组在一起。
- 表单定义:列出研究 中的每个表单定义,其中包括所有表单相关属性的列。
- 评估:列出研究 中已执行的评估 的类型和状态。
- 编码列表:将研究 中的每个编码列表定义 列为标题行,并列出编码列表的每个编码列表条目定义 的行。
- 单位编码列表:将研究 中的每个单位定义 列为标题行,并列出编码列表的每个单位条目定义 的行。
- 审查计划:列出审查计划描述、类型和事件日期。
- 规则(可选):列出研究 中的每个规则定义,其中包括规则详细信息(如规则表达式)和属性的列。
- 病例手册变量:列出研究 中的每个 病例手册变量,其中包括变量详细信息和变量映射条目 或事件日期 的列。
- 研究设置:列出研究 的已配置设置,包括标准日期格式、受试者 ID 生成格式 等。
- 受试者组:列出研究 中的所有受试者组,包括标签、编码、类型 和外部 ID。
- 医疗编码条目(在启用了 Vault Coder 的 Vault 中):列出研究 中所有已配置的医疗编码条目定义。
- 主要导出视图(可选):列出为研究 设置的研究数据提取 视图中的所有列。
- 方案偏离(在启用了“方案偏离”功能的研究 中):列出研究 中方案偏离的所有已配置类别、子类别 和 严重性。
- 本地实验室:列出本地实验室配置设置,包括“系统常规设置(System General Settings)”、“研究常规设置(Study General Settings)”和“临床意义(Clinical Significance)”研究设置。
- 分类:列出所有分类 及其值,以及它们是否处于活动(已启用)状态。
- 摘要:一个摘要表,其中包括 Vault 名称、研究名称、病例手册版本号、研究工作版本号、描述、病例手册定义名称、更改原因、外部 ID 和文档编号。
- 重复事件组:列出研究 中的所有重复事件组定义,包括每个事件组的事件组名称、序列、默认显示、偏移天数、日期范围提早天数 和日期范围推迟天数。
- 集成配置:启用后,列出所有集成配置(程序)。
- 数据加载程序配置(启用时):列出研究的所有数据加载程序配置,包括列映射
- 安全设置:列出研究 的安全设置 值。如果研究未使用安全集成,则不会显示在 SDS 中。
- 安全表单配置:列出研究 的安全表单配置。如果研究未使用安全集成,则不会显示在 SDS 中。
SDS 选项
在 SDS 生成期间,可以选择 包含规则(Include Rules)和包含导出(Include Export)(如果在 Vault 中启用了“视图集”功能)。这会将规则(Rules)(对于包含规则)和主要导出视图(Primary Export View)(对于包含导出)工作表添加到 Excel™ 文件中。
还可以选择包括密钥 和源 详细信息。
- 包括密钥:此选项会添加定义跨 Vault 唯一 ID 和定义私钥 列。跨 Vault 唯一 ID 提供 Vault、研究和记录 ID,并且对于对象的版本是唯一的。私钥 用于跨版本和研究定义对象。
- 包括源:这将添加源密钥的列。该组密钥将对象绑定到其原点,通常是库。这些密钥包括源名称(研究或库集合的名称)、源类型(研究 或库)、源定义名称(源研究或库中对象的当前名称)和源密钥(将对象绑定到源 的跨 Vault 唯一 ID)。
Vault 在计划 - 树、表单定义、规则、编码列表 和单位 工作表中包含这些附加列。
如何创建研究规范
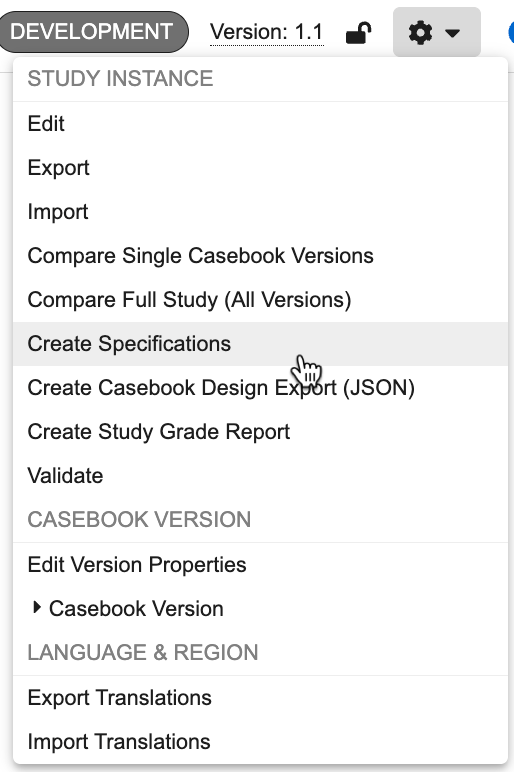
要创建研究规范,请执行以下操作:
- 在工作室(Studio)中导航到研究。
- 可选:要为旧版病例手册生成规范,请从操作(Actions)菜单中选择该版本。
-
在创建规范对话框中,选中要生成的文档类型(所有 CRF PDF(All CRF PDF)、唯一 CRF PDF(Unique CRF PDF)、包括 SDS(Include SDS))。
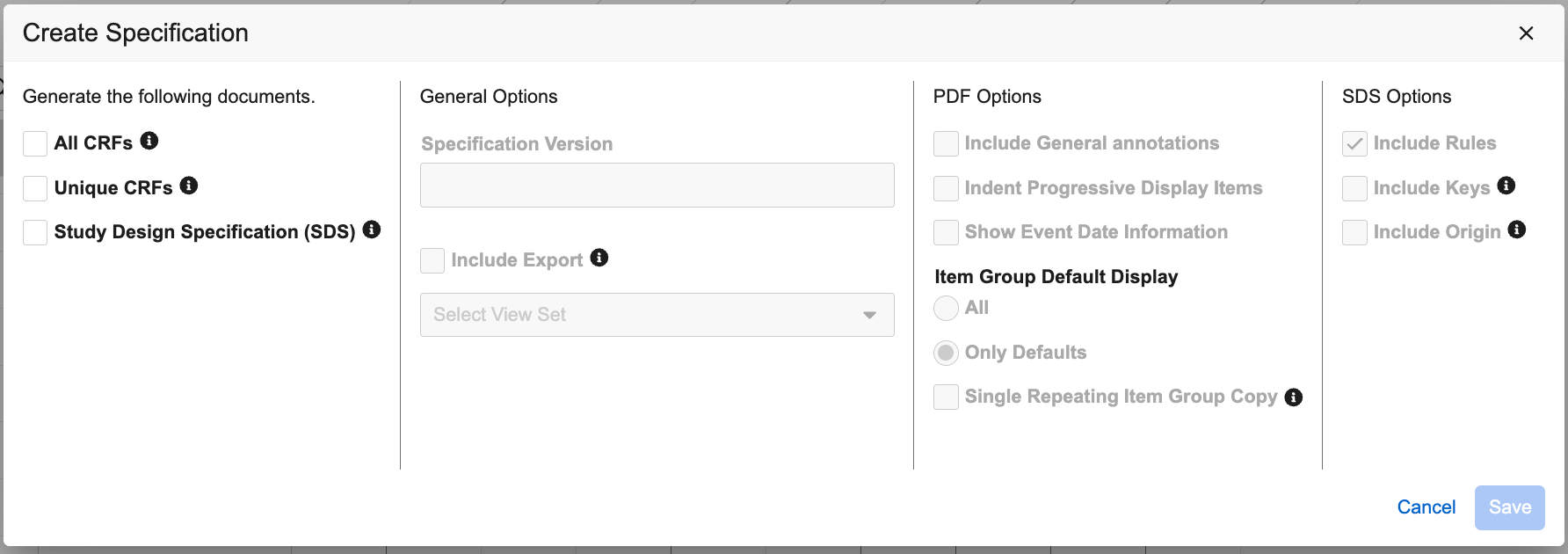
- 可选:输入规范版本(Specification Version)。
- 可选:选择是否包括导出(Include Export)视图集。
- 可选:选择是否包括常规注释(Include General Annotations)。
- 可选:选择是否 缩进渐进式显示项。
- 可选:选择是否显示事件日期信息(Show Event Date Information)。
-
可选:对于条目组默认显示(Item Group Default Display),选择显示所有(All)数据或仅默认值(Only Defaults)。

- 可选:选中单个重复条目组副本(Single Repeating Item Group Copy),可为重复条目组生成单份副本。若未选中,这将在 PDF 中创建重复条目组的额外副本。
- 点击保存。
- Vault 将启动生成研究规范的作业。完成后,Vault 会发送一个通知,其中包含用于下载文件的链接。
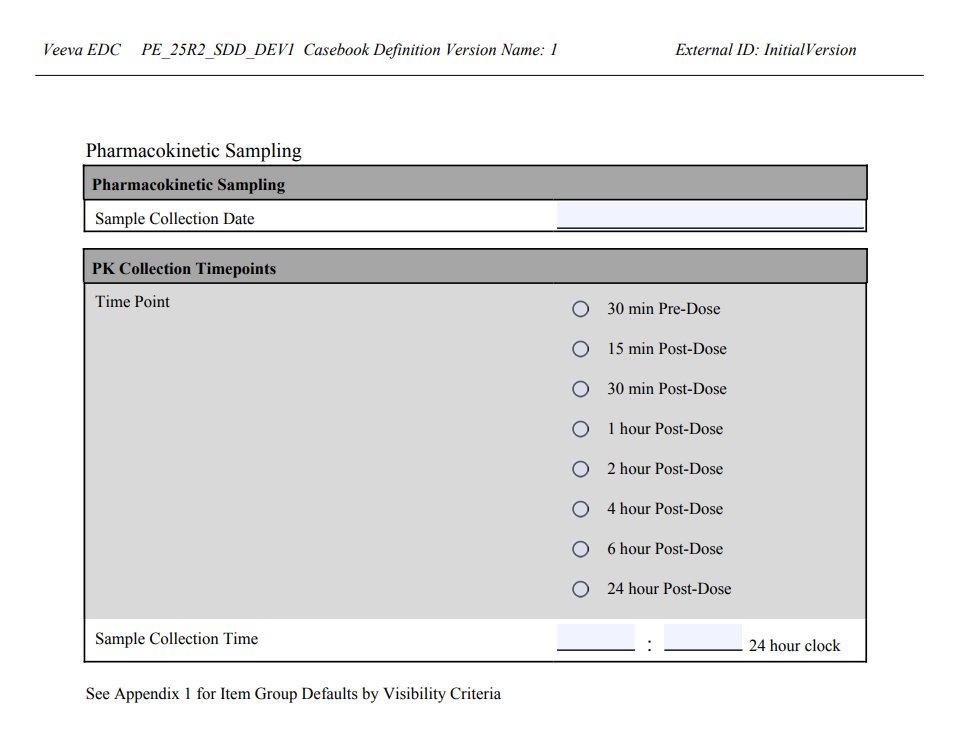
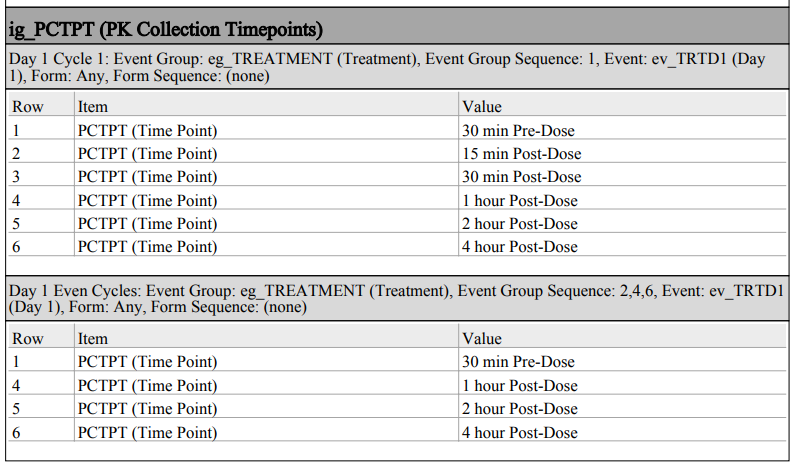
PDF 中条目组默认显示的配置
通过创建规范对话框中的条目组默认显示选项,可配置默认条目组在 PDF 中的显示方式。
以下表格详细说明选择不同选项时,默认数据在输出 PDF 中的呈现形式。
病例手册设计导出
CDE(病例手册设计导出)是特定病例手册版本的研究设计的 JSON 表示形式。可以通过 EDC API 或在工作室中检索 CDE。
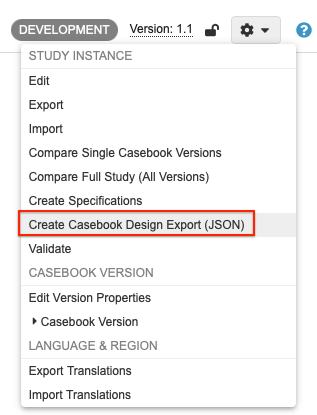
要在工作室中生成 CDE,请执行以下操作:
- 在工作室(Studio)中导航到研究。
- 在创建病例手册设计导出确认对话框中单击创建(Create)。
- Vault 将启动生成 CDE 的作业。完成后,Vault 会发送一个通知,其中包含用于下载文件的链接。
相关权限
默认情况下,具有标准 CDMS Study Designer(CDMS 研究设计者)研究角色的用户可以执行此处所述的操作。