26R1 新增功能
预发布日期:2026 年 3 月 16 日和 23 日 | 发布日期:2025 年 4 月 10 日和 17 日我们很高兴为你带来 Veeva Clinical Data 26R1。请阅读下文了解新功能。你可以在 26R1 功能启用详细信息中找到有关启用新功能的信息。
临床数据
本部分中的功能是对 Veeva EDC 和 CDB 所有应用领域都适用的更改。
文件附件
用例
数据录入现已支持文件附件,无需再使用自定义解决方案或 EDC 外部的第三方文件存储软件。将临床数据文件附加到 eCRF 中后,可在病例手册中纳入受试者原始文件,例如:医学转录文本、病程记录、JPEG 病理切片图像、CT 扫描报告、EKG 心电图 PDF 报告、X 光片放射影像文件,以及医疗设备专有数据文件。随后可直接在 EDC 应用程序中,结合临床数据对这些附件进行查看、审查与核实。在研究期间及研究结束后,支持单个或批量下载,方便导出文件。
描述
工作室
工作室中新增了“文件附件(File Attachment)”条目类型,供研究设计者在表单设计条目时使用。文件附件条目可包含在非重复表单、重复表单以及重复和非重复条目组中。
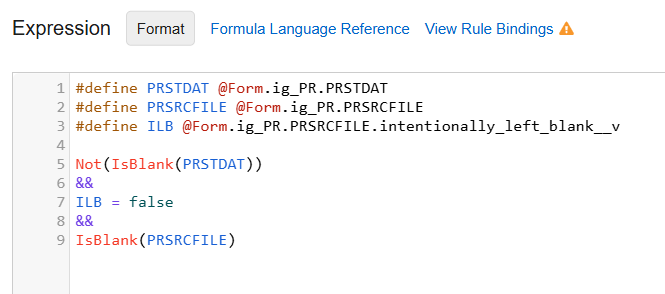
文件附件条目还可在规则中使用:必要检查、渐进显示以及用户定义规则(确认文件已附加)。
文件附件规则示例
为保证系统完整性,存在几项有意的设计限制。文件附件条目类型不能用于以下场景:
- 作为“设置派生值”或“设置受试者状态”规则的目标
- 数据加载程序配置
- 医学评估
研究设计规范(SDS)、差异报告以及空白和带注释的 PDF 均已更新,以包含文件附件条目。这些条目类型也可从库和其他研究中复制,以最大化设计复用。
数据输入
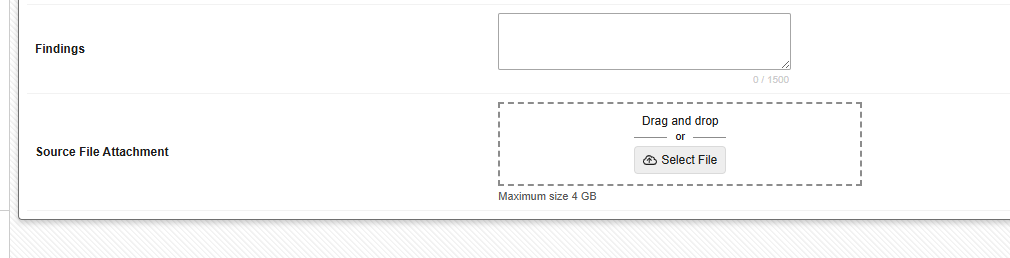
研究中心用户可以通过简单的文件选择器或直接将文件拖放到表单中,从计算机上传最大 4 GB 的文件到已配置的文件附件条目。
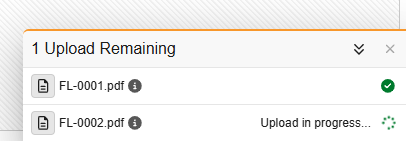
上传开始前,系统会提示用户确认文件不包含任何受保护健康信息(PHI)或个人身份信息(PII)。上传开始后,屏幕右下角会出现专用的“上传抽屉”,用户可在继续处理其他表单的同时跟踪上传进度。在上传过程中,用户可以继续自由使用数据录入。
如需查看可在文件附件查看器中查看的完整文件类型列表,请见此处。所有文件类型均可上传,但以下文件类型会被阻止:
| Format Name | MIME Type(s) |
|---|---|
| 可执行文件 (Windows Executable) |
|
| 可执行与可链接格式 (Linux Executable) |
|
| Apple 磁盘镜像 (macOS Executable) |
|
| Mach-O 格式 (Legacy MacOS Executable) |
|
| DICOM 文件 ——此类文件已通过 Veeva EDC 成像功能支持。 |
|
上传时,系统会对文件附件名称进行去标识化处理,分配一个去标识化的文件名,以确保原始文件名不保留任何潜在的 PHI/PII。与其他条目类似,与文件附件条目相关的所有操作(包括上传、删除和重新添加文件)均记录在审计跟踪中。在表单提交后修改文件时,用户必须输入更改原因。当研究中心无法获取源文件时,文件附件条目也可标记为故意留空(ILB)。
审查
文件成功附加后,监查员或数据管理员等授权用户可使用内置查看器查看文件,或下载文件进行审查。该文件也可在编码器 UI 的表单视图中查看。文件附件条目与其他条目功能相同,可被质疑、标记为方案偏离、纳入 SDV/DMR 审查计划、签署、冻结和锁定。这些最终用户操作也会显示在审计跟踪中。
在数据录入、审查、审计跟踪、列表和提取中,条目将显示系统分配的去标识化名称和文件扩展名。这有助于确保文件名的隐私和安全,并防止文件名中可能包含 PHI/PII 的情况。去标识化的文件名也将显示在 CDB 中。
在 EDC 工具中,研究管理员将看到一个新的“文件附件提取(File Attachment Extract)”作业,该作业将研究中的文件附件批量发送到 Vault 的文件暂存服务器,用户可在该服务器上获取下载的附件。作业完成后,用户会收到电子邮件通知。
API
研究中心用户必须手动附加文件,API 无法将文件添加到条目中。API 调用将支持检索文件附件条目的元数据。
启用和配置
在数据模型 2 研究的工作室配置中自动可用。
了解详细信息
EDC 应用程序标签页新增稳定 URL
用例
作为一项旨在提升产品可访问性的多年工程的一部分,我们正在为 Veeva EDC 改进用户界面和用户体验。作为此项工作的一部分,此版本包含了更稳定的 URL 路由。
描述
Veeva EDC 中的应用程序标签页现在将提供稳定的 URL。有关详细信息,详见下表。
| 新基础 URL | EDC 标签页名称 |
|---|---|
| #/app/page/data-entry | 数据输入 |
| #/app/page/review-studies | 审查(Review)> 我的研究(My Studies) |
| #/app/page/review-study-sites | 审查 > 我的研究中心(My Study Sites) |
| #/app/page/protocol-deviations | 审查 > 方案偏离(Protocol Deviations) |
| #/app/page/assessments | 评估 |
| #/app/page/studio-library | 工作室(Studio)> 库(Library) |
| #/app/page/studio-studies | 工作室 > 研究(Studies) |
| #/app/page/imaging | 成像 |
| #/app/page/coder | 编码器 |
| #/app/page/labs | 实验室 |
| #/app/page/edc-tools | 工具(Tools)> EDC 工具(EDC Tools) |
| #/app/page/coder-tools | 工具 > 编码工具(Coder Tools) |
| #/app/page/system-tools | 工具 > 系统工具(System Tools) |
| #/app/page/safety-integrations | 工具 > 安全集成(Safety Integrations) |
| #/app/page/job-manager | 作业管理器 |
| #/app/page/my-training | 我的培训 |
| #/app/page/clinical-reporting | 临床报告 |
| #/app/page/randomization | 随机化 |
| #/app/page/data-loader | 数据加载器 |
| #/app/page/workbench | 工作台(Workbench (CDB)) |
请注意,现有页面和书签页面将被重定向到新的应用程序标签页。但是,如果使用了非预期的 URL 模式,现有书签可能失效。
启用和配置
此功能自动可用。
数据输入
本部分中的功能是对数据录入(Data Entry)选项卡的变更,该选项卡是研究者和临床研究协调员进行研究数据录入的工作区域。
改进标记为删除的事件组
用例
当动态事件组的规则结果不再成立时,事件组内的数据现在会向研究中心用户提供更清晰的指示。这有助于研究中心更好地查看事件组中可能需要重置数据的事件和表单,同时防止研究中心错误地添加重复事件组的新实例。
描述
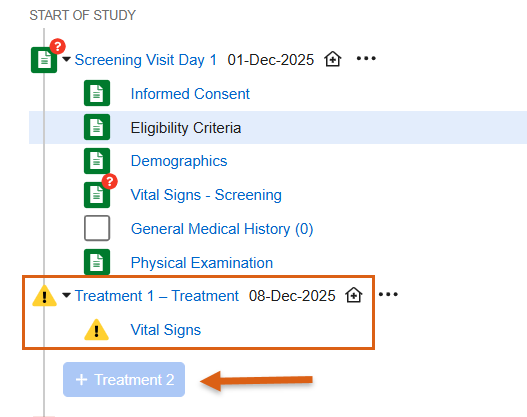
当规则确定某个包含数据的事件组应被移除时,系统现在会阻止向其中添加新表单和事件。对于重复事件组,“+新建(+New)”按钮将被禁用。如果用户尝试添加下一个事件组,他们将看到一条消息:“此操作无法执行,因为根据输入的其他数据,此事件组已不再需要。(This action cannot be performed because this event group is no longer required based on other data entered.)”
当规则条件不再成立时,如果事件组或其关联的事件或表单不包含任何数据,系统将继续像之前一样自动移除它们。
启用和配置
此功能自动可用。
两步事件重置
用例
重置事件和表单时,现在采用两步流程,确保研究中心在重置数据前确实有此意图。此流程在数据来自外部系统(如 IRT 系统)时尤其有用。两步流程在删除数据时提供了更多的控制权和保护,并减少了外部系统重新发送数据的需求。
描述
清除所有表单数据
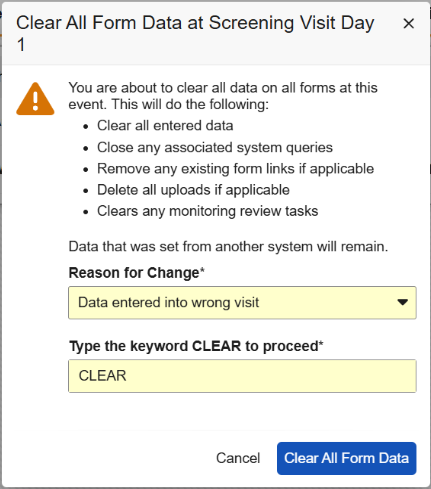
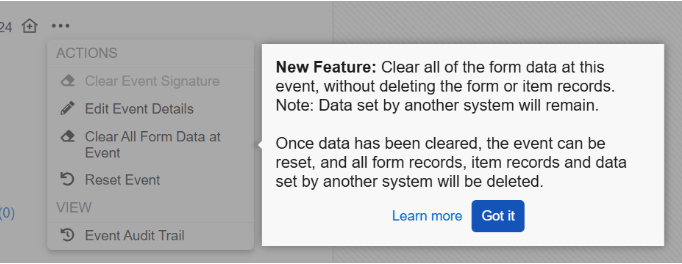
包含一个或多个有数据表单的事件将在事件操作(Actions)菜单中显示一个新选项,称为清除事件中所有表单数据(Clear All Form Data at Event)。研究中心用户在选择此选项时必须提供更改原因,然后输入“CLEAR”一词以确认操作。为了帮助研究中心用户更好地理解此选项,我们新增了一个对话框,详细说明将要执行的操作。对话框中的附加文本告知研究中心,来自其他系统的数据将保留。此步骤允许研究中心重置表单数据,同时保护 IRT 等外部系统传入的数据。
清除表单数据时,事件数据、访问方式以及任何外部数据将保留。如果表单包含指向不同事件中表单的条目-表单链接,则需要在清除数据前移除该链接。同一事件内表单之间的条目-表单链接将被移除。无论表单在同一事件还是不同事件中,表单-表单链接都将被移除。
任何未处理或已回答的手动质疑也将保留。系统质疑将被关闭。
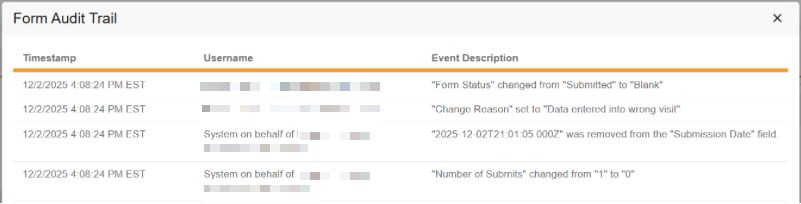
被清除的表单和条目数据将显示在审计跟踪 UI 中。
事件重置
完成清除事件中所有表单数据步骤后,当事件中存在外部数据且没有其他表单数据时,将显示重置事件(Reset Event)选项。重置事件对话框要求研究中心用户输入更改理由并输入“RESET”一词。完全重置事件将执行以下操作:
- 删除所有数据,包括从其他系统设置的值
- 删除所有表单质疑和系统事件质疑
- 删除所有条目和表单记录
- 清除事件日期和访视方式(如适用)
如果没有外部数据,重置事件选项将与清除事件中所有表单数据选项同时显示。
事件重置期间的操作将显示在包含审计的审计导出或 PDF 中。
对于未计划事件,只有在清除事件中所有表单数据步骤后,才能删除该未计划事件。
冻结和锁定数据
用户无法对已冻结(Frozen)或已锁定(Locked)的表单和事件选择清除事件中所有表单数据或重置事件操作。将鼠标悬停在禁用的菜单选项上时,将显示一条信息消息,详细说明研究中心用户无法执行这些操作的原因。
限制数据
如果事件组中没有其他表单数据,用户仍然可以重置包含标记为删除(Marked for Removal)的事件。受限表单将保留,并且仅对具有受限数据访问权限的用户可见。事件仍将被重置。包含受限数据的非计划事件将向受限和非受限用户均显示为标记为删除。
在发布后首次访问事件操作菜单时,将弹出一个显示帮助文本的提示框,向研究中心用户介绍新功能。
启用和配置
此功能将自动可用于使用数据模型 2 的 Vault 和研究。
更新的表单重置和表单 ILB 对话框
用例
我们对“表单重置(Form Reset)”和“表单特意留空(ILB)(Form Intentionally Left Blank (ILB))”对话框中的特定 UI 组件和信息进行了更新,以使其与应用程序中的其他对话框保持一致。
描述
在此版本中,“表单重置”和“表单特意留空(ILB)”对话框中的警告和信息图标已放大,对话框文本后面的黄色和蓝色背景框已改为白色。
对“表单重置”对话框进行了以下更改:
- “关闭所有关联的系统质疑(Close any associated system queries)”已更新为“删除所有系统质疑并关闭手动质疑(Delete all system queries and closed manual queries)”
- “输入 ‘RESET’ 以确认你想重置此表单(Type “RESET†to confirm that you want to reset this form)”已更新为“输入关键字 RESET 以继续(Type the keyword RESET to proceed)”
对“故意留空(Intentionally Left Blank)”对话框进行了以下更改:
- 按钮文本已从“提交(Submit)”更新为“标记为空白(Mark as Blank)”
启用和配置
此功能自动启用。
数据审查
本部分中的功能包括对审查(Review)选项卡(临床研究监查员和数据管理员的工作区域)或数据录入选项卡中审查功能的更改。
快照 UI/UX 一致性与标签更新
用例
此功能更新了快照 UI/UX 的多个方面,以使审查功能在应用程序中保持一致。就绪状态选择的标签也变得更加具体,以帮助明确所选择的快照类型。
描述
创建和修订快照时,保存并获取结果(Save and Get Results)按钮和保存(Save)按钮现在始终处于启用状态。选择任一保存后,任何必填字段、逻辑或超长字符数的屏幕验证错误将显示为红色,并在字段正下方显示相应的错误消息。错误消息的文本也已更新,以与应用程序中的类似消息保持一致。
信息文本和就绪状态标签已更新,以明确现有功能(就绪标准会搜索范围内的事件/表单)。
在“表单”区域下,当包含的表单(Included Forms)字段设置为此范围内的所有事件中的所有表单(All forms in all events within range)时,就绪状态的标签更新如下:
- 事件中所有表单均已完成
- 事件中所有质疑均已回答
- 事件中所有质疑均已关闭
- 事件已完成 SDV
- 事件已完成 DMR
- 事件已签署
当选择仅所选的表单(Selected forms only)时,就绪状态的标签更新如下:
- 表单已完成
- 表单上所有质疑均已回答
- 表单上所有质疑均已关闭
- 表单已完成 SDV
- 表单已完成 DMR
- 表单已签署
就绪状态复选框的更新标签将反映在快照报告中。
启用和配置
此功能自动可用。
报告中的协议偏离名称可打开审查标签页
用例
数据管理员和 CRA 现在可以从“报告(Reporting)”区域的自定义报告中更快速地直接导航至“审查(Review)”标签页中的特定“方案偏离(Protocol Deviation)”记录。方案偏离记录上的改进链接有助于维护用户在 EDC 各标签页间导航时的工作流。
描述
在“报告”中,“方案偏离名称(Protocol Deviation Name)”中带下划线的链接将直接引导你到“审查”标签页中的特定记录。当你查看自定义报告并单击方案偏离名称(例如,类似 PDV-0001 的链接)时,系统现在会自动将你带到“审查”标签页中的该特定方案偏离记录。
启用和配置
此更改自动适用于包含方案偏离名称列的新建和现有自定义报告。
临床编码
以下是 Veeva Coder 的新功能(Veeva Coder 的临床编码区域)。
编码器中的表单至表单可见性
用例
编码员需要完整的临床上下文才能做出准确的编码决策。目前,编码员用户无法轻松查看通过表单至表单链接与编码请求关联表单相链接的表单中的数据。此项增强功能使链接表单中的重要临床上下文 EDC 数据可直接在特定编码请求的操作菜单中访问,通过将所有必要信息集中在一处,提高了编码员的效率和准确性。
描述
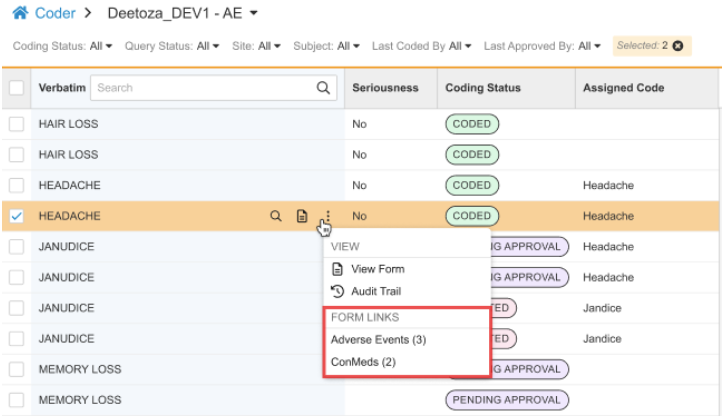
操作菜单中的表单链接
在列表视图中,特定编码请求的操作菜单中新增了“表单链接(FORM LINKS)”子部分。标准 CDMS Clinical Coder(CDMS 临床编码员)、CDMS Clinical Coder Administrator(CDMS 临床编码器管理员)和 CDMS Clinical Coder Manager(CDMS 临床编码器管理员)角色已更新,包含了“查看表单链接(View Form Linking)”权限。这允许编码员查看在 EDC 中通过表单至表单链接关联的数据。
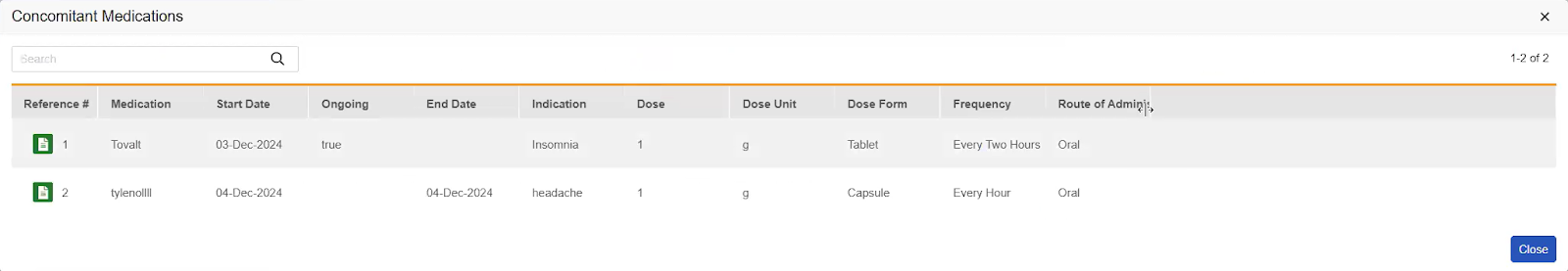
如果存在表单至表单链接,此子部分将为每种已创建的、不同类型的表单至表单链接显示一个操作。仅当数据录入中添加了现有表单链接时,才会显示“表单链接”部分。每个操作的标签是链接表单定义的短标签(Short Label)(例如不良事件(Adverse Events)或 ConMeds)。当为表单(Form)短标签配置了翻译时,将显示翻译后的标签。括号中的计数显示与该当前编码请求关联的该类型表单至表单链接的数量。单击表单链接操作将打开一个对话框,每行显示一个链接表单,列与链接表单上录入的条目一致。
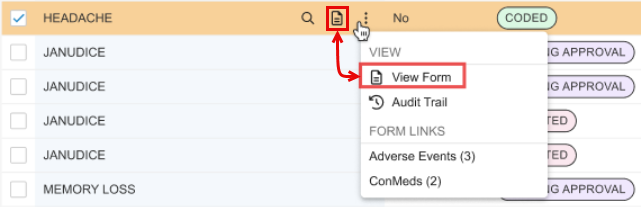
查看表单操作
为保持一致,操作菜单中包含针对编码请求的“查看表单(View Form)”操作。此操作复制了编码请求行中通过单击“查看表单”图标()存在的独立操作。
启用和配置
此功能立即可用。任何自定义角色必须被授予“查看表单链接”权限才能使用此功能。
了解详细信息
WHODrug B3/C3 字段标签更新
用例
2026 年 3 月,WHODrug 将对其数据文件进行更改,这要求 Veeva 更新其界面标签以保持兼容性。此更新确保临床研究符合最新全球词典结构,特别是针对 B3 和 C3 格式。通过采用这些更改,系统可防止 WHODrug 提供的词典文件与研究团队使用的编码环境之间出现不匹配。
描述
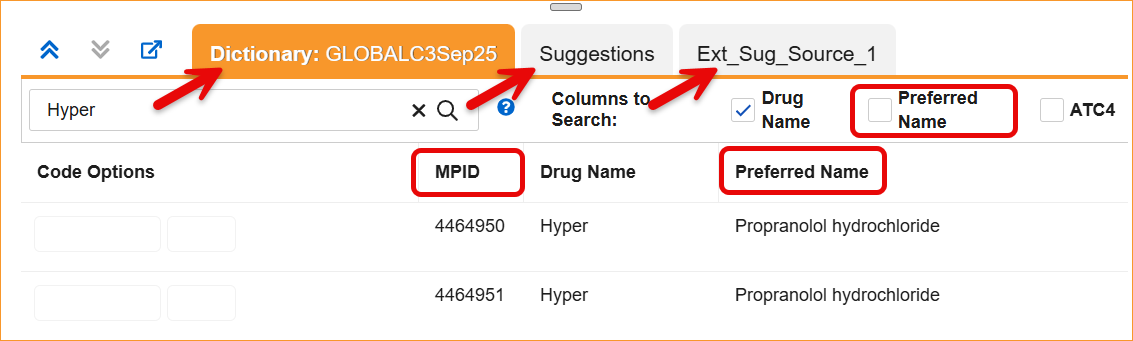
系统现通过一系列系统级的标签和逻辑更新,支持更新的 WHODrug B3 和 C3。最显著的变更涉及重命名标准编码字段,以与新的词典术语保持一致。具体来说,首选名称(Preferred Name)已更新为物质名称(Substance Name),首选代码(Preferred Code)已更新为物质代码(Substance Code),首选(Preferred)已更新为物质(Substance),仿制药(Generic)已更新为通用名称(Generic Name)。对于 C3 词典,MPID 列现已重新标记为 RID。
这些更新体现在以下区域:
- 编码面板:词典(Dictionary)、建议(Suggestion)和外部建议(External Suggestion)面板中的列标题和筛选器现在显示更新后的标签。
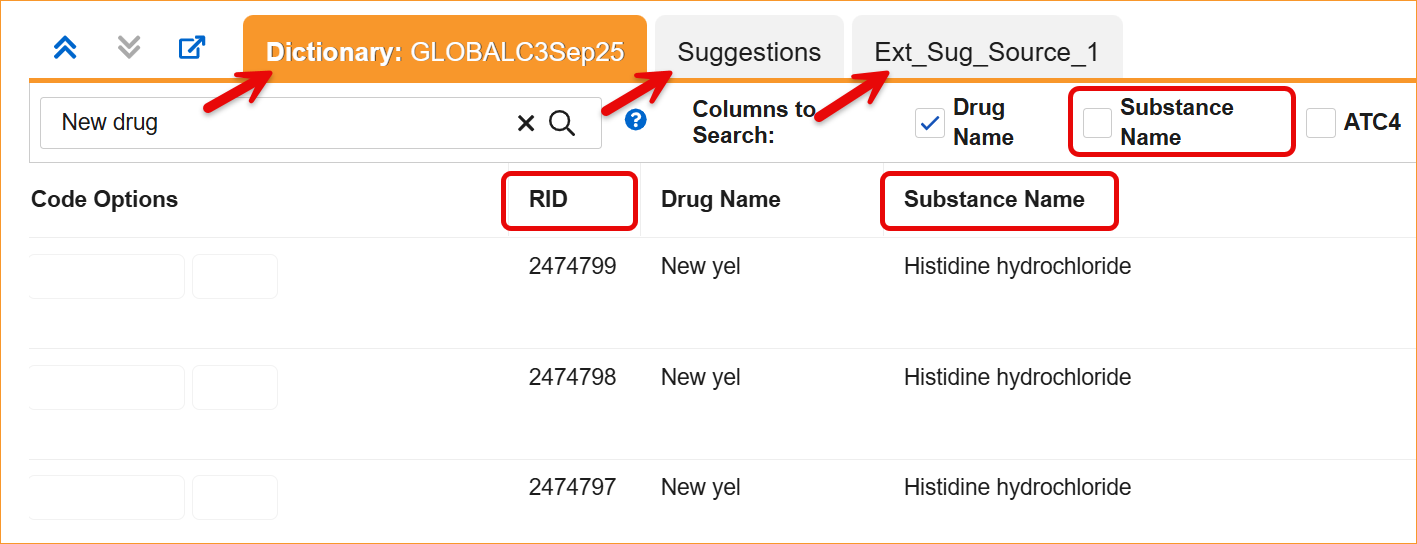
- 同义词列表:导入和导出流程以及同义词列表详细信息网格现在需要使用并显示更新后的标题。
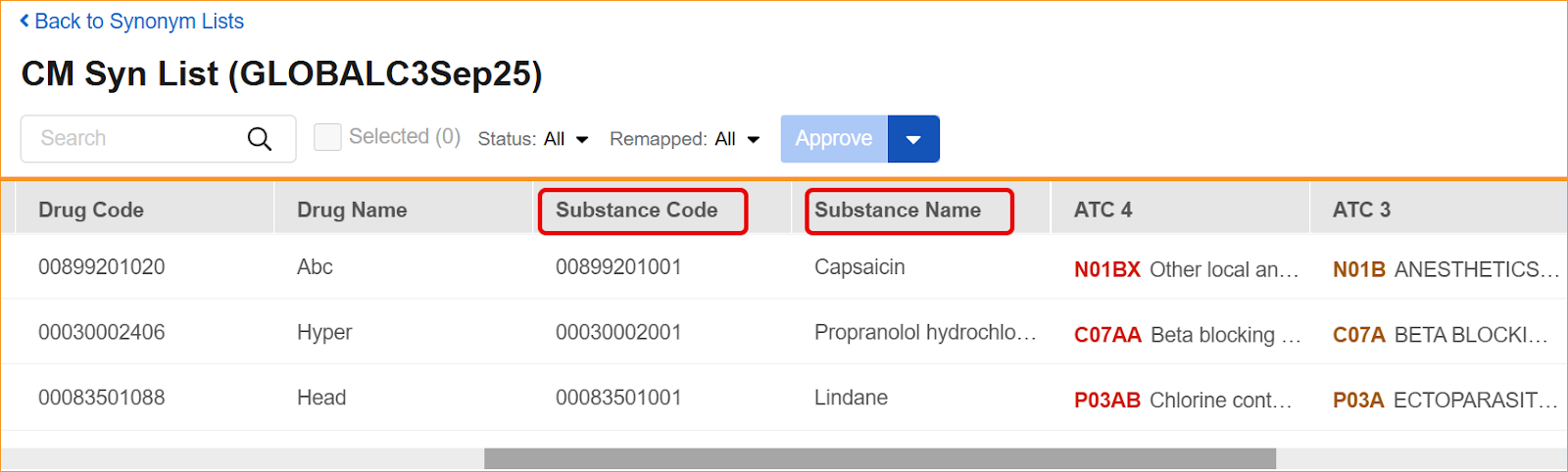
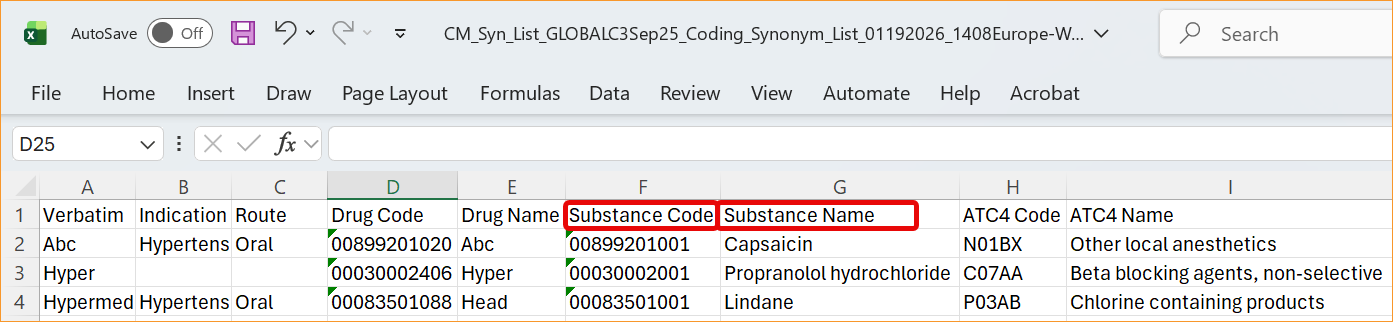
- 报告和提取:标准报告,包括 WHODrug 编码报告(V4)、版本影响报告和唯一术语报告,已更新为新的列别名。
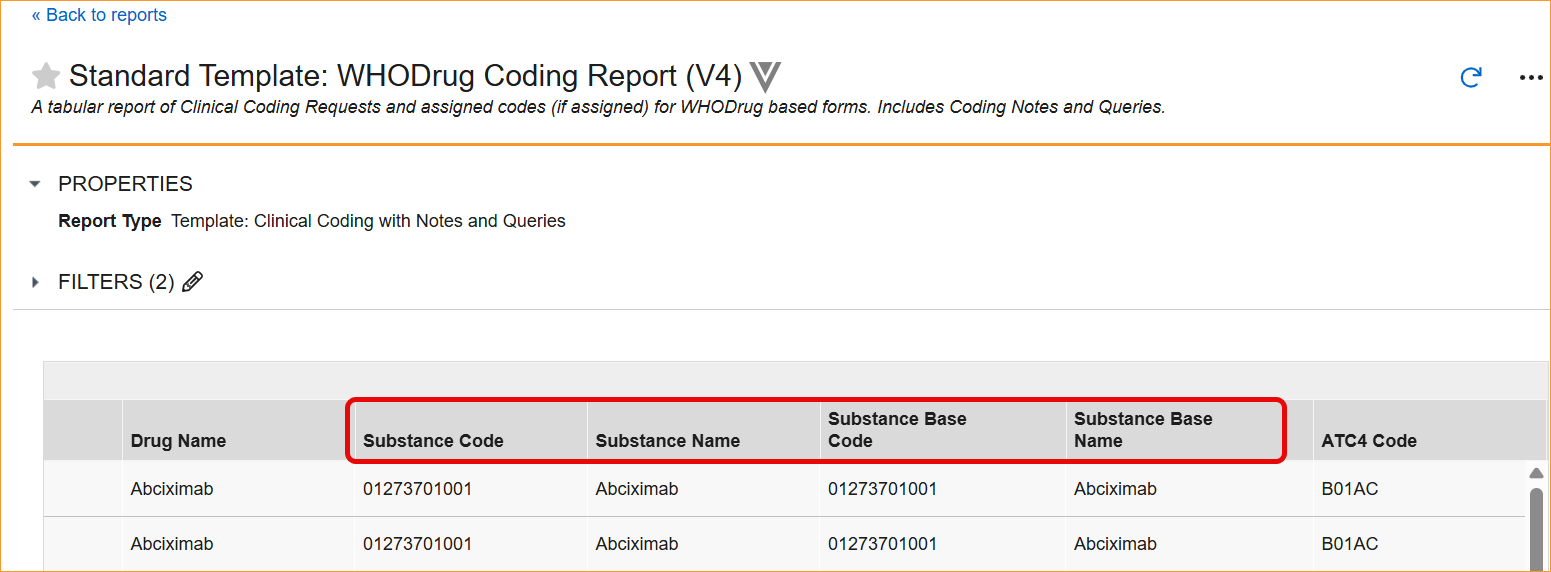
- 研究数据提取(从 26R1 版本开始):使用 WHODrug B3 或 C3 词典的数据集(表单)具有重命名的列标题和 SAS 标签。虽然名称更改为关注物质而非首选术语(首选代码 → 物质代码,首选名称 → 物质名称,首选基础代码(Preferred Base Code)→ 物质基础代码(Substance Base Code),首选基础(Preferred Base)→ 物质基础(Preferred Base)),但底层数据类型和长度保持不变,以确保技术稳定性。
请注意,虽然编码器界面和研究数据提取在 26R1 版本中已更新,但 API 和 CDB 等其他区域将在后续版本中更新以匹配此新术语。
启用和配置
此功能自动可用。
在编码器中显示质疑的冻结和锁定状态
用例
目前,编码器用户无法知道与编码请求关联的 EDC 数据是否被冻结,导致对冻结数据发起质疑后,才通过研究中心回复得知数据需先解冻,造成延误。此功能在 Veeva Coder 的质疑面板中以横幅形式添加了清晰的视觉指示器,使编码员能够快速识别需要其他团队操作的数据。这改进了编码器工作流,并在需要解锁或解冻数据以进行质疑时加快了流程。
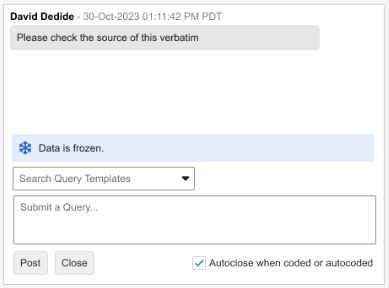
描述
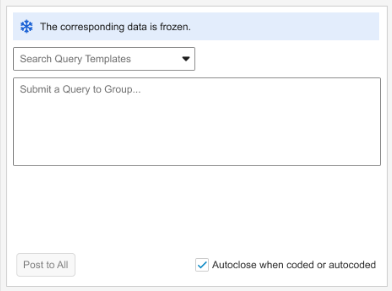
此增强功能在编码器的质疑面板中显示横幅,以显示给定逐字术语的源 EDC 数据的已锁定或已冻结状态。数据已锁定时的行为保持不变,无法向锁定数据发布质疑。横幅显示在“搜索质疑模板(Search Query Templates)”框或“提交质疑(Submit a Query)”自由文本输入字段的上方。根据视图模式,编码器用户可以看到以下信息:
锁定数据
-
列表模式(List Mode)错误横幅文本:“无法发布、关闭或自动关闭质疑,因为相应的表单已被锁定。(Queries can’t be posted, closed, or autoclosed because the corresponding form is locked.)”
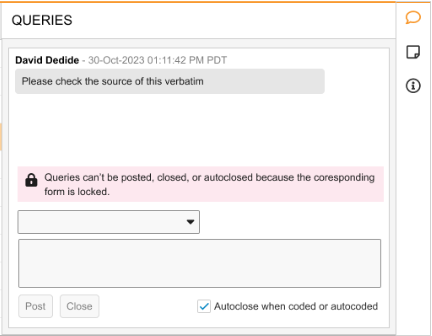
-
分组模式(Grouped Mode)错误横幅文本:“相应的表单已被锁定,无法接收质疑。(The corresponding forms are locked and cannot receive queries.)”
 在分组模式视图下,只要组中至少有一个表单被锁定,就会显示横幅。
在分组模式视图下,只要组中至少有一个表单被锁定,就会显示横幅。
当数据被锁定时,“搜索质疑模板”框(如果存在)和“提交质疑”文本输入字段将被禁用,从而阻止质疑操作。现有设计中,关于表单被锁定的信息直接显示在“提交质疑”文本输入字段中,而不是显示错误横幅,变更后不再显示该信息。
冻结数据
与锁定数据不同,当数据被冻结时,质疑输入字段保持启用状态。冻结影响数据源,但不妨碍输入质疑的功能。
启用和配置
此功能自动可用。
了解详细信息
改进了已删除代码的 JDrug 自动编码功能
用例
此增强功能对于依赖 JDrug 词典进行临床研究(尤其是在日本)的团队至关重要。它解决了“幽灵”代码的问题,即已从词典中正式删除但可能仍被自动化系统选中的条目。通过确保自动编码过程仅匹配处于活动状态的有效条目,该解决方案有助于保持与当前日本编码标准的合规性,并消除了识别已弃用代码的手动审查需求。
描述
在自动编码过程中,系统现在会自动过滤掉任何“维护标志(Maintenance Flag)”值为“C”的 JDrug 代码。“C”标志表示该代码在当前词典版本中已被删除,系统现在将这些条目视为不符合自动匹配条件。这确保了自动编码结果准确、最新,并与可通过词典面板手动选择的代码完全一致。
启用和配置
此功能自动可用。
改进了审计跟踪中对已编辑的编码器质疑消息的跟踪
用例
目前,当用户同时具有“编码器”和“审查”标签页的访问权限,并从“审查”标签页编辑与编码器相关质询关联的消息时,系统的审计跟踪无法在 Veeva Coder 中将此编辑准确反映为单独的事件,导致难以追踪质疑消息的更改历史。
此增强功能确保对编码器质疑消息的所有更改都通过清晰、独立的审计条目进行跟踪,从而提高审计完整性并满足法规合规性和审计需求。
描述
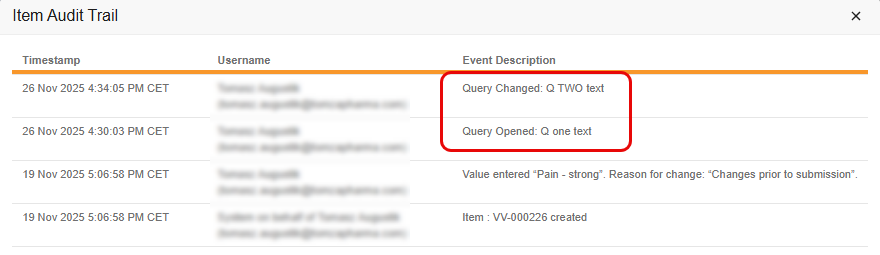
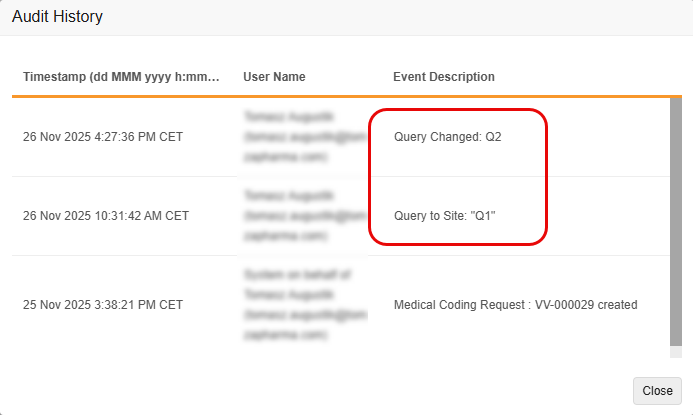
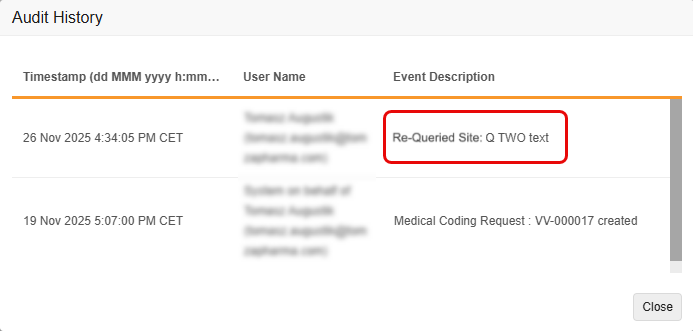
通过此功能,每当编辑与编码器相关的质疑消息时,编码器审计跟踪都会创建一个新的、独立的审计条目,而不是简单地用新消息更新原始审计条目。此更改确保原始质疑消息和所有后续编辑都能在审计跟踪中清晰记录和可见。它还提高了 EDC 中的条目审计跟踪与编码器中的审计历史之间的一致性。
启用和配置
此功能自动可用。
编码管理
以下是编码器工具的新功能(Veeva Coder 的管理区域)。
将编码系统标签更新为 Veeva Coder
用例
配合最近 Vault 应用程序品牌从 Vault [应用程序] 更新为 Veeva [应用程序] 的举措,编码系统的产品名称及所有系统引用现在都使用更新的名称 Veeva Coder。此更改确保所有 Veeva 应用程序中的产品命名保持一致。
描述
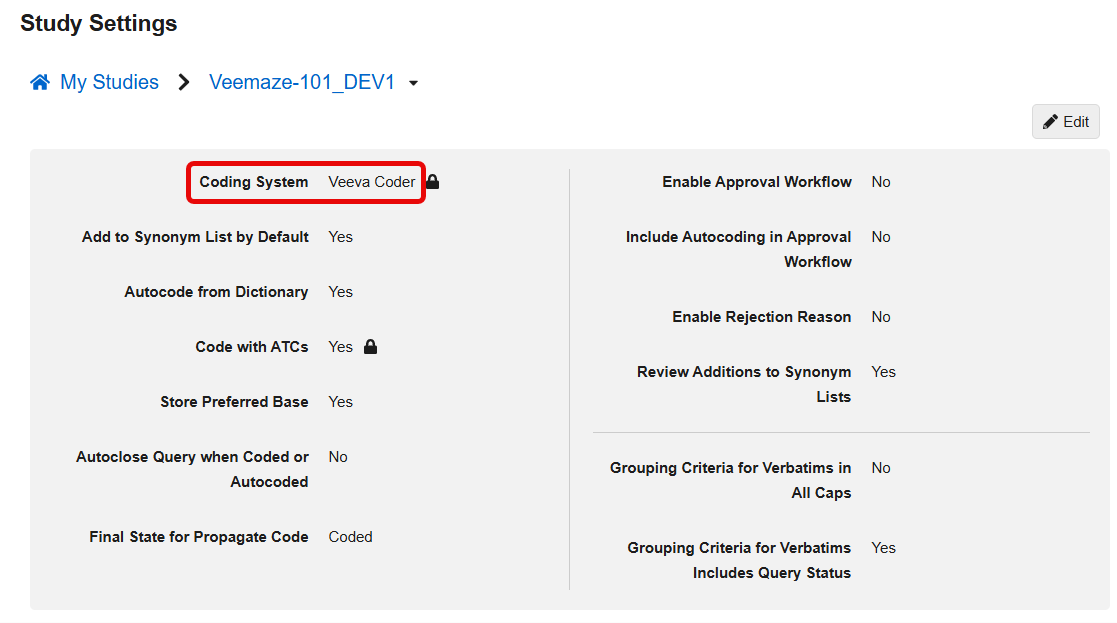
此功能更新了所有系统引用中显示的编码系统产品名称,包括编码器工具(编码器工具)> 研究设置(Study Settings)。在此版本中,编码系统的标签从 Vault Coder 更新为 Veeva Coder。
启用和配置
此功能自动可用。
成像
以下是 Veeva EDC 的成像检查模块“Veeva EDC 成像”的新功能。
成像:异步单个检查下载
用例
异步处理改善了下载成像检查的体验,通过允许用户继续其正常工作流来提高生产力。研究中心用户、CRA、数据管理员和成像专家不再需要在成像下载完成时保持登录状态。他们可以继续在应用程序的其他区域工作,或完全关闭浏览器。
描述
从数据录入、审查、评估中的检查查看器或“成像(Imaging)”标签页中的检查列表单击下载链接,将启动检查下载的异步处理。系统会显示一个简短的通知,告知你流程已开始。
如果你尝试下载已经开始下载的检查,系统将识别出活动请求并阻止重复下载。你可以同时下载多个不同的检查。
在下载处理期间,你可以恢复正常工作流,导航到应用程序内的其他区域或关闭浏览器窗口。
当检查准备好后,系统会发送一封包含文件直接下载链接的电子邮件。下载链接在清除前有效期为 7 天,之后用户只需重新启动下载即可。
启用和配置
此更新自动适用于使用 Veeva EDC 成像的早期采用者。
了解详细信息
成像:更新 DICOM 去标识化配置文件
用例
DICOM 图像通常包含大量元数据,包括敏感的患者健康和身份识别信息(PHI/PII)。此功能确保系统的 DICOM 去标识化流程和配置文件与最新的 DICOM 标准(具体为 2025c)保持同步。自动去标识化流程现在覆盖了新定义的标签,确保系统降低风险并保持合规性的能力。
描述
Veeva EDC 成像的安全配置文件已更新,包含截至 2025c 版本 DICOM 标准中定义的所有标签。这确保了标签浏览器正确显示所有可用标签。
现有的去标识化流程已更新,以包含新的 DICOM 标签。
- 对于每个 DICOM 文件,系统将识别标记为“DEID”(去标识化)的新标签。
- 这些新标签的原始值将被替换为去标识化的虚拟值。
此更新是系统数据管理的后台更改,不包括对现有用户体验(UX)或工作流的任何更改。
从 2024c 到 2025c 版本中已纳入去标识化配置文件的 DICOM 标签列表:
| 属性名称 | 标签 | 虚拟值 |
|---|---|---|
| 民族代码序列 | (0010,2161) | SQ |
| 民族 | (0010,2162) | UC |
| 性别认同代码序列 | (0010,0044) | SQ |
| 性别认同评论 | (0010,0045) | UT |
| 性别认同序列 | (0010,0041) | SQ |
| 组织学诊断代码序列 | (0008,1304) | SQ |
| 蒙太奇频道标签 | (0040,B03F) | LO |
| 蒙太奇名称 | (0040,B03B) | LT |
| 使用名称 | (0010,0012) | LT |
| 使用名称评论 | (0010,0013) | UT |
| 使用人名序列 | (0010,0011) | SQ |
| 主要诊断代码序列 | (0008,1302) | SQ |
| 主要诊断代码序列 | (0008,1301) | SQ |
| 代词代码序列 | (0010,0015) | SQ |
| 代词评论 | (0010,0016) | UT |
| 次要诊断代码序列 | (0008,1303) | SQ |
| 临床使用性别参数类别代码序列 | (0010,0046) | SQ |
| 临床使用性别参数类别评论 | (0010,0042) | UT |
| 临床使用性别参数类别参考 | (0010,0047) | UR |
| 临床使用性别参数类别序列 | (0010,0043) | SQ |
| 第三人称代词序列 | (0010,0014) | SQ |
启用和配置
此功能自动可用。
了解详细信息
评估
以下是 Veeva EDC 评估区域的新功能。
医疗评估网格更新
用例
以前,搜索医学评估记录需要完整输入方案编号,排序选项有限。此更新通过引入高级筛选和通配符搜索功能,提高了工作流管理效率。这对于管理多个研究的用户尤其有帮助。
描述
我们升级了医学评估网格,以改进整体界面和数据管理能力。
关键改进包括:
- 改进的筛选:搜索功能现在支持部分匹配和通配符搜索,用于筛选方案编号。
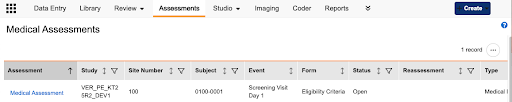
- 冻结列:为在滚动时保持上下文,“评估(Assessment)”列现在被冻结为第一列。
- 列大小调整:列现在具有自动宽度设置,以更好地适应显示的数据。用户在手动调整列大小时,也可以选择截断或换行显示单元格文本。
启用和配置
这些更改在版本发布时自动适用。
研究设计和配置
此区域中的功能适用于工作室,即 Veeva EDC 的研究设计和配置区域。
工作室病例手册版本更新
用例
创建和编辑病例手册版本时新增字段,帮助研究设计者为修订提供更好的参考。病例手册版本名称和外部 ID 现在可以在上线后更改的开发与测试期间进行更新。
描述
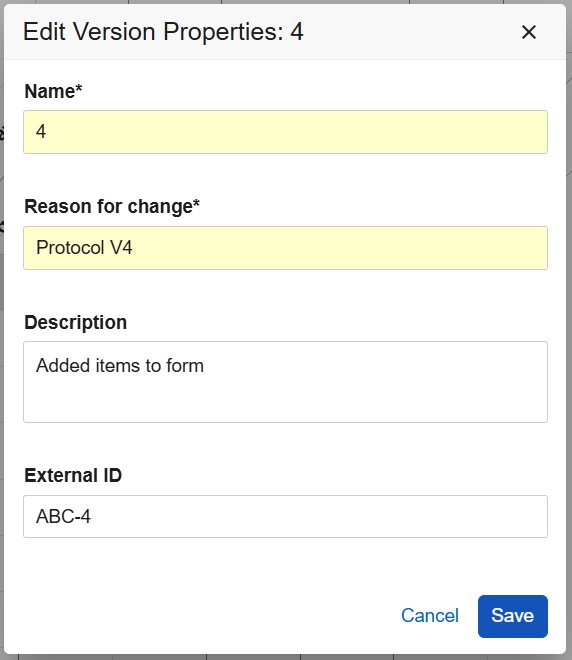
编辑或创建病例手册版本时,现在可以为每个新的病例手册版本设置唯一外部 ID。研究设计者可以为未发布的研究版本更新病例手册定义(版本)名称、更改原因、描述和外部 ID。
新的可选字段描述(Description)和外部 ID(External ID)在“创建新版本(Create New Version)”对话框中可用。更改原因(Reason for change)和外部 ID 字段现已包含在“编辑病例手册版本(Edit Casebook Version)”对话框中,允许设计者在更新研究设计时修改这些值。此外,为清晰起见,“编辑(Edit)”对话框的标题已更新为“编辑版本属性:[版本号](Edit Version Properties: [version number])”。
当超出字符限制时,字段长度会强制执行并显示屏幕错误消息:
- 名称(128)
- 更改原因(255)
- 描述(256)
- 外部 ID(128)
先前发布的版本和状态为正在验证(Validating)的版本的属性,可通过新的工作室菜单选项查看版本属性(View Version Properties)进行查看。选择此项将打开“查看病例手册版本”对话框,为只读模式。
启用和配置
此功能自动可用。
了解详细信息
工作室:跨 Vault 复制实验室和成像表单
用例
跨 Vault 复制实验室和成像表单进一步扩展了设计复用能力,并减少了在研究内从头构建表单所需的手动工作。
描述
从其他研究或跨 Vault 的库复制事件组、事件或表单时,实验室面板、实验室表单和成像表单及其相关的条目组、条目、代码列表和表单属性现在都作为复制的一部分包含在内。只有当源研究和目标研究都启用了实验室或成像设置时,实验室和成像表单才会在表单复制(Forms Copy)对话框中可供选择。
对于实验室表单,分析物、全局代码列表和单位必须存在于目标研究中,才能成功复制表单。
对于成像,模态的全局代码列表必须存在于目标研究中,才能成功复制表单。
启用和配置
此功能对于启用了全局实验室或成像的研究自动可用。
工作室:验证任何设计变更
用例
通过扩展工作室中的临时验证能力,研究设计者现在可以确认无版本的设计变更(如规则)处于已验证状态。以前,验证主要与病例手册绑定。此更新后,设计者即使仅进行了无版本更新,也能完成验证步骤。此更改确保设计者可以在所有设计元素从开发(DEV)环境部署到测试(TST)环境之前,验证其准确性。
描述
研究验证流程已从病例手册定义移至研究实例。工作室操作菜单中的验证(Validate)选项现在可用于任何研究设计变更,包括无版本组件,如规则、审查计划、表单链接、评估和安全配置。在开发(DEV)环境中,对设计进行任何更改后,研究状态将恢复为进行中(In Progress),并且验证选项将显示在 Studio 操作菜单中。
在验证作业运行期间,工作室将锁定编辑和保存功能,包括导入翻译,以防止数据冲突。
验证完成后,研究状态将更新为已验证(Validated),并且验证选项将被禁用。用户将被悬停消息引导至“作业(Jobs)”区域,在那里他们可以检索当前验证的输出。
启用和配置
此功能自动可用。
受试者 ID 生成设置包含在研究复制中
用例
此功能更新了工作室中现有的研究设置复制功能,使其包含受试者 ID 生成的设置。
描述
启动研究复制时,系统现在包含以下受试者 ID 生成详情:
- 格式:受试者 ID 使用的结构。
- 类型:选择的特定生成类型。
- 范围起始与结束:为受试者编号定义的特定数值边界。
启用和配置
此功能自动可用。
工作室复制日志:新增摘要标签页和日志消息
用例
在工作室中复制设计时,输出文件现在会汇总复制选择内容,并在日志中提供更多详细信息,以便设计者更好地了解复制操作的结果以及某些规则被标记为无效或跳过的原因。
描述
工作室复制作业的输出文件现在包含一个专门的“摘要(Summary)”标签页。新的“摘要”标签页显示时间戳、源 Vault、源研究和环境详情,以及为复制选择的选项。“状态消息(Status Message)”列中包含了更详细的消息。“日志(Log)”标签页中新增的“备注(Notes)”列对状态消息进行了扩展,在以下特定情况下提供了更多信息:
- 规则已复制 - 已更新以匹配名称上的目的地定义
- 规则已复制并标记为无效 - 缺少目的地研究引用
- 规则无法复制,因为在目的地中找不到一个或多个引用
- 规则已跳过,无法解析规则中的标识符
启用和配置
此功能自动可用。
工作室 PDF 中的表单名称和计划驱动的默认值附录选项
用例
在生成工作室 PDF 时,新选项提供了更清晰的输出,并允许设计者根据其组织需求进一步格式化 PDF。当使用特定的默认数据配置,以及两个不同的表单设计具有相同标签时(例如生命体征(Vital Signs,VS 和 VSS),此功能尤其有用。
描述
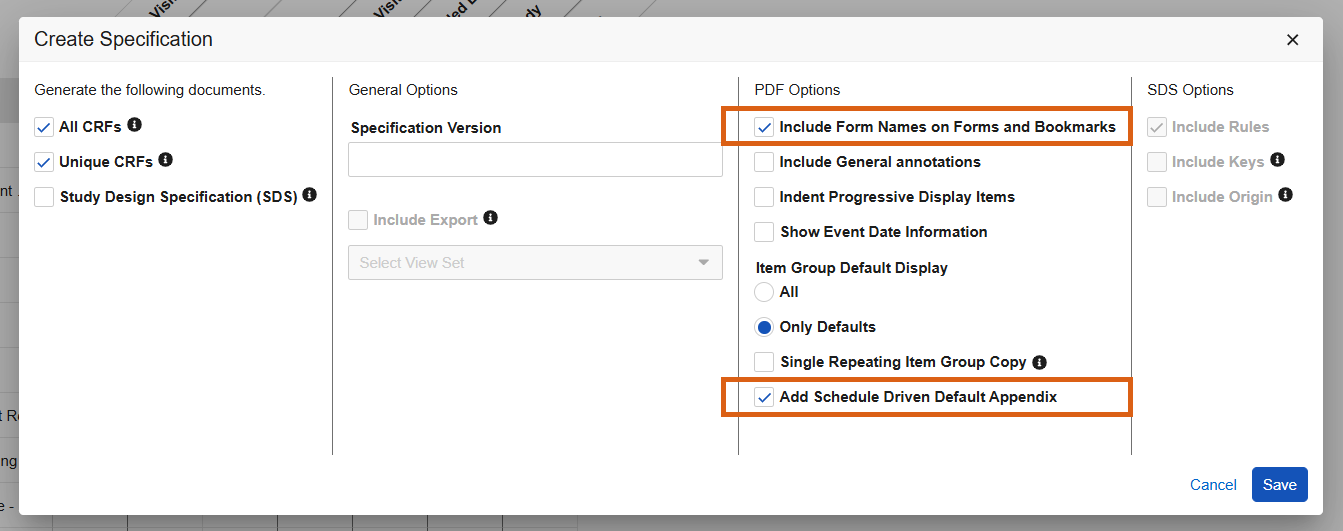
生成工作室规范 PDF 时,在“创建规范(Create Specification)”对话框中会看到新的复选框:
- 在表单和书签上包含表单名称(Include Form Names on Forms and Bookmarks)
- 添加计划驱动的默认值附录(Add Schedule Driven Default Appendix)
在 PDF 和书签中,表单名称将显示在表单标签旁边的括号中。
当选中“添加计划驱动的默认值附录”选项,并且在表单设计中使用了计划驱动的默认值时,附录将包含在 PDF 的末尾。
为节省设计者时间,当选择“包括常规注释(Include General Annotations)”时,“添加计划驱动的默认值附录”的选项将默认勾选。
当使用 API 自动生成 PDF 时,启动作业请求中包含两个新的请求参数:include_form_names_forms_bookmarks 和 schedule_driven_default_appendix。仅当你同时生成“所有 CRF”或“唯一 CRF”时,这些选项才能设置为“true”。
启用和配置
这些更改在工作室中自动可用。
了解详细信息
在电子邮件中显示条目的上次提交值
用例
研究设计者现在可以将条目的先前值配置为包含在发送电子邮件规则的消息中。在电子邮件正文中同时显示先前值和当前值,对于发送与不良事件(AE)和其他表单相关的电子邮件尤其有用。
描述
在工作室配置用户自定义规则时,.previous_submit_value__v 条目属性现在可作为令牌用于包含在电子邮件消息中。研究设计者将在发送电子邮件规则的“操作”部分看到这个额外的令牌,并可以使用此令牌在电子邮件正文中提供条目的先前数据值。
示例:${Custom.@Form.igAE.AESER.previous_submit_value__v}
启用和配置
此功能自动可用。
了解详细信息
增加工作室帮助内容
用例
工作室中属性面板的“帮助内容(Help Content)”字符限制已延长,支持更长描述,以便在数据录入期间更好地告知研究中心用户。
描述
工作室对象属性面板中“帮助内容”字段的字符限制已增加到 1500。此更改适用于事件组、事件、表单、条目组和条目的“帮助内容”字段。当超过 1500 个字符时,用户将收到警告,并需要在保存前缩短字符长度。
启用和配置
此功能自动启用。
为表达式引擎 v2 规则强制启用相互结构
用例
此功能为使用表达式引擎 v2 的研究中的规则强制执行一致的相互结构行为。它有助于确保混合使用 @Form 浮动标识符和完全限定标识符的规则遵循其预期行为,当另一个标识符被提交时按预期重新评估。
描述
对于使用规则表达式 V2 的研究,新规则和正在复制到研究中的规则将强制将“相互结构”值设置为“是(Yes)”,并且 Vault 所有者将无法在管理区域(业务管理(Business Admin),规则定义(Rule Definitions))中编辑此值。
在比较研究时,即使研究使用不同的表达式引擎版本,规则的相互结构设置差异也将包含在比较中。“相互结构”字段值从“否(No)”更改为“是”的规则也将包含在验证测试脚本文件中。
启用和配置
此功能对于使用表达式引擎 v2 的研究自动可用。
强制校验派生条目配置的有效性
用例
工作室中的新限制和验证有助于研究设计者正确配置与派生条目相关的系统编辑检查、渐进显示和默认数据,防止因工作室配置不当而导致的生产问题。
描述
系统编辑检查(条目属性)
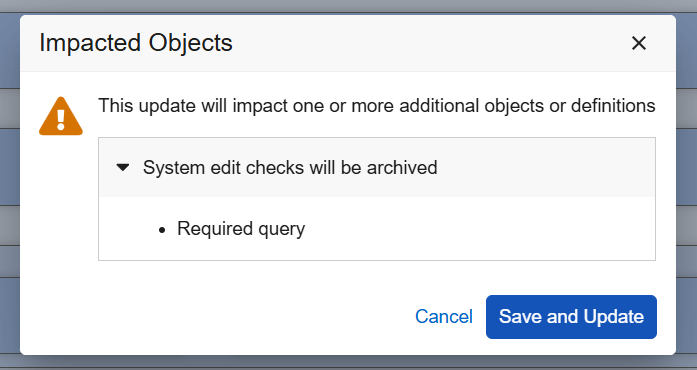
当条目的条目类型(Item Type)更改为派生(Derived)并保存时,EDC 现在会自动归档与该条目关联的任何活动系统编辑检查(例如,必填、未来日期和范围检查)。这确保了对于研究中心用户无法修改的条目,必填、未来日期和范围检查不会在数据录入中自动生成。对于先前在派生条目上添加的编辑检查,一个新的对话框将告知设计者哪些系统编辑检查设置将被归档。
渐进式显示
当可见性仅设置为包含在提取中(Include in Extracts)时,系统现在会阻止在渐进显示规则中使用派生条目。当修改派生条目且显示可见性(Display Visibility)属性仅指定为包含在提取中,并且包含渐进显示规则时,工作室将自动归档渐进显示规则,并显示一个新的受影响对象对话框。随后,渐进式显示部分将从条目或条目组的属性(Properties)面板中隐藏。
对于现有的无效配置(无论是在条目组还是条目上),拖放编辑器中会出现警告图标和通知。属性面板中会显示一个带有清除渐进显示(Clear Progressive Display)按钮的警告横幅,允许用户更正配置并归档规则。
如果研究包含具有派生条目的无效渐进显示配置,则在运行病例手册验证时也会包含警告。
默认数据
派生条目将不再作为可配置默认数据的可用列出现。配置为默认数据的条目不能更改为派生条目类型。
研究设计者现在可以使用条目列旁边的新橡皮擦图标 清除为默认数据配置的整个列。如果派生条目先前包含在默认数据中,则该列现在将显示警告图标和橙色高亮。网格顶部的红色横幅将通知用户,他们需要删除该列才能保存对默认数据配置的更改。
如果研究包含具有派生条目的无效默认数据配置,则在运行病例手册验证时也会包含警告。
启用和配置
此功能自动可用。
工作室规则:强制显式空白处理
用例
以前,规则编辑器中的“空白处理(Blank Handling)”字段默认为空,这常常导致对系统如何处理缺失数据产生混淆。具体对于数字字段,系统在规则执行期间将空值视为“0”。然而,研究设计者通常希望将其视为“null”。移除空白选项可确保规则行为更具可预测性,并提醒研究设计者在需要时主动更改设置。
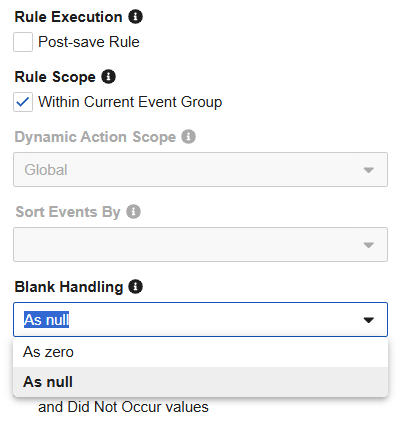
描述
规则编辑器已更新,确保每条新规则都明确设置了如何处理空白字段。所有新规则现在将默认设置为为空(As Null),而不是空选项。此外,空的“空白(blank)”选项已从选择中移除。配置规则时,你现在将看到两个清晰、不同的选择:为空或为零(As Zero)。
现有规则将保持不变,以确保其当前逻辑不受影响。如果现有规则当前具有空白值,则该空白选项将保留,除非研究设计者手动选择新选项。当编辑旧规则的空白处理时,系统将要求研究设计者必须选择两个显式选项之一才能保存。
启用和配置
此功能对于使用表达式引擎 v2 的研究自动可用。
了解详细信息
规则电子邮件应以研究语言和区域设置显示
用例
由发送电子邮件规则产生的电子邮件先前以触发电子邮件的数据录入研究中心用户的用户语言/区域设置显示。在此版本中,电子邮件中的数据将以研究语言和区域设置显示。此更改有助于在用户语言/区域设置与研究语言/区域设置不同的情况下,使数据和电子邮件内容保持一致。
描述
当强制使用研究语言时,包含在发送电子邮件规则中的以下数据点将以研究语言和区域设置显示:
- 日期 & 日期时间条目
- 代码列表条目
- 访视方法
- 事件日期
当未强制使用研究语言时,电子邮件中包含的数据点将以用户语言和区域设置显示。
电子邮件的主题和正文的其他方面将根据研究设计者配置的规则操作显示。
启用和配置
此功能自动可用。
工作室:核心数据定义验证
用例
研究构建通常需要遵守组织标准和元数据存储库。已从其组织标准创建核心数据定义 JSON 文件的客户,现在可以在工作室中根据该文件验证研究设计定义。研究设计者和库管员可以直接在工作室中上传和管理 JSON 格式的“核心数据定义”(CDD)文件,以根据源标准验证研究设计。这有助于研究团队减少通过基于风险的测试进行验证的工作量,同时确保研究合规性。
描述
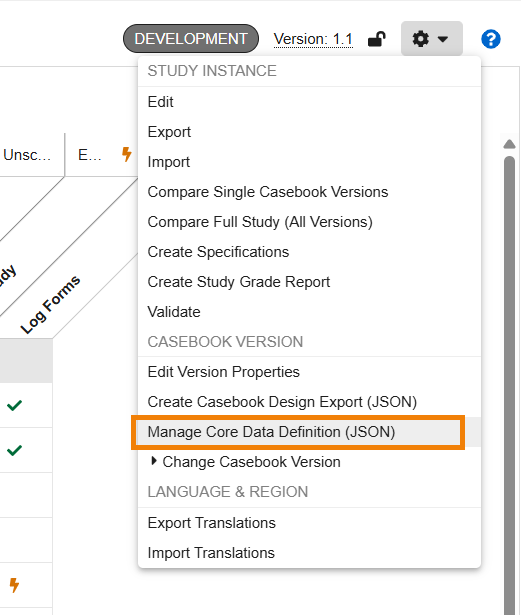
工作室操作菜单中新增了一个“管理核心数据定义(JSON)(Manage Core Data Definition (JSON))”操作,允许研究设计者上传、移除和重新添加 .json 格式的核心数据定义文件。“创建病例手册设计导出(JSON)(Create Casebook Design Export (JSON))”和新的“管理核心数据定义(JSON)(Manage Core Data Definition (JSON))”操作都归在菜单的“病例手册版本(Casebook Version)”区域下。
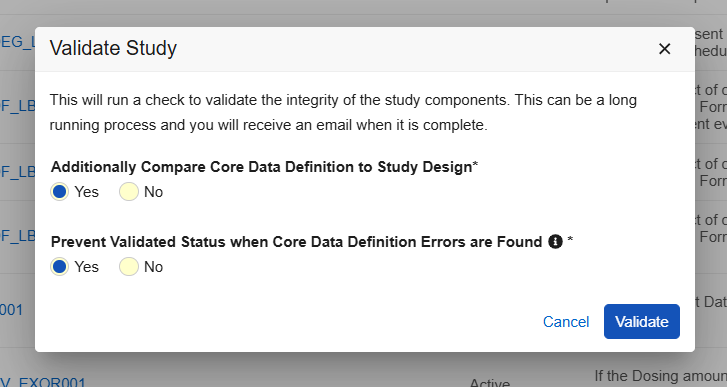
当选择“验证”并且存在核心数据定义文件时,在“验证研究(Validate Study)”对话框中会看到两个新的“是/否”选项:
选择“另外将核心数据定义与研究设计进行比较(Additionally Compare Core Data Definition to Study Design)”将根据核心数据定义文件验证研究设计,并提供一个单独的 .csv 文件,与工作室验证文件一起打包在一个 zip 文件中。系统将发送一封包含验证输出链接的电子邮件通知。
选择“找到核心数据定义错误时阻止已验证状态(Prevent Validated Status when Core Data Definition errors are Found)”将阻止研究获得已验证状态,并在发现错误时阻止成功部署。在“部署研究设计(Deploy Study Design)”对话框中有一个新选项“忽略任何核心数据定义发现(Ignore Any Core Data Definition Findings)”。选择此选项将忽略数据定义验证,并允许成功部署,即使核心数据定义发现了设计错误。
启用和配置
此功能在工作室中自动可用。
研究管理
本部分中的功能适用于系统工具(System Tools)或 EDC 工具(EDC Tools),即 Veeva EDC 的研究级管理区域。
用于即时 VeevaID 注册和增强用户管理的 Person__sys
用例
此功能通过利用即时 VeevaID 注册模型,引入了一种更高效的研究中心工作人员上线方式。以前,用户帐户会立即创建,这通常导致为可能永远不会登录的个人产生大量帐户。在 26R1 中,完整用户帐户的创建将延迟到 VeevaID 注册完成后才进行。这为申办方提供了显著更高的可见性,并允许管理员跟踪邀请状态。
描述
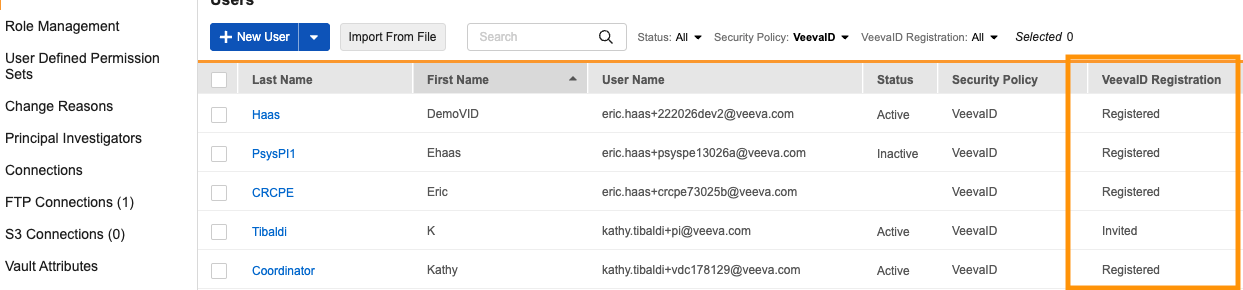
通过此更新,标准 person_sys 对象用于管理研究中心用户详细信息和研究访问权限,用户在正式注册前将处于待处理(Pending)状态。
用户网格中的新 VeevaID 注册(VeevaID Registration)列显示实时状态,包括已邀请(Invited)、已注册(Registered)、已过期(Expired)或已撤销(Revoked)。
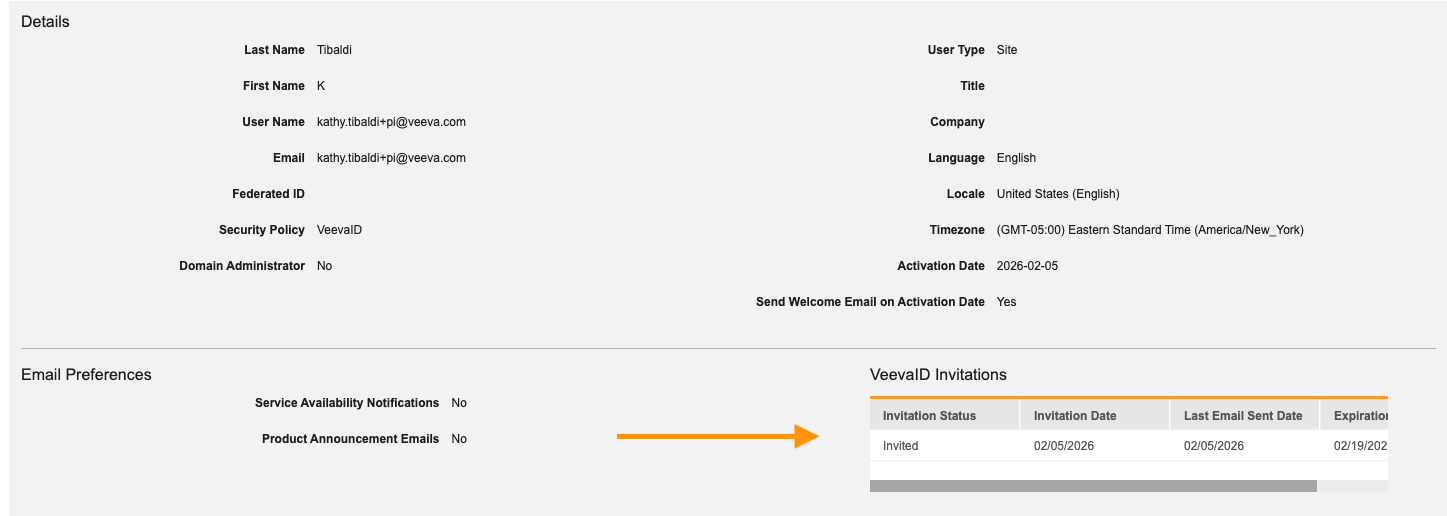
添加新研究中心用户时,系统现在支持激活日期(Activation Date),将邀请保留到指定日期再发送给用户。
VeevaID 注册电子邮件已更新,包含 Vault 名称和注册后登录的链接。对于使用 CDMS 培训的客户,此初始注册电子邮件将取代先前从培训 Vault 发送的电子邮件。研究中心用户完成 VeevaID 注册后,将收到第二封详细说明研究和角色访问权限的电子邮件。
用户 VeevaID 邀请历史记录现在显示在系统工具的“用户(User)”页面上。
现在,系统每 72 小时会向尚未完成 VeevaID 注册的研究中心用户发送一次电子邮件提醒。提醒将按此频率继续发送,直到注册完成、管理员撤销邀请,或初始发送日期后 14 天已过且邀请过期。在注册完成之前,可以随时触发新的邀请。
新的 VeevaID 注册报告可帮助管理员分析一个或多个研究的注册进度。
系统将为申办方(Sponsor)类型的用户创建 Person_sys 记录。但是,用户创建和管理流程不会改变。
我们还更新了检索用户 API。在此版本中,此端点现在的行为如下:
- 当
user__sys尚不存在时(即已被邀请但尚未注册 VeevaID 的待处理研究中心用户),返回person__sys - 当因不存在
user__sys而返回person__sys时,应用以下规则:user_id将为空字符串user_name将与user_email相同
- 不再返回 Vault 所有者记录
启用和配置
此功能将在客户 Vault 中分阶段启用。客户将在启用前收到通知。联系你的服务顾问讨论早期参与事宜。此功能与集中化的主要研究者管理功能相关联,将作为单个版本的一部分同时发布。
基于事件的审查计划
用例
以前,表单的审查要求会应用于整个研究计划中表单的每个实例。这种行为要求研究设计者创建同一表单的不同版本,以便为不同事件实施不同的审查要求。通过此功能,研究设计者可以根据表单所在的事件设置特定的审查要求,从而简化实施基于风险的审查计划的过程。
描述
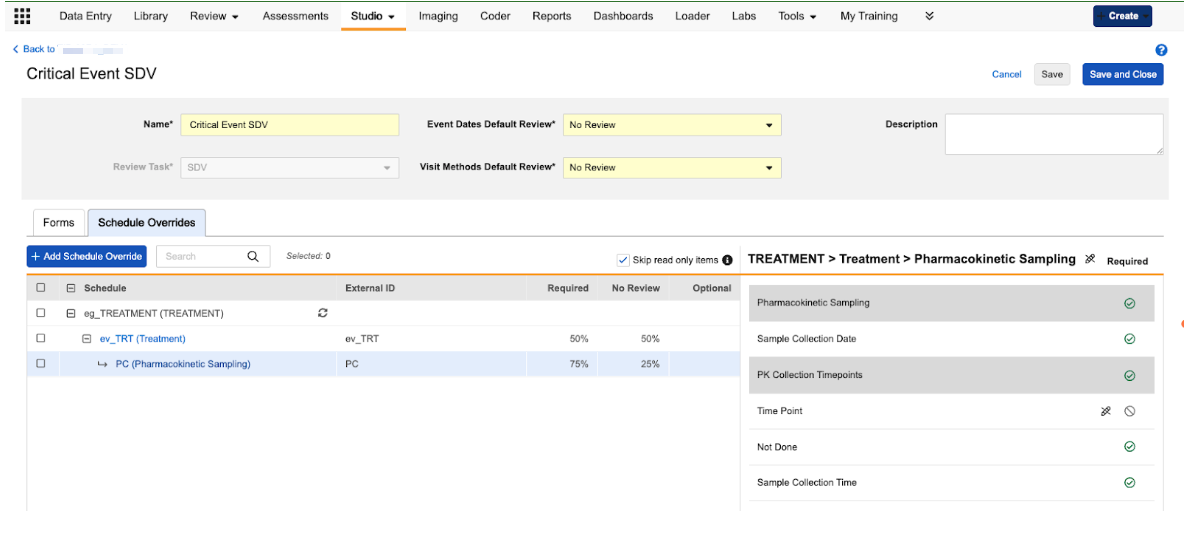
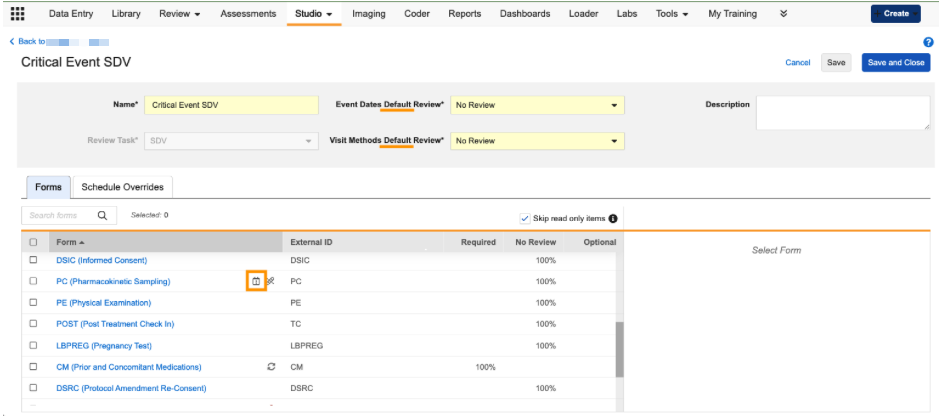
我们在工作室的“审查计划(Review Plan)”配置区域引入了一个新的计划覆盖(Schedule Overrides)标签页。此标签页允许用户为特定访视(事件)或这些访视中的特定表单定义独特的审查规则。
当用户导航到计划覆盖标签页时,他们可以从研究计划中选择特定事件和表单来创建覆盖。添加覆盖后,用户可以执行以下操作:
- 设置事件级别要求:为单个事件的事件日期(Event Date)和访视方式(Visit Method)配置特定的审查要求。
- 设置表单级别要求:为表单上的条目定义独特的审查要求,这些要求仅在特定访视期间完成该表单时适用。
- 批量管理覆盖:使用设置为(Set As)工具一次更新多个覆盖,或使用复制配置(Copy Configuration)选项将特定配置从一事件/表单实例应用到计划中的其他实例。
其他更新
- 事件日期和访视方法审查字段的审查计划标题现在标记为默认值。
- 研究设计规范(SDS)作业已更新,包含以下计划覆盖详情:
- 事件日期审查(Event Date Review)和条目必填(Item Required)列已更新为事件日期默认审查(Event Dates Default Review)和条目审查要求(Item Review Requirement)
- 我们为访视方式默认审查(Visit Methods Default Review)、事件组标签(Event Group Label)、事件组名称(Event Group Name)、事件标签(Event Label)、事件名称(Event Name)、事件日期审查要求(Event Date Review Requirement)、访视方式审查要求(Visit Method Review Requirement)、表单标签(Form Label)和条目组标签(Item Group Label)添加了新列。
- 表单名称(Form Name)列现在出现在访问方式必填(Visit Method Required)列之后。
- 差异报告已更新以考虑计划覆盖。
启用和配置
此功能自动可用。
测试数据验证作业
用例
当对未发布的研究版本进行更新时,可能会移除与测试数据仍然关联的设计定义,这会在尝试生成研究数据提取或 PDF 时导致错误。通过新的“测试数据验证(Test Data Verification)”作业,你可以精确定位研究设计不再支持的特定数据,从而识别哪些受试者受到这些“破坏性变更”的影响。可以重置、移除单个数据或受试者,或将其移至单独的研究中心进行移除,从而保留其余有效的测试数据,并在测试过程中节省时间。
描述
拥有管理作业(Manage Jobs)权限的用户现在可以从 EDC 工具 > 作业历史(Job History)运行新的测试数据验证作业,以识别由于研究设计变更而导致无效的数据。新任务会审查研究中是否有无效数据,特别寻找缺失的定义,例如被移除的事件、表单或条目组,以及会导致系统错误的数据类型变更。
作业完成后,用户会收到一封带有作业输出下载链接的电子邮件。生成的 CSV 文件提供了详细信息和病例手册位置,以便轻松定位无效数据。输出文件将问题分为两大类:
- 定义已移除:当研究设计者在未发布版本中移除了一个已在该环境中关联了测试数据的定义(如表单或事件)时发生。
- 定义已更改:当现有条目的数据类型、长度或精度发生了修改,导致系统无法再处理先前输入的值时出现。例如,将字段从数字更改成日期。
启用和配置
此功能在开发(DEV)和测试(TST)环境中自动可用。
了解详细信息
集中化的主要研究者管理
用例
主要研究者(PI)的管理现在更加灵活,允许申办方独立于其系统用户帐户来跟踪研究者详情。此更新允许收集更多 PI 信息(作为研究中心的主要联系人),并为申办方提供了一个专门用于管理 PI 记录的工具,而不仅仅是创建记录。
描述
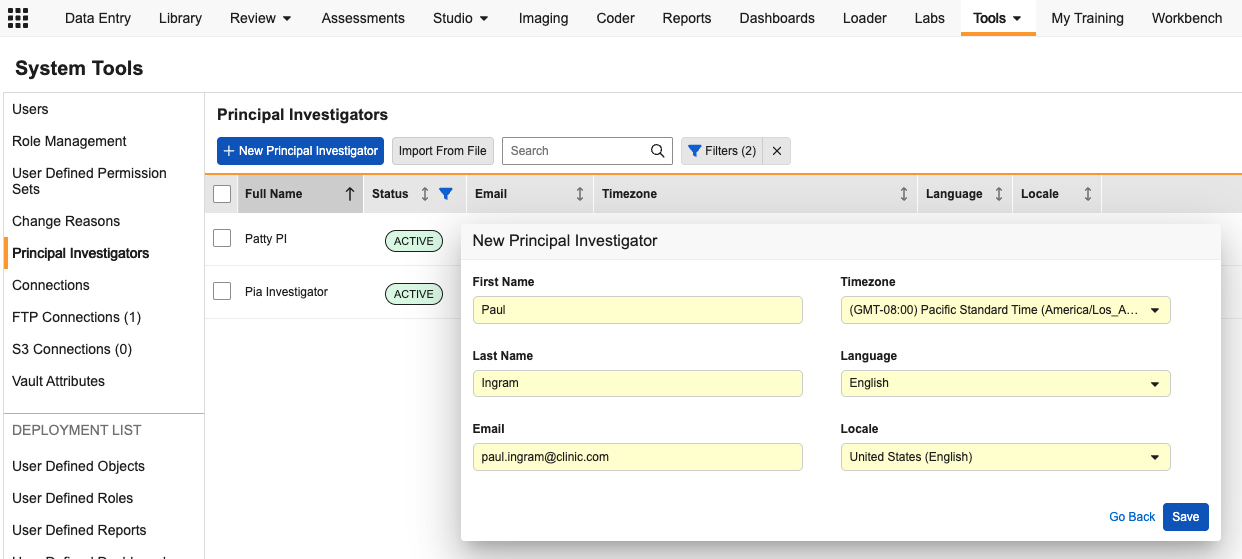
此功能使用标准 Person__sys 对象来支持 PI 管理,提供了一种更强大的方式来捕获研究者数据。通过系统工具中新增的主要研究者(Principal Investigators)标签页,管理员可以在单个网格中查看和搜索所有 PI。
在“主要研究者”标签页中,可以:
- 查看所有活动研究者记录的全面概览,包括全名(Full Name)、状态(Status)、电子邮件地址(Email Address)、时区(Time Zone)、语言(Language)和区域设置(Locale)。
- 编辑联系方式、激活/停用记录或将重复的研究者合并为单个活动记录。
- 选择单独或通过批量导入创建新 PI 记录。也可以通过 EDC 工具中的研究中心创建继续创建 PI 记录,该屏幕添加了用于额外记录详情的字段。
- 获得仅限于用户管理员和具有以下权限的自定义角色的访问权限:“系统工具”标签页、查看用户、编辑用户和所有研究中心的研究级访问权限。
此标签页中的 PI 信息用于在数据录入和审查标签页中显示,并包含在研究文件格式(SFF)提取、研究数据提取(SDE)、CDB 和安全病例中。
在你的 vault 中启用后,现有的 PI 记录将出现在新标签页中。如果之前未收集电子邮件地址,系统将为用户电子邮件地址显示“dev.null@veeva.com”。语言和区域设置将填充相应的 Vault 设置。这些值可以通过“主要研究者”标签页单独更新,或通过导入批量更新。
对自定义报告的影响
启用后,当前在研究中心(Study Site)(site_v)对象上使用主要研究者字段的自定义报告应更新为引用主要联系人(Primary Contact)字段,因为主要研究者字段将被弃用。
启用和配置
此功能将在客户 Vault 中分阶段启用。客户将在启用前收到通知。联系你的服务顾问讨论早期参与事宜。此功能与用于即时 VeevaID 注册和增强用户管理的 Person__sys 功能相关联,将作为单个版本的一部分同时发布。
了解详细信息
FTP 交付更新
用例
此功能提供了一个新选项,使 Veeva 在交付 CDB 导出时,可区分发往 Vault 的出站连接与外部 FTP 连接。
描述
系统工具和 EDC 工具中更新的 FTP UI 为 Veeva Vault 的 CDB 交付方法包含了一个新的子类型,该子类型支持将导出内容交付到 Vault。客户在创建新连接或修改现有的 CDB FTP 连接时,如果希望将导出内容交付到 Vault 文件暂存区,应选择此类型。
启用和配置
此功能自动可用。
数据更改报告的日期范围扩展
用例
申办方通常需要长时间审查临床数据变更,以确保研究的完整性。在此版本之前,数据更改报告仅限于 90 天的窗口,这迫使用户运行多个单独的报告来覆盖一整年的活动。此更新通过允许用户提取涵盖长达一年的单一报告,消除了这种手动工作,为监控研究中的长期数据趋势和审计跟踪提供了更高效的方式。
描述
此功能将数据更改报告的最大日期范围从 90 天延长至一年(考虑到闰年,为 366 天)。运行提取时,用户现在可以选择自定义日期范围,或使用“处于过去(In the last)”筛选器,持续时间最长为 366 天。
为确保生成的文件保持可用,此功能包含了对 Excel 输出的保护措施。如果用户选择的条件可能超过 1,048,576 行的限制,系统将显示错误消息。在这种情况下,用户将被提示选择更小的日期范围或将文件格式切换为没有行限制的 CSV。
预发布说明:审计跟踪数据不包含在 Vault 的预发布副本中。因此,DCE 仅显示在预发布 Vault 创建或刷新之后发生的数据变更。
启用和配置
此功能自动可用。
受试者进度列表:完成与清洁状态的逻辑更新
用例
以前,如果受试者没有分配特定的审查计划或没有准备好审查的数据,系统会将某些进度列默认为“否”。即使受试者没有待处理的工作,此操作也会在整体“清洁(Clean)”列中产生误导性的“否”值。通过此功能,Veeva 改进了受试者进度列表中的逻辑,以确保“清洁”状态报告更准确地反映数据审查的实际状态。
描述
我们改进了用于计算受试者进度的逻辑,以确保用户的列表和提取更加精确。当未分配审查计划或不需要数据时,相关字段将保持空白,而不是默认为否。
“清洁”列的逻辑已更新,以识别这些空白值。如果输入完成(Entry Complete)、已锁定(Locked)、已签署(Signed)和所有质疑已关闭(All Queries Closed)列均为是,且受试者 SDV 完成(Subject SDV Complete)和受试者 DMR 完成(Subject DMR Complete)为是或空白,则受试者现在被视为清洁。
启用和配置
此功能自动可用。
用户管理支持未映射的培训要求
用例
此功能引入了一个关键的保护措施,防止管理员无意中向分配给缺乏映射培训要求的角色的用户授予研究访问权限,帮助客户避免与法规审计或手动培训状态更新相关的风险。
描述
此更新引入了培训合规性的三项重大改进:为未映射的研究设置默认培训状态的功能、当培训未映射到角色时增强的警告,以及一个简化跨 Vault 重新计算培训状态的新工具。
未映射研究的默认培训状态
管理员现在可以定义当用户被分配到未定义培训要求的研究时,系统将自动应用的特定培训状态。这确保不会仅仅因为缺少映射而默认授予访问权限。
在系统工具中,管理员可以导航到 Vault 培训连接的操作(…)菜单,选择编辑学习系统(Edit Learning System),并根据需要查看或更新。默认设置为已培训(Trained),以匹配当前功能。
增强的用户管理警告
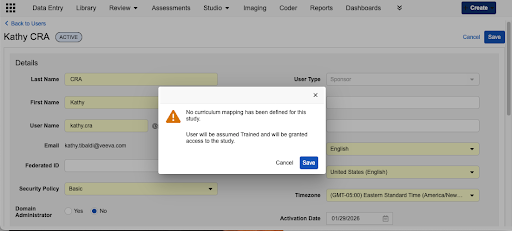
为用户分配角色时,系统现在会执行实时验证以检查培训要求。如果未找到要求,将显示一个突出的警告对话框,要求管理员在继续之前确认风险。
可能的警告包括:
- 研究无映射:如果研究未定义课程,系统会警告管理员并应用新的默认状态。
- 已映射研究中的未映射角色:如果研究有培训要求,但正在分配的特定角色没有,则会显示警告,说明未为该角色分配课程,用户将被假定为已培训并获得研究访问权限。
- 所有研究访问权限:当授予用户对 Vault 内所有研究(All Studies)的访问权限时,如果没有任何研究为该角色映射培训,将显示警告,并且用户将被分配默认培训状态。
如果在研究或角色的用户导入过程中缺少映射,也会显示这些警告。
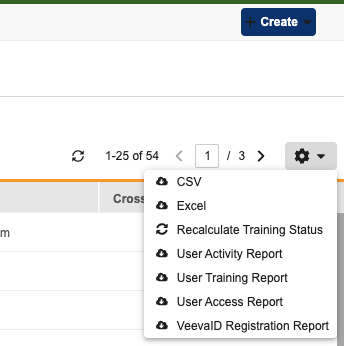
重新计算培训状态工具
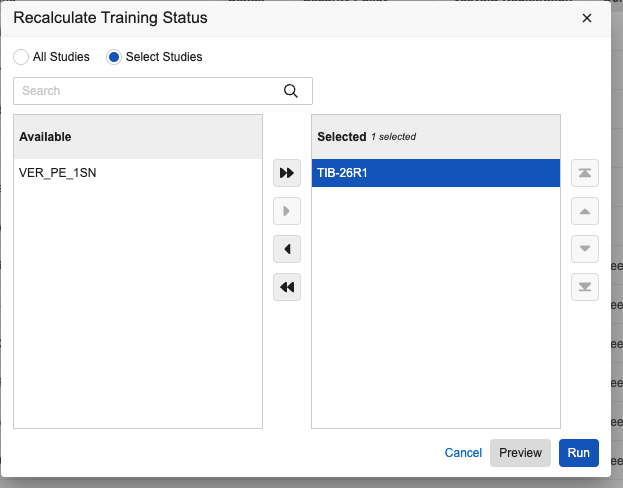
系统工具中提供了新的重新计算培训状态(Recalculate Training Status)操作。此操作允许授权用户在选定的研究中刷新选定(或所有活动)用户的培训数据。这在培训要求更改或默认设置更新时非常有用。新操作包括一个预览模式,可生成 CSV 报告,帮助你在运行实际作业之前查看哪些用户可能因当前培训完成情况而失去访问权限。
此功能无法在预发布版本中测试,因为不支持 Vault 培训连接。
启用和配置
此功能在发布后自动在所有 Vault 中启用,并将应用于所有在 EDC 工具中将启用学习系统(Enable Learning System)设置为是的研究。默认培训状态将设置为已培训,以匹配当前功能。
了解详细信息
支持更高容量的规则作业
用例
以前,单个规则作业最多运行 100 条规则,超过 100 条,研究管理员需要拆分成多个作业。现在,单个作业中可以包含更多规则。更高容量的规则作业减少了研究管理员运行的单独作业数量,提高了效率。
描述
在此版本中,可以在单个“运行规则(Run Rules)”作业中选择运行最多 300 条规则。
启用和配置
此功能自动可用。
了解详细信息
事件与表单进度列表:更新列顺序
用例
为提高一致性和可读性,我们更新了事件和表单进度列表的布局。这些更改确保相关的序列信息被组合在一起,更加便于数据管理员和监查员追踪其各自组内事件和表单的时间顺序。
描述
此更新适用于:
- CSV 提取:为事件和表单进度列表生成的 CSV 文件。
- 报告模板:用于这些列表的标准报告模板。
为了与下游现有数据保持兼容,这些列顺序更改将不应用于版本化提取。(事件进度版本化提取和表单进度版本化提取)。
启用和配置
此功能自动可用。
研究部署:移动“包含系统数据(Include System Data)”选项
用例
以前,在部署期间,包含系统数据的选项突出显示在主研究部署对话框中,导致这些设置在常规研究更新时很容易被用户意外选中。此更新增加了一层保护,以确保仅在特定意图下才部署系统数据。
描述
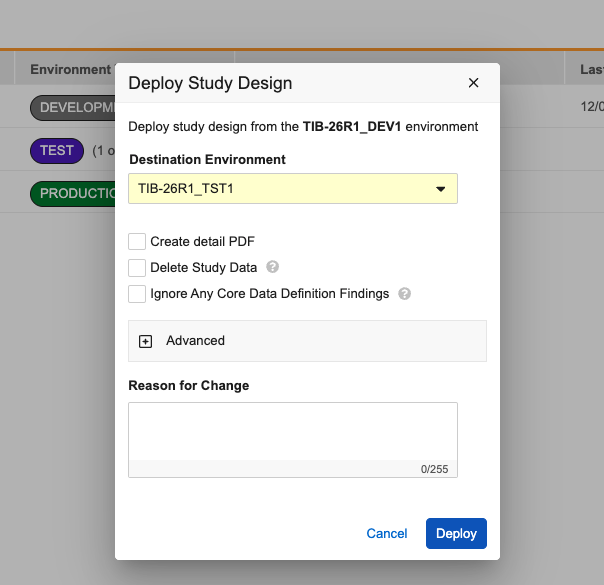
为改进部署过程并最大限度地减少意外的 Vault 部署,“研究部署(Study Deployment)”对话框现在默认隐藏系统级设置。对话框底部添加了一个新的“高级(Advanced)”部分。当对话框打开时,此部分保持折叠状态,将焦点集中在标准部署任务上,例如创建详细 PDF 或删除研究数据。
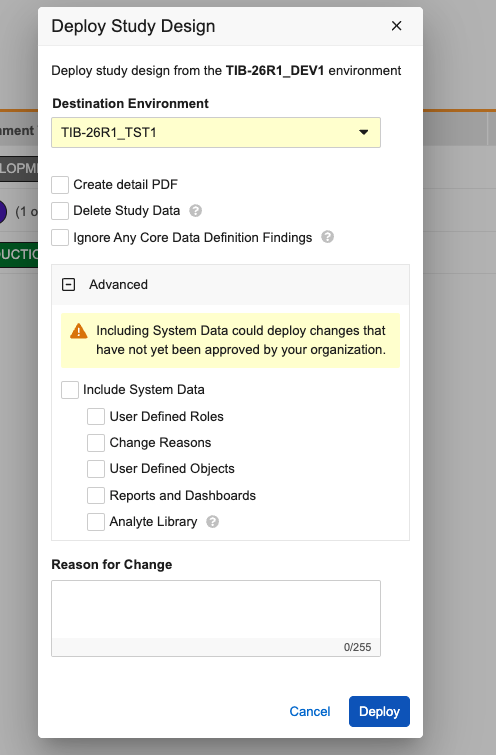
要在部署中包含 Vault 级更改,请单击展开“高级”部分。在其中,你将看到一条警告消息,提醒你包含这些数据可能会部署尚未经组织批准的更改。在此部分中,你可以选择包含:
- 用户定义的角色和对象
- 更改原因
- 报告和信息板
- 分析物库
启用和配置
此功能自动可用。
了解详细信息
重新设计规则作业输出文件
用例
规则作业(EDC 工具)的输出文件已重新设计,以提供关于规则执行结果的更全面详情并提高可用性。此更改有助于研究设计者和首席数据管理员在运行规则时更全面地了解预期行为。
描述
此功能为“运行规则”作业结果输出引入了一个新的单个 Excel 文件,取代了当前压缩的 CSV 文件集。
新的 Excel 文件包含五个不同的标签页:
- 摘要(Summary)标签页:提供作业的高级概览,包括作业 ID、Vault 和研究名称、选定的规则数量以及包含的受试者数量。
- 受试者(Subjects)标签页:列出作业中包含的每个受试者,并提供每个受试者产生的总变更的总体计数,例如创建和移除的表单、打开和关闭的质疑、更改的受试者状态以及更新的派生值。
- 规则摘要(Rule Summary)标签页:列出作业中包含的每条规则,并提供受该规则影响的受试者总数的总体计数,以及该规则采取的每项特定操作的总数(例如创建和移除的表单、更改的派生值以及更改的受试者状态数量)。
- 规则详情(Rule Details)标签页:列出作业中发生的每次规则执行以及在病例手册中产生的操作。每次执行包括操作发生的具体病例手册位置。必要时,“操作详情(Action Details)”列现在会提供有关特定结果的附加信息,包括由于目标被锁定、冻结或不存在而未发生预期操作的情况。操作标签已更新以提高准确性和清晰度。
- “错误”标签页:列出作业期间遇到的任何错误的详细信息,包括规则名称和规则失败的受试者。为提高可读性和简化错误管理,技术故障详情和大量代码引用已被移除,并替换为特定的错误 ID。
在预览模式下运行的“运行规则”作业的结果现在包含与实时作业结果相同级别的详细信息。
当强制使用研究语言时,“运行规则”作业文件的内容现在以研究语言显示。
启用和配置
此功能自动可用。
了解详细信息
启用变更:部署 UI 与处理改进
描述
在 25R3 版本中,“部署 UI 和处理流程优化”功能以分阶段发布形式启用,需要 Veeva 支持。此功能现已扩大适用范围,以使所有客户受益。
此功能现已更新为对所有 Vault 自动启用,以在整体部署处理过程中将部署后端处理拆分成一系列小包进行。详见 25R3 发行说明。
启用和配置
版本发布时,此功能将自动可用。
工作历史记录包含 SDS 和工作室验证
用例
“研究设计规范(Study Design Specifications)”和“工作室验证(Studio Validation)”作业结果现在集中存放,并与其他研究作业一起进行更正式的追踪。这有助于为设计文档和验证提供集中位置,以防设计者删除或放错电子邮件通知。
描述
验证和研究设计规范(SDS)作业现已纳入 EDC 研究作业框架。作业输出文件和日志会自动存储,并在“作业历史”(EDC 工具)中与其特定的作业 ID 关联。在“作业历史”中,将鼠标悬停在信息图标上会显示生成文件时选择的选项。
运行验证验证作业以包含核心数据定义时,输出 ZIP 文件包含工作室验证和核心数据定义验证。
发起作业的用户仍会收到相同的确认电子邮件,其中包含直接下载输出文件的链接。
启用和配置
此更改在发布时自动适用。
从 EDC 中移除遗留的 CDB 工作台导出作业
描述
此版本从 EDC 工具中移除了遗留的 CDB 导出作业选项(以及其任何剩余的计划实例)。24R2 版本引入了从 EDC 到 CDB 的增量数据摄取,从而不再需要此导出作业。
启用和配置
此更新在发布时自动应用。
随机化
本部分中的功能是适用于 Veeva EDC 的随机化模块的新功能。
为新研究禁用 EDC 随机化
用例
此更改确保客户为所有即将进行的试验使用当前的 Veeva 随机化产品或第三方供应商。
描述
在此版本中,创建新研究时,传统的 EDC 随机化设置将不再可用。虽然使用 EDC 随机化的现有研究将继续正常运行,不受影响,但以下更改将影响新创建的研究:
- 工作室设置:对于新研究,“启用 Veeva 随机化(Enable Veeva Randomization)”选项将不再出现在工作室研究设置中。
- 新研究创建:“导入随机化配置(Import Randomization Configuration)”选项已从新研究界面中移除。此外,如果用户复制了已启用 EDC 随机化的现有研究,新副本将自动禁用该设置。
- 报告和规则:对于新研究,随机化引用将不再出现在研究设计规范(SDS)、差异报告、库或规则中。
启用和配置
此更改立即适用于新研究。当前使用 EDC 随机化的现有研究不受影响。
实验室
本部分中的功能是适用于 Veeva EDC 的实验室模块的新功能。
正常范围中支持年龄下限/上限值的修饰符
用例
临床研究团队通常需要按精确年龄组来定义实验室正常值范围。以前,年龄范围边界在系统中通常被解释为包含边界。通过此功能,团队可以使用数学运算符明确界定年龄边界是包含性的还是排除性的。此功能对于维护源数据准确性至关重要,例如区分“12 岁以下”(<12)与“12 岁及以下”(≤12)的受试者范围。
描述
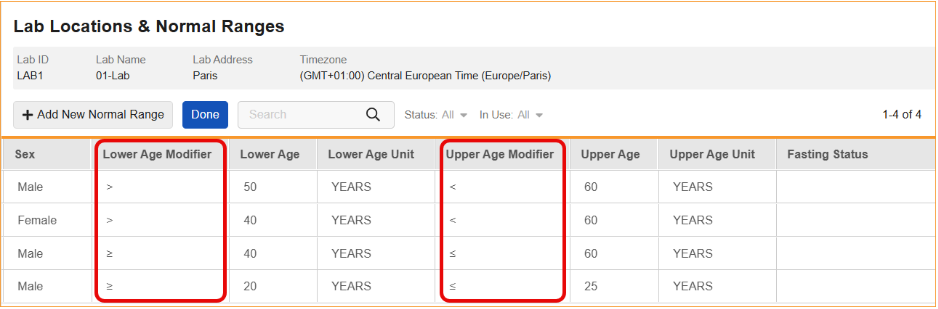
此更新在实验室参考范围记录中引入了年龄下限修饰符(Lower Age Modifier)和年龄上限修饰符(Upper Age Modifier)字段。通过这些字段,可以选择特定的运算符来限定年龄值:
- 年龄下限修饰符:大于或等于(≥)或大于(>)。
- 年龄上限修饰符:小于或等于(≤)或小于(<)。
这些修饰符现在显示在“实验室位置和正常范围”网格中,新列位于相应年龄值之前。
为了确保数据完整性,系统现在会强制执行额外的验证规则。当定义了年龄值时,必须选择修饰符;反之,当选择了修饰符时,必须输入相应的年龄值。如果任一条件未满足,将显示错误消息。
此外,系统通过评估数值年龄和修饰符来识别重叠范围。例如,定义为 ≥12 岁的范围与定义为 <12 岁的范围被识别为非重叠。如果发生逻辑冲突,例如将下限年龄设置为 >12 且上限年龄设置为 <12 —,系统将阻止用户保存记录。
此外,标准模板:实验室参考范围(Standard Template: Lab Reference Ranges)报告已修改以支持这些更新,现在可以显示年龄下限修饰符和年龄上限修饰符列。
为支持这些更改,以下列已添加到 SDE 的 SYS_LABRANGES 数据集中:
- LABLOWERAGEMODIFIER
- LABUPPERAGEMODIFIER
启用和配置
此功能自动可用。
了解详细信息
移除正常值范围上下限值自动添加的尾零
用例
目前,当用户输入正常值范围下限或上限时,系统会在保存记录前根据分析物的精度设置自动添加尾零。此行为可能导致问题,因为保存的数据与用户输入的内容不完全匹配。更重要的是,如果稍后更新了分析物的精度,运行“更新过期的正常范围(Update Outdated Normals)”作业可能会添加更多尾零,从而可能破坏下游流程,如 SDV、DMR 和签名。
描述
此功能改变了正常值范围下限和上限在系统中的存储方式,以确保保存的数据与用户输入的数据匹配,而不添加尾零。
在此版本中,自动添加尾零的功能已被移除,因此正常值范围下限和上限将完全按照用户输入的方式保存。此功能确保了数据完整性,并防止了因分析物精度更改而导致的下游验证中断。
此功能还阻止用户保存非数字或单位数据类型的分析物,并针对这些情况更新了错误消息。
启用和配置
此功能在 GR 中自动启用。请联系 Veeva 支持团队进行 LR 启用操作。
角色管理与安全
本节中的功能是对系统工具 > 角色管理(Role Management)和系统工具 > 用户(Users)区域的增强,以及对 Veeva Clinical Data 中的标准研究角色(Study Roles)、安全性和访问控制的更改。
新增质疑团队
用例
三个新的专业质询团队提供了更精细化的质询分配和管理控制。
描述
在此版本中,Veeva EDC 引入了三个新的质疑团队:医疗监查、医疗审查和药物警戒。当管理员创建或重命名自定义角色时,这些新团队现可作为“团队(Team)”下拉菜单中的可选选项。此外,也可以在位于工作室“研究设置”的“用于系统质疑的质疑团队(Query Team for System Queries)”下拉菜单中选择这些团队。没有为这些新团队添加任何标准角色。
启用和配置
此功能自动可用。
了解详细信息
将“管理安全配置”权限移至“研究设计”部分
用例
为使管理安全配置(Manage Safety Configuration)权限与工作室中执行的配置工作更匹配,我们在角色“管理(Role Management)”标签页中移动了此权限的位置。
描述
在系统工具 > 角色管理中,管理安全配置权限已从研究管理(Study Administration)部分移至研究设计(Study Design)部分。此更改仅涉及该权限在角色管理 UI 中的显示位置,对实际权限本身以及任何标准或自定义角色均无影响。
启用和配置
此更新在发布时自动应用。
连接与集成
本节中的功能是与 Veeva Clinical Data 的新连接或集成,或对现有连接或集成的增强。
临床运营-EDC 连接:仅适用于 CTMS 中连接研究的方案偏离管理
用例
此功能改进了 Veeva EDC 和 Veeva CTMS 之间的一致性。由于临床运营-EDC 连接是单向的,在 EDC 中对方案偏离(PD)所做的更改可能会无意中覆盖 CTMS 中管理的数据。通过限制连接研究中 EDC 内的编辑功能,此增强功能将 CTMS 确立为方案偏离的主要管理工具。
描述
对于连接到 Veeva CTMS 的研究,此更新改变了用户在 EDC 中与方案偏离的交互方式。一旦在 EDC 中创建了 PD,在 EDC 内编辑偏离字段的功能将被禁用。
当查看 CTMS 管理的方案偏离时,适用以下规则:
- 编辑(Edit)按钮被禁用。将鼠标悬停在按钮上会显示提示,说明该记录在 CTMS 中管理。
- 用户可以查看方案偏离及其审计跟踪的完整详情。
用户可以使用操作菜单中的新选项停用方案偏离(Inactivate Protocol Deviation)在 EDC 中手动停用方案偏离。如果偏离已在 CTMS 中标记为停用,此选项非常有用。
选择停用方案偏离会触发一个确认对话框,用户必须提供更改原因(Reason for Change)。如果该偏离在 CTMS 中尚未停用,连接将根据在 EDC 中进行的更改更新状态。
启用和配置
此功能对于连接到 Veeva CTMS 的 EDC 研究自动可用。
了解详细信息
临床运营-EDC 连接:部分 SDV 和 DMR 在 CTMS 中显示为进行中
用例
对于通过临床运营-EDC 连接进行连接的研究,SDV 和 DMR 状态会从 Veeva EDC 传输到 Veeva CTMS。为了更准确地反映和说明当前的 SDV 和 DMR 受试者访视(Subject Visit)状态,如果 SDV 或 DMR 已部分执行,系统将在未开始(Not Started)和已完成(Completed)之外指示进行中状态。此附加信息可在 CTMS 中新配置的字段中使用。不受限数据和受限数据的处理方式保持不变。
描述
- 未开始:访视中没有任何需要 SDV 或 DMR 的数据点(包括事件日期、访视方式和所有条目已完成 SDV 或 DMR
- 进行中:访视中至少有一(1)个数据点,但并非所有需要 SDV 或 DMR 的数据点(包括事件日期、访视方式和所有条目)已完成 SDV 或 DMR
- 已完成:访视中所有需要 SDV 或 DMR 的数据点(包括事件日期、访视方式和所有条目均已完成 SDV 或 DMR
每当事件或表单被重置,或 SDV 或 DMR 计划发生更改时,SDV 或 DMR 状态会自动更新。附加性和可选性的 SDV 或 DMR 不包含在状态计算中。
启用和配置
对于使用临床操作-EDC 连接的研究,此功能会自动启用。测试此功能需要与 Veeva CTMS 集成的环境,无法仅在 EDC 内进行测试。新状态将回填到所有连接的事件上,并在发布周末自动传输到 CTMS。因此,在 CTMS 中配置的新状态可能不会在发布后立即显示。
临床运营-EDC 连接:EDC 研究国家/地区名称保留用于连接研究
用例
EDC 研究国家/地区(Study Country)名称可能与 CTMS 研究国家/地区名称不同。以前,当通过临床运营-EDC 连接将研究国家/地区从 Veeva CTMS 传输到 Veeva EDC 时,EDC 研究国家/地区名称会被 CTMS 研究国家/地区名称覆盖(例如,“British Indian Ocean Territory”与“British Indian Ocean Territory (the)”)。覆盖可能导致规则编程或其他集成出现问题。
描述
如果通过临床运营-EDC 连接创建了新的研究国家/地区,CTMS 和 EDC 之间根据国家/地区代码进行国家/地区映射。在 EDC 中,新的研究国家/地区名称将与 EDC 国家/地区名称匹配。
如果通过连接更新了研究国家/地区,EDC 中当前的研究国家/地区名称将保持不变。如果当前名称是 CTMS 研究国家/地区名称,则保持不变。如果当前名称是 EDC 研究国家/地区名称,也保持不变。
在极少数情况下,如果通过连接更新研究国家/地区以指向不同的国家/地区(基于国家代码/地区映射),EDC 中的研究国家/地区名称将与新映射的 EDC 国家/地区名称匹配。
CTMS 中的研究国家/地区名称现在可能与 EDC 中的不同。在 EDC 中,26R1 之前创建的研究国家/地区名称和之后创建的研究国家/地区名称也可能不同。
启用和配置
对于使用临床操作-EDC 连接的研究,此功能会自动启用。测试此功能需要与 Veeva CTMS 集成的环境,无法仅在 EDC 内进行测试。
临床运营-EDC 连接:按研究国家/地区和研究机构汇总相同问题的用户异常消息
用例
如果由于研究或研究国家/地区级别的数据同步问题导致需要临床运营-EDC 连接的用户异常消息(UEM),每个受影响的研究国家/地区或研究中心可能会生成多条具有相同错误消息的 UEM。例如,如果一个研究被锁定,但临床运营-EDC 连接尚未断开,任何需要在 Veeva CTMS 和 Veeva EDC 之间同步的更改都将导致为每个研究国家/地区和每个研究中心生成一条用户 UEM,因为锁定会阻止其数据同步。为了减少 UEM 的数量,现在只创建一条列出所有受影响研究国家/地区(或研究中心)的消息。
描述
如果相同的临床运营-EDC 连接问题影响了多个研究国家/地区或多个研究中心,则只为研究国家/地区创建一条 UEM(列出所有受影响的研究国家/地区),并为研究中心创建一条 UEM(列出所有受影响的研究中心),两者都显示影响所列所有研究国家/地区或研究中心的错误消息。
研究国家/地区和研究中心分别列在 UEM 的“条目数据(Item Data)”部分。这适用于错误消息为“研究已锁定(Study is locked)”和“无法找到匹配的研究国家/地区记录(Matching Study Country record cannot be found)”的情况。
启用和配置
对于使用临床操作-EDC 连接的研究,此功能会自动启用。此功能无法仅在 EDC 中单独测试,需要与 Veeva CTMS 进行集成测试。
了解详细信息
安全-EDC 连接:每个 EDC Vault 均可使用连接配置
用例
配置安全-EDC 连接以将一个或多个 Veeva EDC Vault 连接到 Veeva Safety Vault 不再需要联系 Veeva 支持。
描述
现在,Vault 所有者和安全管理员可以完成安全-EDC 连接的配置,无需 Veeva 支持介入。
启用和配置
此更改将自动应用。
安全性-EDC 连接:基于条目值的新研究药物管理与识别
用例
临床试验通常需要复杂的研究药物给药方案,包括由研究者选择的受试者或访视特定药物应用、特定国家/地区的研究药物给药或各种子研究要求。以前,“研究药物名称”的定义仅限于为研究药物的每个安全配置进行静态配置。因此,为每个研究药物构建一个研究药物 EDC 表单的需求导致难以支持更复杂的研究设计。
对于安全-EDC 连接研究,我们现在引入了一种动态方法,允许研究中心在数据录入期间在 EDC 表单上选择所施用的研究药物。这显著简化了涉及多种研究药物的复杂研究的 EDC 表单构建过程,同时确保无论施用哪种药物,数据都能正确流向安全系统。
为此,在工作室的“安全集成”配置区域引入了一个新的“研究药物(Study Drug)”对话框,并且“研究药物名称(Study Drug Name)”安全字段到 EDC 条目值的映射可实现更灵活的配置。此新功能有助于对安全-EDC 连接研究的研究药物记录进行更可靠和灵活的管理。
描述
新研究药物配置
对于使用安全-EDC 连接的研究,在“工作室 > 安全集成”下新增了一个研究药物标签页。
从这里,研究设计者可以创建新的研究药物记录,包括名称(在研究内唯一)、设盲(Blinding)指示以及分类为“未给药”时排除(Excluded When Classified Not Administered)配置。
对于管理研究药物记录,适用与配置“工作室 > 安全集成 > 安全设置”相同的权限。
安全数据类型:研究药物
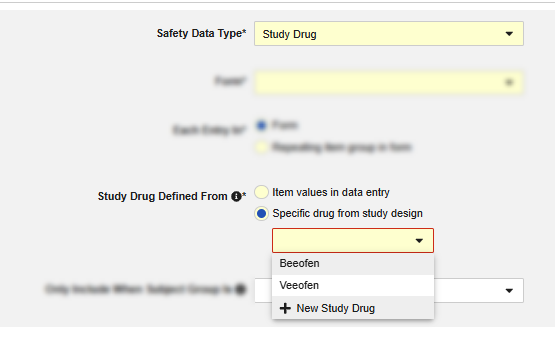
配置“研究药物”安全数据类型时,研究药物定义自(Study Drug Defined From)选项仍然允许研究设计中的特定药物,这取代了静态的研究药物名称。但是,研究药物名称的自由文本字段现在替换为已配置“研究药物”记录的选择菜单。也可以直接从下拉菜单创建新的研究药物记录以供立即选择。
或者,现在可以配置数据录入中的条目值(Item values in data entry),以允许在数据录入期间识别所施用的研究药物。
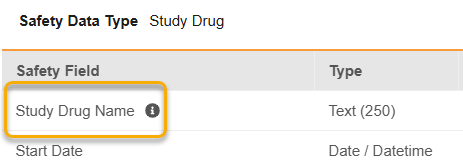
如果选择了数据录入中的条目值,则在“条目配置”步骤中将出现一个新的研究药物名称选项供映射。如果映射的条目是代码列表类型,工作室验证要求代码列表中的所有代码对应于研究中研究药物记录的名称。
安全数据类型:安全病例启动事件
在“安全病例启动事件”安全数据类型的“条目配置”步骤中,这些安全字段适用以下规则:
| 安全字段 | JSON 名称 | E2B 类似位置 |
|---|---|---|
| 对研究产品采取的行动 | AE_PRODUCT_ACTION_TAKEN | G.k.8 |
| 研究药物恢复时反应/事件是否再次出现(Did Reaction / Event Recur when Study Drug Resumed) | AE_PRODUCT_ACTION_RECUR | G.k.9.i.4 |
| 去激发应答(Dechallenge Answer) | AE_PRODUCT_ACTION_DECHALLENGE | 不适用(自 26R1 起安全-EDC 连接的新标准字段) |
| 研究药物的评估方法(Method of Assessment to Study Drug) | AE_PRODUCT_ASSESS_METHOD | G.k.9.i.2.r.2 |
| 研究药物的评估结果(Result of Assessment to Study Drug) | AE_PRODUCT_ASSESS_RESULT | G.k.9.i.2.r.3 |
| 研究药物的评估来源(Source of Assessment to Study Drug) | AE_PRODUCT_ASSESS_SOURCE | G.k.9.i.2.r.1 |
- “研究药物”列下拉菜单现在还将显示 EDC 表单名称,后跟按“研究药物”安全数据类型配置的“研究药物”(以前仅显示研究药物名称)。
-
对于“研究药物定义自”选项设置为“数据录入中的条目值”的每个“研究药物”安全数据类型,“研究药物”列下拉菜单将显示配置的 EDC 表单名称和“在数据录入中设置(set in data entry)”。这表示研究药物将由研究中心在数据录入期间选择。
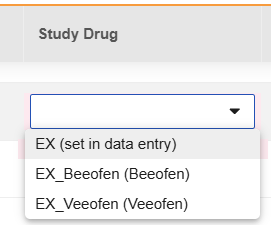
-
如果在“研究药物”列中选择了动态研究药物(“在数据录入中设置”),则新列“研究药物条目(Study Drug Item)”将要求从与相应安全字段的“配置条目(Configured Item)”相同的条目组中选择“研究药物名称”条目。仅允许文本或代码列表类型的条目。

- 现在可以映射到重复或非重复条目组,独立于“每个条目属于(Each Entry In)”的选择。
所有更改都反映在 SDS 中,包括“研究药物名称”列中的在数据录入中设置、新列研究药物条目以及已配置研究药物记录的新标签页。
复制 EDC 表单将支持新功能。由于研究药物的研究特异性,研究药物记录无法在研究之间复制。
功能发布期间现有研究中的情况
在功能发布期间,将为每个“研究药物”安全数据类型上的每个现有研究药物创建一个新的研究药物记录。研究药物记录将使用以下值创建:
- 名称:在各个“研究药物”安全数据类型 >“表单属性(Form Properties)”上配置的自由文本“研究药物名称”
- 已设盲:在各个“研究药物”安全数据类型 > 表单属性上配置的值
- 分类为“未给药”时排除:在各个“研究药物”安全数据类型 > 纳入标准上配置的值。
此后,新的研究药物记录将与相应的“研究药物”安全数据类型关联。此转换对当前安全病例创建或随访传输功能没有影响。
虽然新创建的研究药物记录的研究药物名称在研究内必须唯一,但在本次发布相关转换期间可能会创建重复项。
启用和配置
对于使用 Veeva 安全-EDC 连接的研究,此功能会自动启用。
现有安全-EDC 连接研究的注意事项:在功能发布期间,将为每个“研究药物”安全数据类型上的每个现有研究药物创建一个新的研究药物记录。此后,新的研究药物记录将与相应的“研究药物”安全数据类型关联。此转换对当前的 EDC 行为、安全病例创建或随访传输功能没有影响。更多详情请参阅功能描述。
安全集成:随访扫描作业独立于调度用户
用例
安全随访扫描作业是安全数据传输的重要组成部分。现在其执行不再依赖调度用户。
描述
随访扫描作业现在独立于调度用户及其权限。在 26R1 之前,调度用户必须具有对研究的适当权限才能执行作业。现在,计划的随访扫描作业一旦创建,将独立于调度用户的研究访问权限和权限而执行。
虽然 Vault 仍会记录作业计划历史记录,但将不再从特定研究的“EDC 工具 > 作业计划(Job Schedule)”UI 中提供。这是为未来的功能做准备。
启用和配置
对于使用 Safety-EDC 连接或 E2BLink 链接的研究,此功能会自动启用。
安全-EDC 连接:新增标准安全字段并调整配置限制
用例
通过安全-EDC 连接,不仅可以传输符合 E2B 标准的数据,还可以传输其他与安全相关的 EDC 数据。我们根据 Veeva Safety 标准数据模型,进一步扩展了可从 EDC 传输到 Veeva Safety 的标准安全字段范围。
描述
以下部分按安全数据类型描述了更改。
此版本重新排序了“安全病例启动事件”、“合并用药”和“研究药物”表单类型上的几个安全字段,以将最常用的字段放在顶部。显示顺序的更改仅与更好的研究构建体验有关,对任何 EDC 功能均无影响。
安全病例启动事件
“安全病例启动事件”表单类型现提供以下新字段,以支持(意外)妊娠病例的传输。
Veeva 建议一般的妊娠问题(剖腹产类型、胎儿/婴儿状态)与研究构建中现有的妊娠信息条目相邻。
Veeva 还建议所有与儿童相关的问题都放在一个重复条目组中,以应对多胞胎情况。
- 剖腹产类型
- 胎儿/婴儿状态(Fetal Infant Status)
- 儿童姓名或缩写(Child Name or Initials)
- 儿童名字
- 儿童姓氏
- 儿童出生日期(Child Date of Birth)
- 儿童年龄
- 儿童年龄单位(Child Age Unit)
- 儿童性别(Child Sex)
- 儿童体重(公斤)(Child Weight (kg))
- 儿童身高(厘米)(Child Height (cm))
- 儿童 GP 病历编号(Child GP Medical Record Number)
- 儿童医院记录编号(Child Hospital Record Number)
- 儿童出生胎龄数值(Child Gestation At Birth Number)
- 儿童出生胎龄单位(Child Gestation At Birth Unit)
- 儿童胎儿结局(Child Fetal Outcome)
- 儿童胎儿/婴儿状态(Child Fetal Infant Status)
- 儿童出生结局(Child Birth Outcome)
- 儿童头围(Child Head Circumference)
- 儿童阿氏评分(1 分钟)(Child APGAR Score (1 minute))
- 儿童阿氏评分(5 分钟)(Child APGAR Score (5 minute))
- 儿童阿氏评分(10 分钟)(Child APGAR Score (10 minute))
“安全病例启动事件”现提供以下新字段,以支持研究药物和合并用药信息的传输:
- 去激发应答
- 合并用药采取的行动(Concomitant Medication Action Taken)
- 合并用药复发应答(Concomitant Medication Recurrence Answer)
- 合并用药去激发应答
- 合并用药评估方法
- 合并用药评估结果
- 合并用药评估来源
其中,“儿童年龄单位”、“儿童出生胎龄单位”、“合并用药评估方法”、“合并用药评估来源”允许静态值。
必须为每个研究药物回答“去激发应答”,并且所有合并用药相关字段必须通过条目到表单链接配对。
“安全病例启动事件”安全数据类型上的以下安全字段现在仅在“每个条目属于”设置为“表单”时可用:
妊娠病例(Pregnancy Case)、妊娠事件(Pregnancy Occurrences)、分娩次数(Number Given Birth)、研究药物暴露时怀孕(Pregnant at Study Drug Exposure)、末次月经日期(妊娠病例)(Last Menstrual Date (Pregnancy Case))、怀孕日期(Pregnancy Conception Date)、预产期(Pregnancy Due Date)、怀孕结局日期(Date of Pregnancy Outcome)、怀孕结局(Pregnancy Outcome)、分娩方式(Delivery Method)
以下字段现在允许静态值:
妊娠病例、研究药物暴露时怀孕、医疗专业人员已确认(Healthcare Professional Confirmed)、父级途径(编码)(Parent Route (Code))、批次/批号(Batch / Lot Number)、频率值(Frequency Value)、途径(编码)(Route (Code))、配药研究中心(Site of Dispense)、报告的适应症(Indication Reported)、报告的适应症(编码 LLT)(Indication Reported (Coding LLT))
合并用药
“合并用药”表单类型现提供以下字段:
- 报告的适应症(Indication Reported)
- 报告的适应症(编码 LLT)
研究药物
“研究药物”表单类型现提供以下字段:
- 报告的适应症(Indication Reported)
- 报告的适应症(编码 LLT)
如果死亡
“如果死亡”表单现提供以下新字段。
这些字段将实现对研究中心更友好的研究设计,如果类型已预先配置并单独显示在表单上,研究中心用户可以输入原因而无需选择类型。
- 死亡原因 - 分类为已报告(Cause of Death - Classified as Reported)
- 死亡原因 - 分类为已报告(编码 LLT)(Cause of Death - Classified as Reported (Coding LLT))
- 死亡原因 - 分类为尸检(Cause of Death - Classified as Autopsy)
- 死亡原因 - 分类为尸检(编码 LLT)(Cause of Death - Classified as Autopsy (Coding LLT))
启用和配置
对于使用安全-EDC 连接的研究,此功能会自动启用。对于现有的连接和研究,管理员必须重新运行“系统工具 > 连接 > 安全”下的扫描 Vault Safety(Scan Vault Safety)作业,以显示新引入安全字段的任何翻译值的可用 Veeva Safety 选项。
安全集成:报告者详细信息新增来源、电子邮件和电话
用例
报告者信息现在将来源于 person__sys 对象。此更改是 EDC 范围内用 person__sys 对象替换 person__v 对象作为数据源的一部分,以便更好地与所有其他 Vault 应用程序集成。
这一新的源对象还允许安全-EDC 连接现在传输安全病例报告者的电子邮件和电话号码。
描述
对于安全-EDC 连接和 E2BLink 病例创建,在“工作室 > 安全集成 > 安全设置”中配置的报告者信息现在均来源于 person__sys 对象。这不会对当前数据或功能造成任何影响。
对于安全-EDC 连接,从 person__sys 对象获取报告者信息使其现在还可以传输报告者的电子邮件和电话号码。在“工作室 > 安全集成 > 的安全设置”中,如果为将报告者信息纳入安全病例而选择了报告者的完整研究中心信息(Full Site Information),在为报告者用户配置了电子邮件和电话号码的情况下,现在这些信息也将被传输。
启用和配置
对于使用安全-EDC 连接或 E2BLink 的研究,从 person__sys 对象获取报告者信息的功能自动启用。
在已配置的情况下,对于使用安全-EDC 连接的研究中的新安全病例,报告者电子邮件和电话号码的传输自动启用。现有安全病例不会接收任何随访消息,也不会在随访消息中对报告者信息进行更改,因为该信息在首次发送后是不可变的。
EDC API
EDC API 的新功能如下。请参阅我们的开发者门户的发行说明,了解更详细的功能信息。
EDC API 功能
该版本为 EDC 开发者提供了以下功能:
- 用于检索用户和上传用户的新用户信息数据源
- 检索研究设计定义端点
- 病例手册设计导出(CDE)更新
- 修改研究设计定义端点
- 核心数据定义(CDD)文件管理端点
- 使用数据定义验证和研究设计规范导出启动作业
EDC 临床报告
以下是 Veeva EDC Clinical Reporting(临床报告)应用程序的新功能。
针对临床报告研究的 SFF 增强功能
用例
SFF 的改进为下游系统增加了该格式的价值。
描述
此版本包含以下 SFF 改进:
- SFF 提取现在包含一个源(Source)列,显示数据的来源名称
- 质疑文件新增了来源(Origin)信息和快速质疑(Quick Queries)的列
- SYS_Links CSV 文件现在包含条目到表单的链接信息
- 完整的 SFF 包现在在本地 Vault 时间中午可用
启用和配置
这些功能在发布时自动更新。
了解详细信息
在临床报告中支持 JDrug 编码词典
用例
对于使用 JDrug 编码词典的 Veeva Coder 研究,临床报告中提供的 JDrug 支持在导出中包含合并用药等药物表单的日文编码术语。
描述
JDrug 编码词典值现可在 SFF 和原始导出中使用。原始导出的更新包括为所有配置了 MedDRA、WHODrug 和 JDrug 词典的表单添加了“DictionaryType”和“UserCodedBy”列。JDrug 词典值将适用于在 Veeva EDC 中配置了 JDrug 编码词典的表单。
启用和配置
此功能自动可用。
临床报告中列表数据网格的改进
用例
列表屏幕尺寸利用率的改进提升了用户的使用体验,使数据审查更加便捷——无论用户是使用较小屏幕,还是希望通过将单元格详情面板移动到新窗口的同时仍能查看列表行来更好地聚焦数据视图。
描述
此版本改进了列表屏幕,以更有效地利用可用空间。打开单元格详情面板将自动最大化网格。你可以将详情面板弹出到新窗口,以便完全查看列表数据。用户还可以使用新对话框显示和隐藏列,因此你不再需要一次选择一个列来隐藏或显示单个列。
其他增强功能包括:
- “展开网格(Expand Grid)”按钮已更新为“最大化(Maximize)”或“最小化(Minimize)”网格,为数据网格利用更多屏幕空间。
- 选择质疑或方案偏离的单元格装饰将打开单元格详情面板中的相应部分。
- 上下文筛选:新的网格级选项支持用户通过特定单元格值即时筛选结果。只需悬停在任何单元格上即可显示筛选快捷方式。
启用和配置
这些更改在发布时自动应用。
临床报告实验室标签的增量导入更新
用例
在实验室模块中更改标签时使用增量导入,确保小更改不需要完全重新处理研究数据。
描述
对实验室代码列表或单位条目的标签更改现在将添加到来自 EDC 的增量导入中。这仅适用于使用全局版本实验室的研究。
启用和配置
版本发布时,此功能将自动可用。
将作业 ID 添加到清单和导出日志
用例
为工作台和临床报告导出作业提供唯一标识符有助于提高故障排除效率和可追溯性。
描述
此版本将作业 ID 添加到工作台和临床报告导出作业的导出 manifest.json 文件和导出作业日志中。
启用和配置
版本发布时,此功能将自动可用。
了解详细信息
临床报告用户会话管理
用例
统一用户会话,消除用户在临床报告中活跃工作时被登出的困惑。
描述
临床报告用户会话现在将保持 Vault 会话活跃,并与 Vault 设置保持一致,确保 EDC 和临床报告中的访问权限一致,并符合 Vault 的设置。
启用和配置
版本发布时,此功能将自动可用。
临床数据库(CDB)
Veeva CDB 应用程序的新功能如下。
可用性:临床数据库(CDB)仅对 CDB 许可证持有者提供。请联系 Veeva 服务代表了解详细信息。
审查列表条目值变更检测
用例
数据管理员现在无需进行全面重新审查即可快速评估数据变更的影响,显著加快了审查周期。
一旦设置了审查状态,CDB 会自动识别并突出显示值发生变更的确切单元格。用户可以通过悬停在突出显示的单元格上,即时查看先前的数据值。
通过精确了解变更内容,数据管理员可以快速决定是忽略变更、创建有针对性的质疑,还是更新审查状态。
描述
当列表中的数据在设置了审查状态后发生变更时,CDB 现在提供对这些修改的精细可见性。系统不再仅仅标记整行,而是具体突出显示已更新的确切单元格。
- 视觉突出显示:变更的单元格会自动突出显示以便立即识别。
- 历史背景:悬停在任何突出显示的单元格上,即可即时查看先前值。
- 简化处理:在行级别关闭“数据变更”指示器将同时清除所有单元格的突出显示。
- 简化状态更新:可以直接在审查状态之间转换(例如,从已审查转换为待处理),无需经过重置为未审查(Unreviewed)的中间步骤。
启用和配置
版本发布时,此更新将自动启用。
列表访问
用例
此功能通过将用户的列表访问权限限制在特定类别,使用户能够专注于与其相关的数据,从而确保更高效的审查流程。
描述
配置用户现在可以通过 CDB 配置来全局管理列表权限和类别。利用这个支持继承的网格,他们可以根据类别定义研究角色可以执行的细粒度操作(查看、设置审查状态、创建、修改等)。
新的“列表访问(Listing Access)”页面面向具有配置 CDB(Configure CDB)权限的用户开放。
无法为不具有某项操作权限的角色提供该操作的列表访问权限。例如,如果某个角色没有修改列表(Modify Listing)权限,则该角色无法拥有修改列表的访问权限。
启用和配置
此功能自动可用,但具有配置 CDB 权限的用户必须添加列表类别并为这些类别设置访问限制。
导入错误与警告代码汇总
用例
对警告和错误代码进行分组可简化日志,帮助数据管理员快速识别与第三方数据导入相关的问题。
描述
导入页面上的问题日志现在提供了一个单独的问题摘要(Issues Summary)标签页,汇总了包处理期间识别的唯一错误和警告代码。
启用和配置
版本发布时,此功能将自动可用。
了解详细信息
清单生成器更新
用例
清单生成器的增强功能可确保更好的数据质量,并为用户构建清单文件(.json)以导入第三方和 OpenEDC 数据提供更好的体验。
描述
清单生成器已更新,包含以下功能:
- 清单生成器中针对以下数据类型的必填字段验证:
- 文本(需要长度)
- 浮点数(需要长度和精度)
- 日期、日期时间和时间(需要格式)
- 代码列表(需要代码列表)
- 配置验证将显示在清单生成器中:
- 文本长度必须在 1-3000 个字符之间
- 整数最小值必须大于或等于 -9,223,372,036,854,775,808
- 整数最大值必须小于或等于 9,223,372,036,854,775,807
- 浮点数长度必须在 1-24 位之间
- 浮点数精度必须在 0-7 位之间
- 浮点数最小值必须大于或等于 -999,999,999,999,999,999,999,999
- 浮点数最大值必须小于或等于 999,999,999,999,999,999,999,999
- 上传代码列表的功能:
- 新代码列表或向现有代码列表添加条目
- 提供导入模板 CSV
- 文本默认值现在设置为 500
- 对于向清单条目映射添加新条目,创建时将不再显示错误行
- 当数据类型更改时,任何已输入的属性将被清除
启用和配置
这些功能在发布时自动可用。
了解详细信息
揭盲规则部署
用例
为了对第三方数据的揭盲规则提供更好的控制,用户现在可以从 CDB 工作台应用程序将规则部署到生产环境。
描述
揭盲规则的部署确保只有批准的更新才会被添加到生产环境。这包括部署历史记录的审计,记录规则部署的对象、内容和时间。
通过此功能,一旦为研究启用了部署,生产环境中的揭盲规则将无法编辑。所有编辑必须在 TST 环境中进行。新的批准日志(可下载)将提供有关规则在 TST 环境中最后修改时间的信息。
启用和配置
此功能对于已启用部署的测试研究自动可用。
了解详细信息
导入审计更新
用例
导入审计跟踪中的新列和筛选器提供了有关导入数据包的更多信息,并有助于用户在查看多个审计记录时聚焦列表。
描述
第三方数据包审计包括两个新列:审计日期(Audit Date)(即审计记录创建的日期)和类型(Type)(表示该包是参考数据还是第三方源数据)。
用户还可以通过新的筛选器显示与上传日期(Uploaded Date)、上传者(Uploaded By)(用户)、导入日期(Imported Date)或状态相关的记录。
启用和配置
版本发布时,此功能将自动可用。
了解详细信息
新增第三方数据类型验证
用例
数据类型的验证确保数据符合清单描述的值,从而在导入期间获得更高质量的数据和更有效的错误检测。
描述
系统现在对清单中配置的数值和文本数据类型提供了新的验证,并支持 MySQL BigINT 数字(即超过九(9)位的数字)。
对文本条目定义的验证将确保配置的长度大于零(0)且小于或等于 3000。如果文本字段的长度不符合最小和最大长度要求,新的警告 D-039(大于 3000)和 D-040(长度小于一(1))将显示并设置清单中的值。
在清单中被定义为浮点数的数字将进行新的验证,并产生警告 D-041 至 D-046,以确保条目定义 的长度至少为一(1)位且不超过 24 位。配置的最小值和最大值不能小于 -999,999,999,999,999,999,999,999,也不能大于 999,999,999,999,999,999,999,999。
在清单中定义为整数的数字将进行新的验证,并产生警告 D-049 至 D-052,以确保配置的最小值和最大值在支持的范围内。配置的最小值和最大值不能小于 -9,223,372,036,854,775,808,也不能大于 9,223,372,036,854,775,807。
启用和配置
此功能在发布时自动可用。
了解详细信息
待批准时的第三方数据导入通知
用例
用户现在在其上传的包处于待批准状态并需要在 CDB 工作台中采取行动时,会收到通知。
描述
上传第三方数据包时,如果该包处于待批准状态并需要采取行动(批准),用户现在将收到通知。无论这是来自此来源的第一个包,还是对先前批准的包清单的更改,都会触发此通知。
此功能适用于 Veeva EDC 和 OpenEDC 研究。
启用和配置
此功能在发布时自动可用。
了解详细信息
新增患者清理跟踪器列
用例
新增的列支持更好地审查研究中的受试者,并了解受试者在事件计划中的位置,特别是在使用重复事件组时。
描述
患者清理跟踪器现在包括子研究(Substudy)和最新事件组(Latest Event Group)列,以便在查看跟踪器时提供更多背景信息和筛选选项。
启用和配置
版本发布时,此功能将自动启用。
在 CDB 中支持 JDrug 编码词典
用例
对于使用 JDrug 编码词典的 Veeva Coder 研究,CDB 中提供的 JDrug 支持在更丰富的列表中包含合并用药等药物表单的日文编码术语。
描述
JDrug 编码词典值现可在 CQL、SFF 和原始导出中使用。原始导出的更新包括为所有配置了 MedDRA、WHODrug 和 JDrug 词典的表单添加了“DictionaryType”和“UserCodedBy”列。新的 JDrug 词典值将适用于在 Veeva EDC 中配置了 JDrug 编码词典的表单。
启用和配置
此功能自动可用。
了解详细信息
列表筛选菜单重新设计
用例
筛选器的改进支持更高效地审查列表、视图、检查、方案偏离、质疑和观察。
描述
不同数据类型的筛选器将具有以下相似的操作:
- 操作符选择器已更改为下拉菜单
- 清除(Clear)可将筛选器重置为其默认状态
- 确定(OK)将关闭筛选器菜单并根据所选选项更新列表
- 取消(Cancel)将关闭筛选器菜单而不执行任何操作
- 确定和取消将始终可见,即使选项列表需要滚动条才能查看所有筛选选项
- 在输入字段中按 <kbd>Enter</kbd> 键也将应用筛选器更改并关闭筛选器菜单
根据列的数据类型进行了更新:
- 文本字段(当值列表已知时,例如代码列表)将在复选框列表中显示每个条目。默认情况下,条目未选中,可以选择“全选(Select All)”或从选项中选择以将列表筛选为仅选中的条目——还有进一步选项可以选择“包含(Contains)”、“完全匹配(Is exact match)”或“不匹配(Does not match)”,这些选项会显示一个文本框以输入自由文本
- 文本(当值列表未知时,例如 AETERM 列),即 EDC 中的自由文本录入,默认选中“包含”选项——还有进一步选项可以选择“不包含(Does not contain)”、“开头为(Starts with)”、“结尾为(Ends with)”、“为空(Is empty)”、“不为空(Is not empt)”、“在(In)”、“不在(Not in)”、“完全匹配”和“不匹配”
- 选择“完全匹配”或“不匹配”时会显示“文本比较(Text Comparison)”选项
- 数值选项包括“等于(Is equal to)”、“不等于(Is not equal to)”、“为空”、“不为空”、“大于(Is greater than)”、“大于或等于(Is greater than or equal to)”、“小于(Is less tha)”、“小于或等于(Is less than or equal to)”、“在”、“不在”和“之间”——对于“在”和“不在”操作符,用户可以输入逗号分隔的值列表
- 选择“等于”、“不等于”、“大于”、“大于或等于”、“小于”或“小于或等于”时会显示数值比较选项
- 计量单位(UOM)选项保持不变——筛选值时,会显示“计量单位(Unit of Measure)”下拉菜单,允许筛选使用不同单位收集的数据
- 选择“等于”、“不等于”、“大于”、“大于或等于”、“小于”或“小于或等于”时会显示 UOM 比较选项——当用户单击比较(Compare)按钮时,输入字段将替换为下拉菜单
- 布尔值提供复选框以按“真”、“假”、“空白”和“全选”筛选列表
- 日期、时间和日期时间值显示“晚于(Is after)”、“早于(Is before)”、“为空”、“不为空”,以及“介于之间(Is between)”
- 选择“晚于”或“早于”时会显示时间、日期和日期时间比较选项——当用户选择“比较”按钮时,输入字段将替换为下拉菜单。
工作台审查列表中的筛选器支持根据审查状态、质疑状态和观察状态进行筛选。这些筛选器的更新包括:
- 所有筛选值默认将取消选中
- 当取消选择“全选”时,该类别下的所有值都将取消选中
启用和配置
这些更新在发布时自动启用。
CDB 网格改进
用例
列表屏幕尺寸利用率的改进提升了用户的使用体验,使数据审查更加便捷——无论用户是使用较小屏幕,还是希望通过将单元格详情面板移动到新窗口的同时仍能查看列表行来更好地聚焦数据视图。
描述
此版本改进了列表屏幕,以更有效地利用可用空间。用户现在可以弹出单元格详情面板,这将自动最大化网格。用户还可以使用新对话框显示和隐藏列,因此你不再需要一次选择一个列来隐藏或显示单个列。
启用和配置
这些更改在发布时自动应用。
更新审查列表时间阈值
用例
刷新时间更新后,运行时间较长的列表可在有限的基础上进行刷新。
描述
审查列表时间阈值已更新,因此运行时间超过 30 秒(最长 5 分钟)的列表在连续 50 次运行超过 30 秒后,将每天刷新一次。CDB 将自动禁用任何运行超过五分钟的列表。
启用和配置
版本发布时,此功能将自动启用。
我的观察任务在审查列表中的筛选
用例
能够筛选审查列表以仅显示已分配的观察,使用户可以轻松找到并处理分配给他们自己的观察。
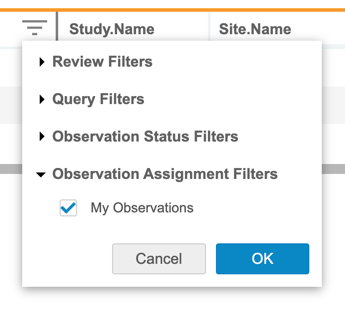
描述
审查列表筛选器有一个新选项观察任务(Observation Assignment),可以筛选以仅显示分配给当前用户的观察。
启用和配置
版本发布时,此功能将自动可用。
列表数据网格改进
用例
列表屏幕尺寸利用率的改进提升了用户的使用体验,使数据审查更加便捷——无论用户是使用较小屏幕,还是希望通过将单元格详情面板移动到新窗口的同时仍能查看列表行来更好地聚焦数据视图。
描述
此版本改进了列表屏幕,以更有效地利用可用空间。打开单元格详情面板将自动最大化网格。你可以将详情面板弹出到新窗口,以便完全查看列表数据。用户还可以使用新对话框显示和隐藏列,因此你不再需要一次选择一个列来隐藏或显示单个列。
其他增强功能包括:
- “展开网格(Expand Grid)”按钮已更新为“最大化(Maximize)”或“最小化(Minimize)”网格,为数据网格利用更多屏幕空间。
- 选择质疑、观察或方案偏离的单元格装饰将打开单元格详情面板中的相应部分。
- 上下文筛选:新的网格级选项支持用户通过特定单元格值即时筛选结果。只需悬停在任何单元格上即可显示筛选快捷方式。
启用和配置
这些更改在发布时自动应用。
研究文件格式 API 增强功能
用例
SFF 的改进为下游系统增加了该格式的价值。
描述
此版本包含以下 SFF 改进:
- SFF 提取现在包含一个源列,显示数据的来源名称(EDC 或第三方数据源名称)
- 质疑文件新增了来源(Origin)信息和快速质疑(Quick Queries)的列
- 标签文件现在包含第三方数据(仅限 CDB 工作台)
- 我们移除了 EDC 工具中为 OpenEDC 研究开启 SFF 的选项(仅限 CDB 工作台)
- SYS_Links CSV 文件现在包含条目到表单的链接信息
- 完整的 SFF 包现在在本地 Vault 时间中午可用
- 我们为第三方数据包含了额外的方案偏离信息
启用和配置
这些更新在发布后自动应用于所有 SFF API 包。
了解详细信息
将作业 ID 添加到清单和导出日志
用例
为工作台和临床报告导出作业提供唯一标识符有助于提高故障排除效率和可追溯性。
描述
此版本将作业 ID 添加到工作台和临床报告导出作业的导出 manifest.json 文件和导出作业日志中。
启用和配置
版本发布时,此功能将自动可用。
了解详细信息
临床报告实验室标签的增量导入更新
用例
在实验室模块中更改标签时使用增量导入,确保小更改不需要完全重新处理研究数据。
描述
对实验室代码列表或单位条目的标签更改现在将添加到来自 EDC 的增量导入中。这仅适用于使用全局版本实验室的研究。
启用和配置
版本发布时,此功能将自动可用。
在未找到受试者警告时重新处理第三方数据
用例
生产研究中的自动重新处理提供了一种方式来协调在不同时间进入系统的数据,并确保来自第三方提供商的数据与病例手册记录匹配,以避免来源之间的数据协调。
描述
在生产环境中,第三方数据的自动重新处理由警告触发。D-032 警告现在也将触发重新处理。该警告的消息已更新为:“未找到受试者名称。受试者名称 [受试者名称] 的研究中心确定失败(Subject Name Not Found. Site determination failed for subject name: [subject name])”。
启用和配置
版本发布时,此功能将自动可用。
基于数据类型的第三方数据掩蔽
用例
数据类型掩蔽确保在将数据摄取到下游系统时,具有已设盲列和揭盲规则的列表保持数据类型。
描述
在此版本中,通过 CDB 工作台配置中的一个新选项,可将数据类型掩蔽应用于 Vault 中的所有研究。数据类型掩蔽将应用于整数、小数、日期、时间和日期时间数据类型。
以下值将用于根据列的数据类型显示该值已设盲:
- 整数列在 UI 和导出中将显示 -2147483648
- 小数列在 UI 和导出中将显示 -9999.9999(在此版本中,审查列表将显示 -10000)
- 日期列在 UI 中将显示 Jan 1, 1583,在导出中将显示 1583-01-01
- 时间列在 UI 和导出中将显示 00:00:00
- 日期时间列在 UI 中将显示 Jan 1, 1583 12:00AM,在导出中将显示 1583-01-01 00:00:00
日期时间条目的 SAS 文件格式将更新为 DATETIME19。
启用和配置
版本发布时,此功能将自动可用。
CDB 用户会话管理
用例
统一用户会话,消除用户在 CDB 工作台中活跃工作时被登出的困惑。
描述
CDB 用户会话现在将保持 Vault 会话活跃,并与 Vault 设置保持一致,确保 EDC 和 CDB 中的访问权限一致,并符合 Vault 的设置。
启用和配置
版本发布时,此功能将自动可用。
CDB API
以下是 CDB API 的新功能。请参阅我们的开发者门户的发行说明,了解更详细的功能信息。
CDB API 功能
该版本为 CDB 开发者提供了以下功能:
- CDB 检索质疑 API
- 研究文件格式 API 增强功能
EDC 迁移器
本部分中的功能是针对 Veeva EDC 迁移器的新功能。
迁移器和 YAML 生成器更新
用例
为提高迁移过程中的效率,我们实施了多项增强功能。以前,即使研究不需要医疗编码步骤,用户也必须等待该步骤完成。现在,你可以绕过该步骤以节省时间。设置实验室表单过去需要对不同研究的每个分析物进行单独映射;现在系统使用实验室头文件自动识别正确的数据列。我们还支持未知的实验室时间,免去了提供特定时间的必要,并允许更现实的数据摄取。以前在迁移过程中覆盖实验室正常值时,EDC 审计跟踪中缺少更改原因,但现在已包含在内。最后,我们将实验室代码列表视为标准条目,免去了为其执行额外配置步骤的必要。
描述
此版本引入了以下更新:
- 在执行所有步骤(Execute All Steps)对话框中添加了一个新的跳过医疗编码(Skip Med Coding)复选框,允许用户绕过编码步骤并在迁移报告中将其标记为已跳过(Skipped)。
- 我们现在将实验室正常值覆盖原因直接显示在 EDC 审计跟踪中。
- YAML 构建器现在将实验室结果视为传统代码列表条目,当列名匹配时,无需进行
labCodelistValue。 - 我们利用“labheader.yaml”文件自动识别不同研究中实验室结果分析物值的源数据列。
- 我们现在利用 DateTime TimeNotRequired 模板自动将未知的实验室时间替换为“UN”值,以满足后端要求。
启用和配置
此功能自动启用,但要使其在迁移期间工作,必须在正在迁移的研究中启用研究选项启用“存在未处理的质疑时签名”(Enable Sign with Open Queries)。
迁移器支持签署含未处理质疑的病例手册
用例
目前,在迁移过程中,如果病例手册包含未处理的质疑,即使研究中启用了 EDC 的启用“存在未处理的质疑时签名”设置,迁移器也会阻止其进行电子签名。此功能消除了这一行为,确保在研究配置为允许存在未处理质疑时签名的情况下,迁移的研究能够保留源数据中定义的正确签名状态。
描述
此增强功能允许迁移器在目标研究中启用了相应 EDC 设置的情况下,即使病例手册或表单包含未处理的质疑,也能对其应用电子签名。
在迁移期间,迁移器会检查 EDC 工具 > 研究选项中是否启用了启用“存在未处理的质疑时签名”设置:
- 如果该选项被禁用,迁移器将保持现有行为,不会对存在未处理质疑的病例手册应用签名。
- 如果该选项被启用,迁移器将继续按照迁移输入数据中的指示应用签名,而不会因存在未处理质疑而阻止。
启用和配置
此功能自动启用,但要使其在迁移期间工作,必须在正在迁移的研究中启用研究选项启用“存在未处理的质疑时签名”(Enable Sign with Open Queries)。
为迁移器启用 CDB 增量设置
用例
以前,EDC-CDB 的高速集成选项在迁移环境中受到限制。为了解决了这一限制,此更新允许管理员直接在迁移研究设置中打开或关闭 CDB 集成的增量数据流。
描述
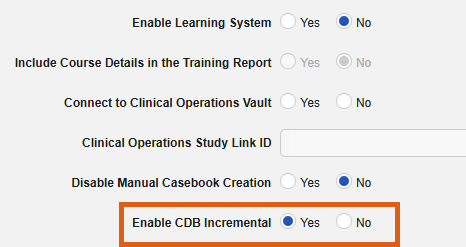
此功能针对迁移研究增强了其数据集成设置的可见性和控制力。管理员现在可以在被指定为迁移(Migration)类型的任何环境中查看和编辑研究设置中的启用 CDB 增量(Enable CDB Incremental)设置。
为了简化监督,该设置的状态也显示在研究环境网格的 CDB 增量(CDB Incremental)列中,方便用户一目了然地看到哪些迁移研究配置了增量数据同步。
启用和配置
启用 CDB 增量设置仅在 CDB 增量功能配置后才可用且可编辑。此功能在发布时对迁移器可用。
安全集成:在 EDC 切换期间暂停安全病例数据传输
用例
在将研究从传统 EDC 系统迁移到 Veeva EDC 时,由传统 EDC 发起的安全病例在安全系统中已存在。在迁移过程中将来自传统 EDC 的安全相关数据加载到 Veeva EDC 中时,将启动从 Veeva EDC 的首次安全病例传输,并可能在安全系统中创建重复病例,或增加额外的收件箱条目,而这些条目必须链接到现有病例。
此项新功能支持将安全数据迁移到 Veeva EDC 或执行发布程序,而不会不必要地生成将安全病例消息传输到安全系统的操作。这显著降低了任何 EDC 迁移或发布程序期间安全病例处理的负载,同时一旦任何切换程序完成,常规随访流程将自动恢复。
对于安全-EDC 连接,此项新功能还允许在需要时(例如在发布程序期间)抑制安全病例随访消息的创建。
描述
此功能引入了支持 EDC 数据迁移的逻辑,包括:
- 启动操作,该操作将启动重复的初始安全病例传输,或抑制因 EDC 更新(例如在发布管理期间)而产生的不必要的随访消息。
在开始 EDC 迁移程序之前,必须在传统 EDC 系统中运行最终的完整安全扫描,以确保所有因 EDC 数据变更而产生的随访消息都已传输到安全系统。在迁移期间,EDC 安全数据、相关的安全病例元数据和迁移指示器由 Vault 所有者上传到 Veeva EDC。作为最终迁移程序的一部分,将在 Veeva EDC 中执行一次完整的临时随访扫描作业。对于使用安全-EDC 连接的研究,迁移研究中的病例现在会自动链接到现有的 Veeva Safety 病例,而不会在 Veeva Safety 中创建任何不必要的收件箱条目。然而,额外的受试者信息将在 Veeva Safety 中更新,供安全团队按需审查。对于使用 E2BLink 的研究,这些病例将创建一个 E2B.XML 文件,该文件不会传输到 AS2 网关,但会模拟成功传输。
安全病例现在在安全系统中注册。随访扫描作业将按计划执行,并在任何安全病例数据发生变更时创建随访消息。
对于安全-EDC 连接,如果需要,此项新功能也可用于抑制安全病例数据传输。为此,必须执行一次完整的临时随访扫描,Vault 所有者必须在 Veeva EDC 中为所有受影响的安全病例设置“暂停传输”指示。在切换程序完成后,必须另外执行一次完整的临时随访扫描。虽然此完整扫描不会触发向 Veeva Safety 发送随访消息,但它将自动恢复由研究中心发起的实际安全病例更新的常规随访扫描作业。
启用和配置
此更改将自动应用。