25R1 新增功能
预发布日期:2025 年 3 月 17 日 | 发布日期:2025 年 4 月 4 日和 11 日我们很高兴为你带来 Veeva Clinical Data 25R1。请阅读下文了解新功能。有关新功能启用的信息,请参阅 25R1 功能启用详细信息。
临床数据
本部分中的功能是对 Veeva EDC 和 CDB 所有应用领域都适用的更改。
名称和徽标更改
说明
在此版本中,Vault CDMS 现在已更名为 Veeva Clinical Data。Veeva 最近已将 Vault 应用程序品牌名称从 Vault [Application] 更新为 Veeva [Application]。根据这一更新,“Vault EDC”和“Vault 编码器”现在称为“Veeva EDC”和“Veeva 编码器”。这些更改会反映在 25R1 版本的用户界面中,具体包括左上角横幅中显示的徽标、标准登录页面、“我的 Vault”页面(如果启用)以及电子邮件通知中使用的徽标。
启用和配置
这些更改将自动应用。
数据录入
本部分中的功能是对数据录入选项卡的变更,该选项卡是研究者和临床研究协调员输入研究执行数据的工作区域。
批量签名可见性和按钮更新
用例
为了帮助减少对签名功能的困惑,“数据录入(Data Entry)”中的“对病例手册进行签名(Sign Casebooks)”按钮已重新标记为“Bulk Sign Casebooks(批量签名病历手册)”,并且现在所有研究的“研究中心(Site)”网格页面上都可以查看该按钮。这些更改可以提高主要研究者对批量签名功能的意识。
说明
在此版本之前,当某个研究或研究中心未使用批量签名设置时,“数据录入”中的病例手册网格页面上的批量签名病历手册按钮(已重命名为对病例手册进行批量签名)会处于隐藏状态。现在,对于所有研究,该按钮都可见。同样,在研究中心网格中,研究中心编号旁边的操作菜单中现在会显示批量签名病历手册选项。根据你在“EDC 工具(EDC Tools)”中的“研究设置(Study Settings)”,该按钮和菜单选项将处于启用或禁用状态。该按钮被禁用的原因可能有多种。如需了解更多信息,可将鼠标悬停在病例手册网格和研究中心网格操作菜单中的该按钮上。
启用和配置
该按钮对于所有 Vault 上的所有研究自动可用,不再被列为 Vault 的功能启用标志的一部分。该按钮和菜单操作是否可供选择将取决于 EDC 工具中的现有研究和研究中心设置。对于新研究和研究中心,该设置将默认为“是(Yes)”。对于现有研究,该功能可在 EDC 工具中启用。
针对查询的 ILB 行为更新
用例
以前,如果研究中心用户将条目或整个表单标记为“特意留空(Intentionally Left Blank)”,则当选择了 ILB 时,现有的查询将被关闭。
说明
此功能将关闭查询的依赖关系从 ILB 操作更改为规则引擎,由规则引擎来决定查询是否将关闭。如果规则的条件不再成立,则根据现有的规则行为,查询将自动关闭。
启用和配置
这些更新自动可用。
突出显示计划外事件的必填字段
用例
以前,在添加计划外事件时,研究中心用户未能充分意识到遗漏了必填字段,并且在某些情况下很疑惑为何“保存(Save)”按钮没有启用。这一改进为研究中心用户提供了清晰的计划外事件对话框,并使用户体验与 EDC 的其他区域更一致。
说明
现在,当添加计划外事件时,保存按钮会一直处于启用状态。留空的必填字段会在对话框中突出显示,且字段下方会显示错误消息。
启用和配置
这些更新自动可用。
针对单一团队、多角色和多研究中心用户的查询团队更新
用例
查询团队功能和查询对话框已作出改进。这些增强功能有助于明确在添加查询时分配了哪个查询团队,并自动分配准确的查询团队。
说明
具有多角色和多研究中心访问权限的用户:现在,当用户属于该研究中心的单一查询团队时,系统将自动为用户分配相应的查询团队。使用多角色安全性时,即用户的角色属于研究中心的多个查询团队,则系统将显示选择器供用户选择适当的查询团队。
属于单一查询团队的用户:打开查询时,查询对话框将立即显示用户的查询团队。这有助于向用户显示他们输入查询时所属的团队。
启用和配置
这些更新自动可用。
受试者 ID 区分大小写
用例
当研究中心或外部系统输入用于创建受试者 ID 的条目时,如果使用大小写不同的相同字符,可能会导致下游问题。此更新强制对受试者 ID 区分大小写,并防止在添加受试者 ID 时出现重复。
说明
为了防止受试者 ID 值重复,引入了区分大小写功能。此功能适用于在工作室 (Studio) 中设置了受试者 ID 生成方式为手动 (Manual) 的研究。研究中心用户将看到屏幕上显示一个错误,提示他们研究中心已存在相关的受试者。当用户离开表单时,系统分配的筛选 ID(SCR-###)将一直保留到受试者 ID 被修改为止。区分大小写也适用于通过外部系统使用 API 填充的受试者 ID。发送大小写不同的相同受试者 ID 会导致收到错误。
启用和配置
此增强功能自动可用。
针对条目更改原因的可用性改进
用例
以前,在某些修改表单数据的情况下,当表单处于“进行中提交后(In Edit)”状态时,研究中心用户无法持续看到选定的更改原因。
说明
为了清楚起见并提高可用性,在用户为条目选择更改原因后,修改后的更改原因现在将一直显示到用户提交表单为止。此外,对于使用本地实验室的研究,更改原因下拉列表需等到用户编辑实验室标题中的值时才会显示。
如果用户在编辑表单时清除更改原因,他们不会再看到空白选择。他们仍将看到下拉列表,并且错误文本将显示:“错误:需要提供更改原因(Error: Change reason is required)”。
启用和配置
这些更新自动可用。
数据审查
本部分中的功能包括对审查(Review)选项卡(临床研究监查员和数据管理员的工作区域)或数据录入选项卡中审查功能的更改。
更新了表单进度列表(Form Progress Listings) 中的列名称
用例
此功能提高了对表单进度列表的理解。
说明
表单进度列表中的以下列已更新:
| 当前名称 | 新的列名称 |
|---|---|
| SDV 覆盖计划 | 表单 SDV 覆盖计划 |
| 需要 SDV | 表单需要 SDV |
| 需要 Re-SDV | 表格需要 Re-SDV |
| SDV 完成 | 表单 SDV 完成 |
| SDV % | 表单 SDV % |
| SDV 时效 | 表单 SDV 时效 |
| 首次 SDV 完成日期 | 表单首次 SDV 完成日期 |
| SDV 完成日期 | 表单 SDV 完成日期 |
| DMR 覆盖计划 | 表单 DMR 覆盖计划 |
| 需要 DMR | 表单需要 DMR |
| 需要 Re-DMR | 表单需要 Re-DMR |
| DMR 完成 | 表单 DMR 完成 |
| DMR % | 表单 DMR % |
| DMR 时效 | 表单 DMR 时效 |
| 首次 DMR 完成日期 | 表单首次 DMR 完成日期 |
| DMR 完成日期 | 表单 DMR 完成日期 |
启用和配置
此增强功能在版本发布时自动可用。
了解详情
事件进度列表(Event Progress Listings) 更新
用例
为了支持研究审查活动,我们添加了新的列,对一些列进行了重命名,并更新了相关逻辑,以提高事件进度列表的可用性。
说明
- 添加了新的列,用于显示如果完成审查后数据发生更改且审查状态被清除,哪些地方需要进行 Re-SDV 和 Re-DMR
- 对于没有事件日期或访视方法的日志事件,“事件日期(Event Dates)”和“访视方法已冻结(Visit Method Frozen)”、“已锁定(Locked)”和“已签名(Signed)”列的逻辑已更新,现在将显示为空白而不是“否(No)”
此外,事件进度列表中的以下列名称已更新:
| 当前名称 | 新的列名称 |
|---|---|
| 事件日期首次 SDV 完成日期 | 事件日期首次 SDV 完成日期 |
| 事件日期 SDV 完成日期 | 事件日期 SDV 完成日期 |
| 访视方法 SDV 完成日期 | 访视方法 SDV 完成日期 |
| 表单 SDV 百分比 | 已完成 SDV 的表单百分比 |
| 事件日期首次 DMR 完成日期 | 事件日期首次 DMR 完成日期 |
| 事件日期 DMR 完成日期 | 事件日期 DMR 完成日期 |
| 访视方法 DMR 完成日期 | 访视方法 DMR 完成日期 |
| 表单 DMR 百分比 | 已完成 DMR 的表单百分比 |
| 冻结日期 | 事件冻结日期 |
| 锁定日期 | 事件锁定日期 |
启用和配置
此增强功能在版本发布时自动可用。
了解详情
提取作业调控器功能优化
用例
这些更新支持研究更灵活地每日多次安排作业,而无需担心受限数据(Restricted data) 的作业选项。
说明
我们取消了基于“受限”状态对作业调控器施加的限制,并将某些列表作业的每日限制提高到每个研究 4 个作业。受此功能影响的作业包括研究数据提取(Study Data Extract)、研究进度列表(Study Progress Listings)和研究进度版本化提取(Study Progress Versioned Extracts)。针对研究摘要指标报告(Study Summary Metrics Report)和附加审查列表(Additive Review Listing)作业的“受限”状态约束将取消,但这些作业仍将限制为每个研究两个计划作业。
我们还在非生产环境中为“审计跟踪导出(Audit Trail Export)”作业添加了“活动期(Active Period)”选项,该选项将显示在 24R3.4 限定版本中。
启用和配置
此增强功能在版本发布时自动可用。
了解详情
在事件列表、提取和报告中包含日志事件
用例
这些更新在使用事件操作摘要记录的列表、提取和报告中提高了 SDV、DMR、冻结、锁定和 PI 签名的可见性。
说明
日志事件现在将包含在事件操作摘要记录中。由于日志事件和计划事件之间存在差异,日志事件摘要中的某些字段的表现会有所不同。这些不同的表现情况将在版本发布后记录在 CDMS 帮助网站上。
这些记录显示在事件进度列表(Event Progress Listing)、SYS_EVT 数据集、“标准模板:时间表偏差报告(V3)(Standard Template: Schedule Deviation Report (V3))”标准报告以及基于“事件进度列表”或“事件操作摘要(Event Operational Summary)”报告类型的任何自定义报告中。
启用和配置
此增强功能在常规版本中自动可用。
已更新查询详细信息列表(Query Detail Listing)中的列名称
用例
为了提高对查询详细信息列表的理解,我们更新了列名称。
说明
我们更新了查询详细信息列表中的以下列名称:
| 当前名称 | 新的列名称 |
|---|---|
| 回答日期 | 查询回答日期 |
| 回答者 | 查询回答者 |
| 关闭日期 | 查询关闭日期 |
| 关闭者 | 查询关闭者 |
启用和配置
此增强功能在版本发布时自动可用。
了解详情
审查:Vault 所有者(Vault Owner) 对计划作业的访问权限
用例
借助此功能,Vault 所有者可以更好地查看“审查(Review)”选项卡的“作业计划(Job Schedule)”区域中的所有作业。
说明
Vault 所有者现在能够修改其他用户创建的作业。他们可以在审查选项卡中看到所有计划的作业,并能够编辑、删除作业或将作业设置为立即运行(Run now)。这些作业包括:
- 附加审查列表
- 核心列表
- 数据导出(旧版)
- 详细 PDF
- 事件进度列表
- 表单进度列表
- 查询详细信息列表
- 研究摘要指标报告
- 受试者进度列表
启用和配置
这些增强功能将自动可用。
事件摘要更新:事件日期和表单输入逾期
用例
这些增强功能有助于进行报告处理,并为使用数据模型 2 的研究提供更好的支持。
说明
对报告区域中的“事件操作摘要”报告类型进行了后端更新。作为用于辅助处理报告数据的临时字段,“事件日期”查找字段现在已不再需要,因此已被弃用。事件操作摘要中的表单输入逾期天数计算公式已更新,现在包括使用数据模型 2 的研究。现在,该公式在计算中会同时考虑 event__v.event_status__v 和 event_summary__v.event_status__v。
启用和配置
此增强功能自动可用。
UI/UX 更新:调色板和徽章颜色
用例
这些是对颜色和样式的持续改进,旨在提高可见性,使 EDC 更易于用户访问。
说明
特定样式(包括徽章上的形状高度、文本大小和背景颜色更新)增加了对比度,从而提升了“审查”、“EDC 工具”和“系统工具(System Tools)”选项卡的显示效果。徽章的更新可以在记录状态(例如“未处理(OPEN)”、“完成(COMPLETE)”、“待定(PENDING)”、“非活动(INACTIVE)”等)和研究环境(例如 DEV、TST、PPT、PROD)上看到。此更改也体现在“我的研究中心(My Study Sites)”页面以及“审查”选项卡中类似页面的页眉图标背景颜色上。
启用和配置
这些更改将自动应用。
临床编码
以下是 Veeva Coder 的新功能(Veeva Coder 的临床编码区域)。
“传播编码”操作的编码源
用例
现在,无论配置的最终状态如何,由于“传播代码(Propagate Code)”操作而应用的编码更新都可以通过受影响代码请求上的手动源字段清楚地加以识别。
说明
当编码器使用对所有表单进行编码并更新同义词列表(Code All Forms and Update Synonym List)操作将编码决策传播到所有匹配的已编码代码请求(Code Requests)和同义词列表(Synonym List)记录时,Veeva 编码器会将这些编码更新反映为手动编码操作。手动源(Manual Source)字段已更新为传播代码,对于受影响的代码请求,所有以前的自动编码属性字段都将被清除。
启用和配置
这些更新自动可用。
了解详情
编码器摘要页面的列更新
用例
我们更新了编码器“摘要(Summary)”页面,以提高“编码查询(Coding Query)”状态的可见性。
说明
未处理的查询(Open Queries)列现在将反映等待研究中心操作的查询计数。新的已回答的查询(Answered Queries)列将反映研究中心已回答、等待审查和关闭的查询计数。
启用和配置
这些更新自动可用。
了解详情
针对同义词列表记录审批的新验证
用例
此更新改善了用户在同义词列表记录审批期间的体验。
说明
该版本新增了针对同义词列表记录审批的验证警告。当用户尝试批准一条同义词列表记录时,如果同一同义词列表中已存在一个处于激活状态且代码不同的匹配同义词列表记录,则该批准操作将被阻止。
启用和配置
这些更新自动可用。
了解详情
代码请求列表筛选器和列更新
用例
在此版本中,我们对编码器代码请求列表筛选器和列进行了更新,以提高可用性和用户的效率。
说明
进行了以下更新:
- 以下筛选器将具有“粘性”,一旦配置,将在单个会话期间对所有编码表单类型保持生效:
- 列表视图:编码状态(Coding Status)、查询状态(Query Status)
- 组视图:编码状态(Coding Status)
- 更新了受试者筛选器,以显示所有受试者,而无论受试者状态如何。以前,状态为“筛选前(Pre Screening)”、“筛选中(In Screening)”或“筛选失败(Screen Failure)”的受试者不会显示。
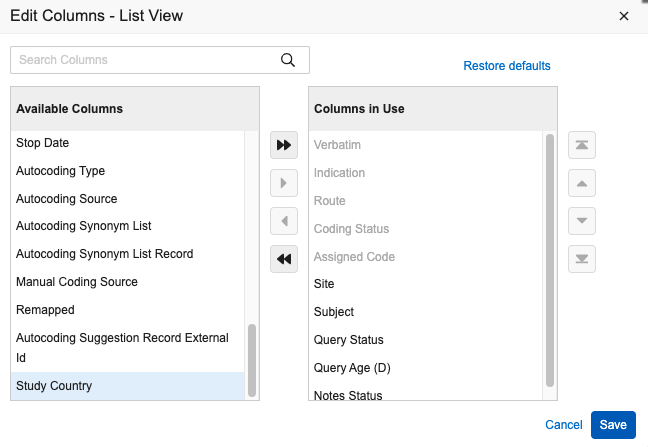
- 现在可以向列表视图添加研究国家/地区(Study Country)列
- 代码请求的时效(天数)(Code Request Age (D))列标签已更新为逐字时效(天数)(Verbatim Age (D))。此外,如果将该列添加到表中,则会启用排序。该字段的计算逻辑也已更新,不管当前编码状态如何,都将根据今天的日期 - 上次未编码日期派生以天为单位的时效。
启用和配置
这些更新自动可用。
了解详情
编码器工具 UI 更新:传播代码的最终状态
用例
此更新提高了“编码器工具(Coder Tools)”>“研究设置”中的清晰度和一致性。
说明
在编码器工具中将“编码系统(Coding System)”设置为“第三方系统(Third-Party System)”时,“传播代码的最终状态(Final State for Propagate Code)”设置现在不可编辑。以前,该设置可编辑,但没有功能上的影响。
启用和配置
此功能自动可用。
更新“等待批准”操作的审计跟踪文本模板
用例
此更新提高了针对“等待批准(Pending Approval)”操作的审计跟踪条目的清晰度和一致性。
说明
针对“等待批准”条目的审计跟踪文本已更新,以涵盖所有可以将代码请求移动到”等待批准“状态的情况。
启用和配置
此功能自动可用。
成像
以下是 Veeva EDC 的成像检查模块“Veeva EDC 成像”的新功能。
评估:成像可见性
用例
评估员可以更好地查看“评估(Assessments)”区域中的已上传检查和成像条目。
说明
如果在工作室中将表单的成像条目组中的以下条目配置为可见,则可以在“评估”的补充数据部分中查看它们:成像检查(Imaging Exam)、预期模态(Expected Modality)、已上传模态(Uploaded Modality)、检查日期(Exam Date)和接收编号(Accession Number)。“成像检查”值是一个可单击的链接,用于在模态窗口中打开已上传的检查。用户可以从模态窗口下载检查。
启用和配置
在成像研究的工作室配置中自动可用。
了解详情
成像:用于多帧导航的垂直滚动
用例
改进了查看已上传的成像检查时的可用性。
说明
为包含多帧的已上传成像检查添加了垂直滚动条。这样一来,在验证和查看已上传的图像时,用户可以垂直滚动浏览一系列帧。为了辅助导航,图像文件名旁边会显示当前帧编号和总帧数。
启用和配置
对于包含 Vault EDC 成像的研究,自动可用。
针对成像的 UI/UX 更新:上传抽屉和网格筛选
用例
这些用于成像研究的 UI 增强功能提高了面向研究中心和成像用户的可见性。
说明
上传抽屉更新了样式,现在,在网格视图中筛选值时,“取消(Cancel)”和“应用(Apply)”按钮更加显而易见。
启用和配置
在使用成像的研究中,这些更改会自动应用。
研究设计和配置
此区域中的功能适用于工作室,即 Veeva EDC 的研究设计和配置区域。
比较规则 V2
用例
新版本的“比较规则(Comparison Rules)”为日期和日期时间比较的编程提供了更高的灵活性和效率,以便研究设计者轻松地为更加多样化的场景配置规则。通过此项改进,用户可以将更多用户定义的规则(User Defined Rules)替换为比较规则,大幅减少了需要花在编程、单元测试、验证、UAT 和故障排除上的时间和精力。
说明
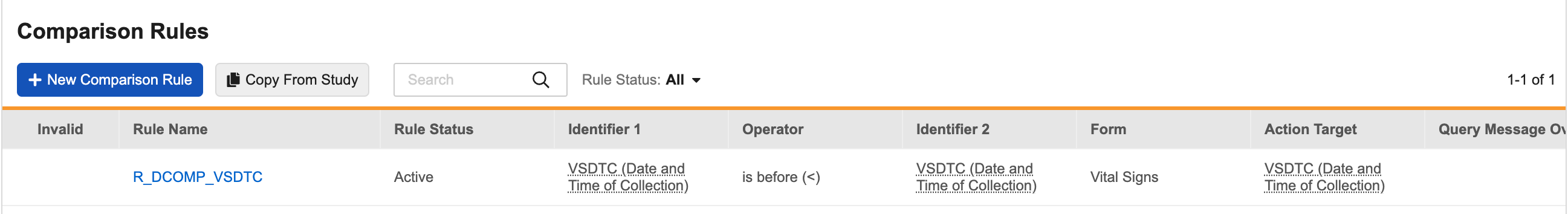
比较规则 V2 引入了一个新的 UI,提高了研究设计者在配置规则时的效率和灵活性。所有用于比较两个日期和日期时间值的查询规则现在都可以编程为系统管理的比较规则。关键的增强功能包括:
- 支持在日期和日期时间数据类型之间进行比较,包括用于日期时间转换的自动时区处理
- 允许使用非完全限定的标识符,包括浮动表单、事件和事件组
- 可配置针对自动处理未知值的最小值/最大值设置
- 两个事件日期或病例手册变量之间的比较
- 可配置用于重复事件组、表单和条目组的序列号
- 针对规则操作(rule action)的选项,可选择将比较规则中使用的任意一个标识符作为目标
- 支持从其他研究/库集合中复制比较规则
- 支持对比较规则进行重命名
- 添加了可立即向用户显示配置错误的 UI 验证
- 支持用户停用比较规则并对其进行存档*
对比较规则进行存档现在会将其从研究中永久移除,其作用更像是删除对象。这是比较规则 V2 特有的行为,不会影响针对用户定义的规则的存档行为。
启用和配置
此功能对新研究自动可用。要对现有研究启用此功能,请联系支持人员。
了解详情
用于重复条目组的其他默认值
用例
为了进一步满足研究设计要求,研究设计者可以在重复条目组上配置其他默认条目。新的 UI 减少了输入值时所需的点击次数,进而提高了设计效率。
说明
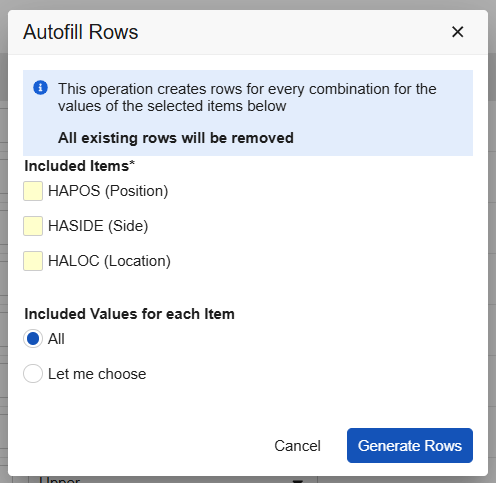
实施了一个新的 UI,用于在条目组属性中选择默认数据选项。研究设计者可以选择用于重复条目组的其他默认值。系统会自动显示可用的默认代码列表条目,并按照它们在条目组中出现的顺序进行显示。设计者可以从选定的条目中选择所有值,也可以选择特定值作为默认值进行显示。
设计者还可以手动配置重复条目组,方法一是让系统自动生成组,然后调整生成的组,方法二是手动添加组。设计者可以设计不限数量的默认值。但是,为了确保对于研究中心用户的可用性,每个表单的条目总数限制为 750 个条目。“条目总数”是指重复条目组行数和列数的乘积加上非重复条目组中的其他条目。
在此功能中,form_total_items 检查已从研究等级中移除,现在将包含在工作室病例手册验证中。
启用和配置
此功能对新研究自动可用。
了解详情
研究语言
用例
通过“研究语言(Study Language)”,研究设计者指定开展研究的基本语言和区域设置。此设置可确保所有系统标签、筛选器、按钮和数据都采用指定的语言,而不是 Vault 语言或用户语言。对于申办方要求研究中心以研究语言查看和输入数据的全球研究,以及需要以不同于 Vault 语言的语言开展的研究,“研究语言”增强了这些研究的开展方式。
说明
添加了以下新的工作室研究设置:强制使用研究语言(Enforce Study Language)、研究语言和研究区域设置(Study Locale),供研究设计者在配置研究设置时使用。用户将在研究设计规范(SDS)中以及从工作室中运行病例手册比较(差异报告)时看到所选的研究语言。
当强制使用研究语言设置设为“是(Yes)”时,输入、查看和保存的数据将以选定的研究语言和区域设置显示。以下区域将以研究语言显示:
- 研究中心列表页面、病例手册列表页面、任务栏、签名页面中的标签、按钮和筛选器
- 表单、事件、编码列表等的研究相关标签。
- 日期格式和日期选择器
- 更改原因
- 审计显示
- 审查活动:系统质疑和质疑对话框、方案偏离、评估、附加审查
- 列表和导出
- 快照
- “作业计划”页面
- 详细 PDF 和收尾 PDF
用户将负责以他们选定的研究语言上传动态消息的翻译。如果翻译不可用,则将默认使用 Vault 语言。
应用程序设置(不属于研究设置的区域,如选项卡名称、搜索栏等)仍将使用作为用户帐户一部分指定的用户语言。
当强制使用研究语言设置设为“否(No)”时,Vault 语言和用户语言仍可用于研究中心或用户需要以 Vault 语言开展的任何研究,且用户仍然可以使用翻译。
启用和配置
自动可用。现有研究的“强制使用研究语言”设置为“否”,“研究语言”和“区域设置”设置为 Vault 语言和区域设置
导入代码列表
用例
此更新提升了 Study Builder 在创建代码列表时的效率。
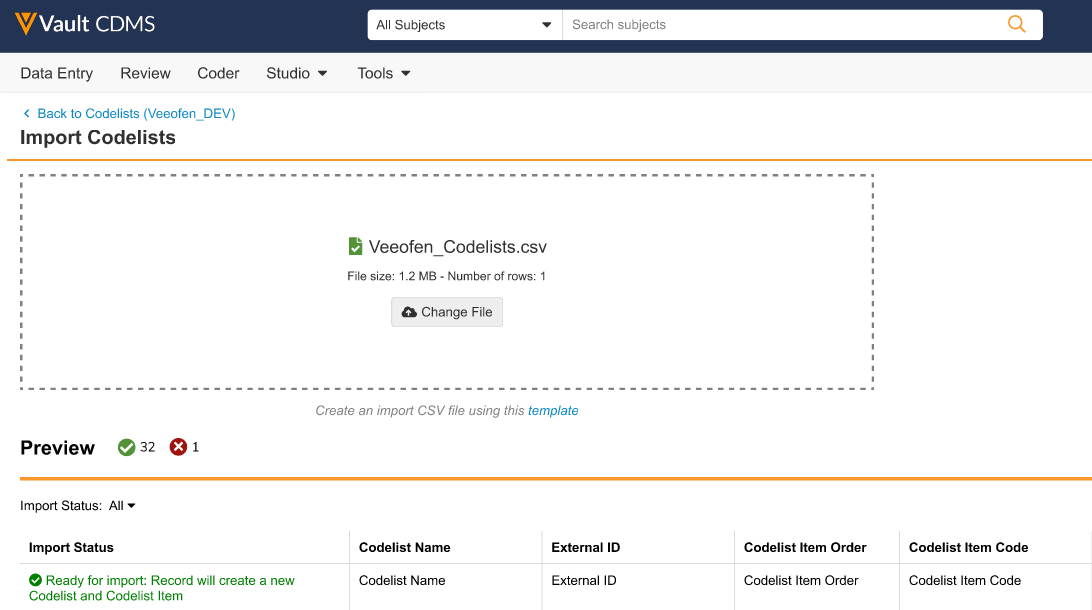
说明
借助此功能,Study Builder 可以通过导入 CSV 文件来创建代码列表。此功能旨在补充而非替代手动创建代码列表的方式。
填写好 CDMS 帮助中提供的模板后,用户可以通过拖放界面导入文件,并预览结果。导入时,系统会验证文件的完整性,确保它包含正确的列和必填值,强制符合字符限制、唯一性并填写必填字段。为了辅助更正,会显示错误和警告。
与此功能关联的导入工具支持每个代码列表最多导入 2,000 个条目。
启用和配置
对于任何具有设计研究权限的用户,包括标准 CDMS Super User(CDMS 超级用户)、CDMS API Read Write(CDMS API 读写)和 CDMS Study Designer(CDMS 研究设计者)角色,此更新立即可用。
了解详情
设置派生规则处理方式更新
用例
以前,对于由多个派生结果指向同一派生条目引起的问题,Vault 没有相应的清理机制来加以修复。为了解决此类规则冲突,更新了“设置派生值”规则的处理方式。导致派生结果冲突的可能原因包括规则配置更改、规则范围更改、停用和替换“设置派生值”规则,或多个“设置派生值”规则尝试为同一条目派生值。
说明
设置派生值规则的存储和处理方式已更新,确保派生值根据正确的规则准确显示在 EDC 中。在确定哪个结果将为派生条目设置值时,Vault 现在会考虑规则状态和范围。有关更多信息,请参阅以下示例。
示例:为一条设置派生值规则配置了一个完全限定的操作(即 $eg.ev.f.ig.item)。此规则被执行并按预期为目标条目设置派生结果。接下来,对同一条规则进行更新,使得原本是完全限定的标识符现在变为了 @Form.ig.item(其中 item group.item 与最初使用的样子相同)。对同一病例手册再次执行规则。在此功能发布之前,新规则不会覆盖旧规则设置的值。此增强功能发布后,新规则会正确更新条目的值。
启用和配置
自动启用。
实验室标题条目更新
用例
对 LBDTC 和 LBSEX 条目的小改进提供了更好的条目属性默认值。
说明
为研究启用“本地实验室(Local Labs)”时,系统为“性别”(LBSEX)生成的条目默认长度为 6,以匹配“性别”代码列表中最长的代码值。系统为“实验室收集日期和时间”(LBDTC)生成的条目在属性面板中包含了“无未来日期(No Future Date)”编辑检查。
启用和配置
当“启用本地实验室(Enable Local Labs)”设置更新为“是”时,对于新研究或现有研究自动可用。可以为现有研究进行这些更改并部署更新。
针对包含链接标识符的规则的验证
用例
为了辅助研究设计者并帮助防止规则不准确的情况,添加了病例手册验证警告,用于检查用户定义的规则中使用的链接标识符。
说明
当现有规则包含一个链接标识符且后跟一个序列号(例如 @Form/CM[2].ig_CM.CMINDC)时,将在工作室的病例手册验证报告中显示警告。Vault 不支持对重复的链接对象进行排序。当使用不受支持的链接标识符修改规则或创建新规则时,规则编辑器将显示“无效的序列号(Invalid Sequence Number)”错误,并且将阻止规则进行保存。
启用和配置
此增强功能自动可用。
工作室搜索的严格匹配更新
说明
CDMS 中进行了一些细微的架构调整,以使工作室中的搜索功能与 Vault Platform 的搜索功能保持一致。
启用和配置
此更新将自动应用。
研究管理
本部分中的功能适用于系统工具(System Tools)或 EDC 工具(EDC Tools),即 Veeva EDC 的研究级管理区域。
用户区域设置不受用户语言限制
用例
以前,Vault 不允许特定的语言使用某些区域设置。取消对语言和区域设置组合的限制可加强用户管理支持。
说明
CDMS 用户管理中的语言和区域设置现在彼此分离,便于用户管理员选择或导入每个用户所需的语言和区域设置组合。请参考 Vault Platform 发行说明了解其他详细信息。
启用和配置
此功能自动可用。
VeevaID SSO 选项的电子签名
用例
一些申办方或 CRO 更倾向于让其研究中心用户使用自己的 SSO/SAML 配置文件通过 SSO 和电子签名进行身份验证。
说明
对于转换为使用 VeevaID 的 CDMS Vault,具有 VeevaID 安全策略的研究中心用户可以使用 VeevaID 或者申办方或 CRO 的本地化单点登录(SSO)对病例手册数据进行电子签名。根据 VeevaID 的配置方式以及用于登录 Vault 的帐户,研究中心用户将使用 VeevaID 或 SSO 进行身份验证。
启用和配置
对于转换为使用 VeevaID 并在域上配置了 SSO 的 Vault 自动可用。
许可证密钥
用例
此功能有助于减少在部署过程中遇到的问题,并从许可证密钥而非研究名称来跟踪该研究是否符合投入生产的条件。
说明
所有非 ELA(企业许可协议)客户的研究现在都需要许可证密钥,该密钥可输入到 EDC 工具中的一个新字段。设置许可证密钥(Set License Key)和计费状态(Billing Status)选项均已添加到“研究主程序(Study Master)”网格中的更多选项(More Options)菜单。只有在客户为每项研究支付 EDC/CDB 费用的 Vault 中才能看到新的菜单选项。
在将研究部署到生产环境之前,必须将销售订单表单中的相应研究许可证密钥输入到 EDC 工具中的 DEV Vault。如果输入的许可证密钥与 Vault 中存储的密钥相匹配,则相应研究将被视为已获许可。在部署到生产环境之前,在工作室中运行验证时,用户将看到缺少许可证密钥的警告。
只有使用 CDB 的研究需要 CDB 许可证密钥,EDC 研究部署不会受影响。对于使用 CDB 的研究,在 CDB 中查看研究数据需要 CDB 许可证密钥。
对于具有完整 ELA 的客户(EDC 和 CDB),所有 EDC 和 CDB 研究均被视为已获许可,不需要许可证密钥。
启用和配置
自动可用。具有管理部署权限的用户可以设置许可证密钥。在生产环境中具有管理研究里程碑权限的用户可以设置计费状态。现有研究将自动迁移至新模型,对研究活动无任何影响。
了解详情
提取:更新受试者研究进展报告
用例
这一新报告更新了用于将事件日期加入到报告中的方法。
说明
此版本引入了新版的标准模板:受试者研究进展(V4) 报告。这一新版本更新了报告类型,以便从事件对象而非事件操作摘要对象填充事件日期。只有 Vault 所有者可查看标准模板:受试者研究进度(V4),但其可以与其他用户和角色共享。
25R1 版本发布后,事件操作摘要对象的事件日期字段不应再用于报告中。所有使用该字段的报告都应更新为从事件对象中提取事件日期。
一旦与用户共享新版本,我们建议 Vault 所有者或报告管理员取消共享以前的 V3 标准报告。
启用和配置
对于 Vault 所有者,此报告将立即可用,直到其与其他用户共享为止。
了解详情
FTP 连接增强功能
用例
FTP 配置报告已更新,现在包含有关研究的更多信息,提高了显示研究信息时的一致性。
说明
我们在 FTP 配置报告中添加了新的研究标签(Study Label)列。
启用和配置
此增强功能在版本发布时自动可用。
作业管理更新:输出文件访问权限
用例
此更新为 EDC 工具作业管理实现了更加一致的用户体验。
说明
在作业管理基础设施的改进过程中,我们更新了作业文件访问权限。包含在作业完成通知电子邮件中的作业文件链接现在指向特定于 EDC 的链接。此外,所有作业文件链接都将在作业运行 60 天后过期。
启用和配置
这些更新自动可用。
管理员:批量签名启用更改
用例
以前,启用了批量签名的 Vault 还需要在 EDC 工具中为特定研究和研究中心配置批量签名。对于新研究,EDC 工具中的该设置默认为“是”,节省了时间和精力,因为用户不再需要为每项新研究确认该设置。
说明
对于新研究和研究中心,EDC 工具中的启用批量病例手册签名(Enable Bulk Casebook Signature)设置将自动设为“是”。
启用和配置
在启用了批量签名的 Vault 中自动可用。对于新研究和研究中心,该设置将默认为“是(Yes)”。对于现有研究,该功能可在 EDC 工具中启用。
受试者移动时标记来源研究中心
用例
在受试者已移至其他研究中心的情况下,这些更新有助于为 CTMS 中的研究中心付款提供更好的支持。
说明
我们对受试者转移/受试者移动流程进行了以下更新:
- 转移受试者(Transfer Subject)的菜单项和按钮标签已更新为移动受试者(Move Subject)。
- 当选择移动受试者时,用户将需要提供移动原因(Reason for Move)
- 选择“受试者位于错误的研究中心(Subject is in the wrong site)”将触发以下操作:
- 将受试者的数据从原始研究中心中移除
- 将受试者和数据移动到新研究中心
- 数据不会继续引用原始研究中心
- 选择“受试者更换了研究中心(Subject changed sites)”将触发以下操作:
- 将受试者的数据从原始研究中心中移除
- 将受试者和数据移动到新研究中心
- 在现有事件、方案偏离和程序上继续引用来源研究中心。
- 在这两种情况下(“受试者位于错误的研究中心”或“受试者更换了研究中心”),用户都将收到确认窗口,需要额外步骤才能完成该操作。
此功能发布后,我们将不再支持在生产环境中通过单个操作移动多个受试者。
启用和配置
此增强功能在常规版本中自动可用。
在审计跟踪导出中显示已删除的查询
用例
数据审查者现在可以了解,在查询被删除之前打开了哪些查询以及对哪些查询进行了操作。
说明
在 25R1 版本之后删除的查询现在会显示在“审计跟踪导出”作业输出中。在此版本之前,只有 Vault 管理员可以查看已删除查询的审计历史记录。有两种情况可以删除查询,一是表单或事件被重置或标记为删除时,二是编码请求随逐字术语值的删除而删除时。
启用和配置
这些更新自动可用。
了解详情
导出作业历史记录
用例
以前,如要获取作业创建列表,用户需联系支持人员。现在,用户可以直接从 EDC 工具中的“作业历史记录(Job History)”区域获取作业创建列表,以获取作业历史记录。
说明
我们在“作业历史记录”网格的右上角添加了一个齿轮图标,供用户以 CSV 或 Excel 格式下载作业历史记录。选择格式后,系统将生成导出文件。用户会收到一封电子邮件通知,上面有一个链接供其在相关应用程序中检索文件。如果用户已自行注销或因长时间无活动而被注销,在检索文件之前,系统将提示他们输入其凭据。示例文件名:$Study_Job Export_$DateTime.xlsx,其中 DateTime 将以用户的时区显示。
文件中将包含以下列,顺序如下:
- 研究
- 作业 ID
- 作业类型
- 作业状态
- 创建者
- 作业详细信息
- 创建日期
启用和配置
此增强功能在版本发布时自动可用。
角色管理与安全
本节中的功能是对系统工具 > 角色管理(Role Management)和系统工具 > 用户(Users)区域的增强,以及对 Veeva Clinical Data 中的标准研究角色(Study Roles)、安全性和访问控制的更改。
支持重复的 PI 人名
用例
多个主要研究者(PI)可以同名。对于不同 PI 姓名相同的情况,“人员(Person)”记录现在支持 PI 重名。
说明
已取消 PI 姓名必须唯一的限制。现在允许 PI 重名,以支持创建姓名相同的两个不同 PI。PI 用户的姓名和电子邮件组合现在被视为 PI 用户记录的唯一标识。在“用户管理(User Administration)”或“EDC 工具”>“研究中心(Sites)”中添加新 PI 时,不会再遇到错误。在 UI 中,PI 的姓名格式已更新为“名字(电子邮件)”。
启用和配置
此增强功能自动可用。
CDMS CDB 程序员标准研究角色
用例
CDMS CDB 程序员角色适用于在 CDB 中工作但不是数据管理员的程序员,主要在 TST 环境中负责创建和部署公开列表、视图和检查。
说明
此版本提供了新的标准角色:CDMS CDB 程序员。
CDB 程序员角色适用于工作台中的生产和测试环境。单独用于生产环境时,该角色无法修改公开列表、检查或视图,但可以使用私密列表测试生产数据。这有助于提高生产环境中的控制力度,并避免意外更新已部署的列表。
在 TST 环境中工作时,我们建议为用户提供 CDMS CDB 程序员研究角色的同时为其提供 CDMS Lead Data Manager(CDMS 首席数据管理员)或 CDMS Data Manager(CDMS 数据管理员)研究角色,具体取决于用户是否需要访问受限数据。附加的角色可以为用户提供公共访问权限,以便他们将其工作保存为公开列表。他们还可以设置计划导出、管理第三方数据的键位映射以及访问 CDB 工具。
启用和配置
此角色一发布即可分配给用户。
连接与集成
本节中的功能是与 Veeva Clinical Data 的新连接或集成,或对现有连接或集成的增强。
临床操作 - EDC 连接:事件操作摘要记录增强功能
用例
“临床操作 - EDC 连接”支持将用于显示 SDV 和 DMR 完成情况的 EDC 事件操作摘要传输到 CTMS 受试者访视记录。在 25R1 之前,SDV 和 DMR 汇总由该连接分开计算。从 25R1 开始,根据 EDC 中的在事件列表、提取和报告中包含日志事件功能,这些数据将直接从 EDC 中的事件操作摘要记录中检索,包括日志事件的数据。
说明
通过“临床操作 - EDC 连接”传输的事件数据现在可以直接从 EDC 的事件操作摘要对象中检索。CTMS 中的现有行为保持不变。实施此增强功能后,用户可能会注意到性能得到改进。
启用和配置
对于使用临床操作-EDC 连接的研究,此功能会自动启用。
了解详情
Safety-EDC 连接:每个研究多个“安全病例启动事件”表单
用例
不良事件(AE)在 EDC 中具有多个表单设计是一个常见概念,考虑到了请求的安全相关 EDC 数据存在各种变化,例如,因研究药物而变化。在此版本之前,要启动从 EDC 到 Vault Safety 的安全病例转移,只能配置一个表单。这就需要设计一个综合的 AE 表单才能涵盖所有可能的情况。
在此版本中,用户可以针对每项研究将多个表单映射到安全病例启动事件表单类型(以前标记为严重不良事件),以启动向 Vault Safety 的数据传输。通过配置多个 EDC 表单来启动安全病例的发送,研究和库中的 AE 表单设计将具有更高的灵活性。
此功能的另一个关键用例是试验参与者意外妊娠。使用此功能,收集妊娠信息的表单可以映射为安全病例启动事件,用于在报告意外妊娠时启动安全病例。
说明
在“工作室(Studio)”>“安全集成(Safety Integration)”>“表单配置(Form Configuration)”中,用户现在可以使用安全病例启动事件表单类型创建多个表单配置。请注意,针对每个研究,用户仍然只能将一个 EDC 表单映射到一个类型表单,例如,一旦实验室检测表单映射到某个表单配置,便无法映射到另一个表单配置。
为了考虑安全病例启动事件的可选性,我们为下列安全类型表单添加了一个“Inclusion Criteria(纳入标准)”部分。通过这些新选择,可以进行相应配置,以便在任意一个或只有选定的安全病例启动事件启动向安全系统的数据传输时,将相应表单包含在安全病例中。
- 伴随用药
- 药物史
- 病史
- 研究药物
- 测试结果
默认配置:这些将默认为任意(Any)。在该附加配置保持不变的情况下,不会导致对现有安全病例进行后续发送。
为了支持此功能,我们已将严重不良事件表单类型重新标记为安全病例启动事件。请参阅安全集成:更新的安全表单类型标签功能,以了解详细信息。
启用和配置
对于使用安全-EDC 连接的研究,此功能会自动启用。实时研究的配置可能会导致对现有安全病例发送后续安全消息。
了解详情
Safety-EDC 连接:妊娠信息
用例
妊娠信息在报告不良事件时可能至关重要,但其本身也可能需要启动从 EDC 到 Safety 的数据传输。通过 Safety-EDC 连接,Vault 现在可以将安全相关的妊娠信息与严重不良事件一起传输,也可以作为独立信息传输。
说明
在“工作室”>“安全集成”>“表单配置”中,以下与妊娠相关的选项可用于在安全病例启动事件(以前称为不良事件)表单类型上进行映射:
- 妊娠病例(Pregnancy Case)(AE_PREG_CASE)
- 妊娠事件(Pregnancy Occurrences)(AE_PREG_INFO_GRAV)
- 分娩次数(Number Given Birth)(AE_PREG_INFO_PARA)
- 研究药物暴露时怀孕(Pregnant at Study Drug Exposure)(AE_PREG_INFO_AT_VX)
- 末次月经日期(妊娠病例)(Last Menstrual Date (Pregnancy Case))(AE_PREG_LAST_MENSTRUAL_DATE)
- 怀孕日期(Pregnancy Conception Date)(AE_PREG_INFO_CONC_DT)
- 预产期(Pregnancy Due Date)(AE_PREG_INFO_DUE_DT)
- 怀孕结局日期(Date of Pregnancy Outcome)(AE_PREG_INFO_OUTCOME_DT)
- 怀孕结局(Pregnancy Outcome)(AE_PREG_INFO_OUTCOME)
- 分娩方式(Delivery Method)(AE_PREG_INFO_DELV_METH)
启用和配置
对于使用安全-EDC 连接的研究,此功能会自动启用。实时研究的配置可能会导致对现有安全病例发送后续安全消息。
了解详情
安全病例(V4)和安全消息 - E2B(V4)报告
用例
我们添加了安全病例(V4) 报告,以反映 E2BLink 和 Safety-EDC 连接的最新增强功能。这些更新还解决了针对不同研究语言的要求。
我们还添加了包含操作详细信息的安全消息 - E2B(V4) 报告,从而改进了对特定于 E2BLink 的消息交换的跟踪。
说明
除了安全病例(V3) 报告中的所有列以外,新的安全病例(V4) 报告还包括以下新列:
- 表单序列
- 病例中的事件
- 报告中最近信息的日期
- 上次发送到安全系统的消息
- 上次发送文件名
- 最后一个 ACK 文件名
- 报告者名字(Reporter First Name)
- 报告者姓氏(Reporter Last Name)
- Vault 安全病例
- 需要进行跟进检查
- 其他跟进待处理
我们建议 Vault 所有者停止共享标准模板:安全病例(V3) 报告,然后改为与这些用户共享安全病例(V4) 标准报告。
除了安全消息报告中的所有列以外,新的安全消息 - E2B(V4) 报告包括还以下特定于 E2BLink 的操作列:
- 研究
- Study Country(研究国家/地区)
- 研究中心
- 受试者
- 发送文件名
- Ack 文件名
- MDN 接收日期
- ACK 接收日期
- 其他 ACK 接收日期
- ACK 错误/详细信息
- 其他 ACK 错误/详细信息
启用和配置
对于 Vault 所有者,这些报告将立即可用于与其他用户共享。
安全集成:更新的安全表单类型标签
用例
我们重新标记了安全表单类型标签和 SDE 列标题,以更好地反映新的安全病例启动的灵活性,并提高安全相关 EDC 数据的精度。
说明
此版本为使用 E2BLink 或 Safety-EDC 连接的研究更新了标签:
- 严重不良事件更新为安全病例启动事件
- 外部实验室到更新为测试结果
- 合并用药更新为合并用药
这些标签更改适用于整个安全相关 EDC 功能。
在研究数据提取(SDE)中,SYS_SAFC 数据集列主要 SAE 的表单序列(Form Sequence of Primary SAE)已重新标记为主要事件的表单序列(Form Sequence of Primary Event)。只有在使用 SDE 25R1 版本时,此更改才适用。请注意,这是使用 SDE 25R1 版本时与 SDE 24R3 版本相比的唯一更改。
启用和配置
此功能自动启用。
EDC API
EDC API 的新功能如下。请参阅我们的开发者门户的发行说明,了解更详细的功能信息。
EDC API 功能
该版本为 EDC 开发者提供了以下功能:
- 复制表单定义
- 病例手册设计导出(CDE)增强功能
临床数据库(CDB)
Veeva CDB 应用程序的新功能如下。
可用性:临床数据库(CDB)仅对 CDB 许可证持有者提供。请联系 Veeva 服务代表了解详细信息。
CDB 对方案偏离的支持
用例
在 EDC 中创建的方案偏离(PD)可以在工作台中查看,并包含在临床报告或工作台的 CDB 导出中。
说明
为了在 CDB 工作台中完全支持方案偏离,我们的第一步以系统列表(Sys_PD)和新的 CQL 属性的形式提供数据。用户可以将系统列表作为自定义列表进行保存,并包含在导出中。在此版本发布后创建的原始类型导出定义将自动包含 Sys_PD 列表,用户只需修改现有导出即可包含此列表。
通过新的 CQL 语法,用户可以创建可排序、筛选和导出的自定义 PD 列表。与 @QRY 类似,@PD 表示法提供对 PD 属性的访问权限以及对相关表单和条目的引用(如果适用)。
启用和配置
在此版本发布后,EDC 方案偏离数据将在研究数据完全提取后可用。
观察
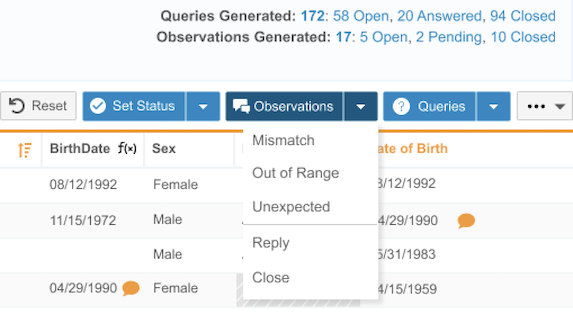
用例
借助观察功能,数据管理员可以通过一种新方法,针对不匹配、超出范围或意外的数据在 CDB 工作台中保存有关数据条目的备注。这有助于多个团队在工作台中进行协作,便于他们查看随时间变化的值并记录发现,而不会在值发生更改时丢失备注,完全无需编写发送给研究中心的查询。
说明
观察结果可以在数据条目所在的任何列表中进行查看,即使数据值发生更改也会一直保留。用户可以在任何数据列表中查看、创建、回复和关闭观察结果。所有观察结果和观察消息都可以包含在提取中。
启用和配置
标准 CDMS Lead Data Manager(CDMS 首席数据管理员)、CDMS Data Manager(CDMS 数据管理员)和 CDMS Super User(CDMS 超级用户)角色具有查看、创建、回复和关闭观察结果的权限。
了解详情
查询指标
用例
我们在新的“质疑指标(Query Metrics)”页面上引入了图表,以帮助深入了解为某项研究生成质疑的方式,并回答以下问题:
- 自动生成或手动创建的质疑是否会导致数据更改?
- 被重新质疑的质疑百分比是多少,由哪些团队发起,或者这些质疑的编写是否能有效避免花时间进行讨论?
- 哪些研究中心在根据质疑时效或响应数量处理已关闭的质疑时遇到问题?
说明
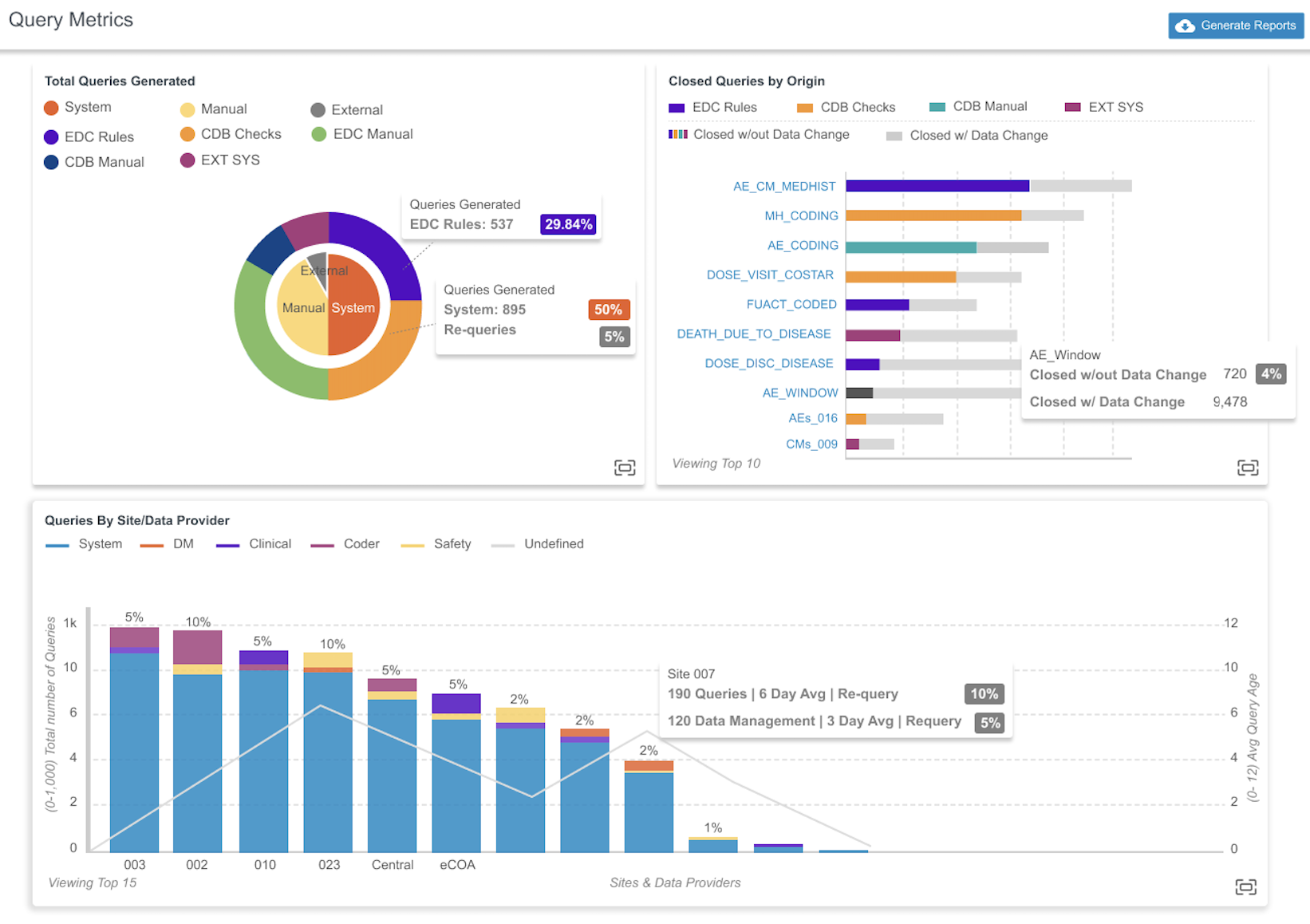
此版本提供了三(3)个图表:生成的总查询(Total Queries Generated)、按来源划分的已关闭查询(Closed Queries by Origin)和按研究中心/数据提供者划分的查询(Queries By Site / Data Provider)。
“生成的总查询”图表分为两部分:
按类型(内圈)
- 由 CDMS 系统自动生成
- 由用户手动创建
- 通过 API 从外部源生成
按来源(外圈)
- EDC 规则
- EDC 手动
- CDB 检查
- CDB 手动
- 外部源
“按来源划分的已关闭查询”图表在水平条形图中显示了 10 个已关闭查询数量最多且没有发生数据更改的来源。
“按研究中心/数据提供者划分的查询”图表在条形图中显示了查询总数,并按来源进行颜色编码。条形图上叠加了一个折线图,显示平均查询时效。
启用和配置
具有在 CDB 工作台中查看所有 CDB 查询列表权限的用户可以查看“查询指标”图表。
了解详情
CQL 对新标题属性的支持
用例
在 24R3 版本中,我们为系统列表添加了新属性。在此版本中,我们更新了 CQL,以在自定义列表和列表生成器中支持这些新属性。
说明
为 CQL 添加的属性如下:
- Study.Label(
@HDR.Study.Label):返回研究的标签。 - EventGroup.ExternalID(
@HDR.EventGroup.ExternalID):返回事件组的外部 ID。 - Event.EventDateLastModifiedDate(
@HDR.Event.EventDateLastModifiedDate):返回事件中事件日期的上次修改日期。 - Event.WindowStatus(
@HDR.Event.WindowStatus):返回事件的窗口状态(提早、范围内或推迟) - Event.DaysOutsideWindow*(
@HDR.Event.DaysOutsideWindow):返回事件的窗口期之外的天数。这表示事件日期相对于计划的事件窗口超出范围(提早或推迟)的天数。 - Event.ExpectedForms*(
@HDR.Event.ExpectedForms):返回事件的预期表单数量。 - Event.FormEntryOverdue*(
@HDR.Event.FormEntryOverdue):返回 True 或 False,以指示事件中的任何表单是否处于逾期状态。 - Event.FrozenDate(
@HDR.Event.FrozenDate):返回事件最近一次被冻结的冻结日期。 - Event.LockedDate(
@HDR.Event.LockedDate):返回事件最近一次被锁定的锁定日期。 - Event.SignedDate(
@HDR.Event.SignatureDate)返回事件最近一次被签署的签署日期。
* 这些字段仅在启用系统列表中的计算字段功能时可用。
我们还使用以下属性更新了核心数据列表配置:
- Study.Label
- EventGroup.ExternalID
- Event.EventDateLastModifiedDate
- Event.WindowStatus
- Event.DaysOutsideWindow
- Event.ExpectedForms
- Event.FormEntryOverdue
- Event.FrozenDate
- Event.LockedDate
- Event.SignatureDate
启用和配置
这些属性将自动可用于包含在以 CQL 编写的自定义列表中或通过列表生成器包含在自定义列表中。核心列表默认值可以更新,以包含核心列表中的属性子集,并在列表生成器中作为默认选定项。
了解详情
对新标题属性的支持
用例
在 24R3 版本中,我们为系统列表添加了新属性。在此版本中,我们还在自定义列表和列表生成器中支持这些新属性。
说明
添加到列表生成器和临床报告的核心数据列表配置中的属性如下:
- Study.Label:返回研究的标签。
- EventGroup.ExternalID:返回事件组的外部 ID。
- Event.EventDateLastModifiedDate:返回事件中事件日期的上次修改日期。
- Event.WindowStatus:返回事件的窗口状态(提早、范围内或推迟)
- Event.DaysOutsideWindow*:返回事件的窗口期之外的天数。这表示事件日期相对于计划的事件窗口超出范围(提早或推迟)的天数。
- Event.ExpectedForms*:返回事件的预期表单数量。
- Event.FormEntryOverdue*:返回 True 或 False,以指示事件中的任何表单是否处于逾期状态。
- Event.FrozenDate:返回事件最近一次被冻结的冻结日期。
- Event.LockedDate:返回事件最近一次被锁定的锁定日期。
- Event.SignedDate:返回事件最近一次被签署的签署日期。
* 这些字段仅在启用系统列表中的计算字段功能时可用。
启用和配置
这些属性将自动可用于通过 EDC 临床报告中的列表生成器包含在自定义列表中。核心列表默认值可以更新,以包含核心列表中的属性子集,并在列表生成器中作为默认选定项。
了解详情
导出中的 CDB 审查备注
用例
此功能支持在导出中传输相关的审查信息。
说明
审查信息将随审查列表一起添加到导出定义中。以下新列将添加到导出中,包括现有的导出定义:
- 审查者
- 审查日期
- 审查状态
- 审查原因
列表数据的末尾已添加这些列。
启用和配置
这些增强功能在版本发布时自动可用。
对重复事件组标签的支持
用例
通过重复事件组,仅需为研究定义一次访视周期,且研究中心可以根据需要生成每个周期。在此版本中,CQL 和 CDB 支持在列表中显示在工作室中定义的覆盖标签。
说明
新的 CQL @HDR.EventGroup.RepeatLabel 可用于为工作台中的自定义列表包含事件组的覆盖标签。此属性将返回重复事件组和非重复事件组的标签。
重复标签将添加到 Sys_Forms、Sys_Events、Sys_ILB 和列表生成器。组织还可以选择将其包含在核心列表中,只需更新 CDB 的配置即可。
启用和配置
在此版本发布后,一旦完成首次完全提取,这些标签即可包含在列表中。
支持在清单中定义表单和条目标签以及条目名称
用例
在导入第三方数据源时,客户现在可以为条目或表单定义标签,以便在列表中通过 CQL 进行引用。此外,对于数据文件中提供的名称,客户可以使用条目名称覆盖功能为条目定义一个不同的名称。例如,假设 CSV 数据文件中定义的条目名称为“LPANEL”,要使导入到 CDB 后的条目名称为“LABPANEL”,可以用后者覆盖前者。
说明
第三方数据和 OpenEDC 数据的提取功能已更新,以便能够为条目名称设置一个已定义的覆盖值,这样系统将导入并显示清单中定义的名称,而非数据 CSV 文件中该列的标题行值。其他的增强功能还包括支持第三方数据源的表单和条目标签,现在可以在导入清单中定义这些源。
启用和配置
版本发布时,此功能将在 CDB 中自动可用。
CDB 和临床报告导出可用性增强功能
用例
我们对 CDB 工作台和临床报告导出的用户体验进行了改进。
说明
针对 CDB 和临床报告中的导出操作,此版本包括以下可用性增强功能:
- 无法再从导出 UI 编辑列表。用户可以改为通过 CQL 或列表生成器在列表本身中进行更改。
- 我们已将无(None)类型重命名为自定义(Custom)。
- SDTM 导出类型已弃用,无法用于新的导出定义。此更改对现有的 SDTM 类型导出无影响。
- 导出属性对话框的“传送(Delivery)”下拉列表中现在会显示 FTP 连接是在研究级别还是在 Vault 级别定义的。
- 问题日志的“列表(Listing)”列现在会列出列表的标题。
- 我们从问题日志中移除了“文件(File)”列。
- 我们加宽了问题日志中的“消息(Message)”列,以提高可读性。
启用和配置
这些增强功能在版本发布时自动可用。
CDB 对事件操作摘要的使用
用例
在 25R1 中,以前由 CDB 计算的 EDC 中的事件属性现在将从 EDC 操作摘要对象中提取。
说明
事件属性字段(例如,已冻结(Frozen)、已锁定和已签名)将从 EDC 事件操作摘要对象提供的数据中提取,而不是通过查看事件记录来计算。
启用和配置
在此版本发布后,一旦完成首次完全提取,此更新自动可用。
将查询来源添加到 CDB 查询列表中
用例
查询来源信息可标识以编程方式或通过 API 创建了添加到 EDC 或 CDB 的查询的系统和用户。此信息现在将包含在查询列表中,程序员也可通过 CQL 获取。
说明
有关查询来源的详细信息提供三(3)个字段:“系统(system)”、“用户(user)”和“ID”。这些字段将被添加到 CDB 中的核心查询列表。请注意,如果查询是在 EDC 或 CDB 中创建的,则来源用户字段将为空,只有包含在 API 请求中时才会填充。
CQL 已更新,支持使用 @QRY.OriginUser 将查询来源用户信息包含在列表中,以及使用 @QRYMSG.OriginSystem、@QRYMSG.OriginID 和 @QRYMSG.OriginUser 将所有三个查询消息字段包含在列表中。
启用和配置
核心查询列表将自动在列表中(包括在导出中)包含这些新列。导出时的更改检测功能会将这些更新识别为对导出定义的更改。
了解详情
将查询来源添加到临床报告查询列表中
用例
查询来源信息可标识创建了添加到 EDC 或临床报告的查询的系统和用户。现在,此信息将包含在查询列表中。
说明
有关查询来源的详细信息提供三(3)个字段:“系统(system)”、“用户(user)”和“ID”。这些字段将被添加到 CDB 中的核心查询列表。请注意,如果查询是在 EDC 或临床报告中创建的,则来源用户字段将为空。此字段只有包含在 API 请求中时才会填充。
启用和配置
核心查询列表将自动在列表中(包括在导出中)包含这些新列。导出时的更改检测功能会将这些更新识别为对导出定义的更改。
研究文件格式 API 增强功能
用例
通过将第三方数据添加到研究文件格式(SFF)API 提取中,所有 CDB 数据都可以通过 API 导出到下游系统。通过在增量 SFF 提取中引入受试者病例手册版本和医疗编码请求跟踪功能,减少了提取完整软件包的必要。
说明
提取到 CDB 工作台中的第三方数据现在将作为通过 SFF API 进行的完整每日提取的一部分包含在 CSV 文件夹中,并在清单文件中进行描述。
在增量 SFF 提取中,受试者病例手册版本和医疗编码请求跟踪功能已添加到导出中。
启用和配置
这些功能在版本发布后自动可用,并且需要使用 24.3 版的 API。
在核心列表原始导出中添加了访视方法
用例
我们在导出中添加了额外的事件信息。
说明
对于原始(Raw)导出类型,我们在核心列表中添加了 Event.VisitMethod。
启用和配置
这些新的列将自动可用。现有导出将显示更改通知,供用户选择是否接受对列表的更新。
SYS 列表中的计算字段
用例
为了更好地与从研究数据提取(SDE)中获取的数据保持一致,工作台和研究文件格式(SFF)提取中的某些 CDB 系统列表已更新。
说明
对于此版本,我们在以下调用函数、列表和 SFF 提取中添加了新列:
- Sys_Events:
- Event.WindowStatus
- Event.DaysOutsideWindow
- Sys_Forms:
- Form.SubmitToSDV
- Form.SubmitToDMR
- Form.SubmitToFrozen
- Form.SubmitToLocked
- Form.SubmitToSign
- Form.EventToSubmit
- 查询列表:
- Query.CausedDataChange
- Query.OpenToReply
我们还更新了 EDC 查询的查询时效(Query Age)计算方式,以使用上次关闭日期(Last Closed Date)字段。这与 Vault EDC 中的该计算方式保持一致。
启用和配置
要在 Vault 中启用此功能,请联系 Veeva 支持进行讨论。
CDB API
以下是 CDB API 的新功能。请参阅我们的开发者门户的发行说明,了解更详细的功能信息。
CDB API 功能
此版本包含对 CDB 开发者的第三方数据加载支持。
EDC 迁移器
本部分中的功能是针对 Veeva EDC 迁移器的新功能。
编码更新
用例
此更新有助于更清楚地了解医疗编码的迁移负载进度和状态。
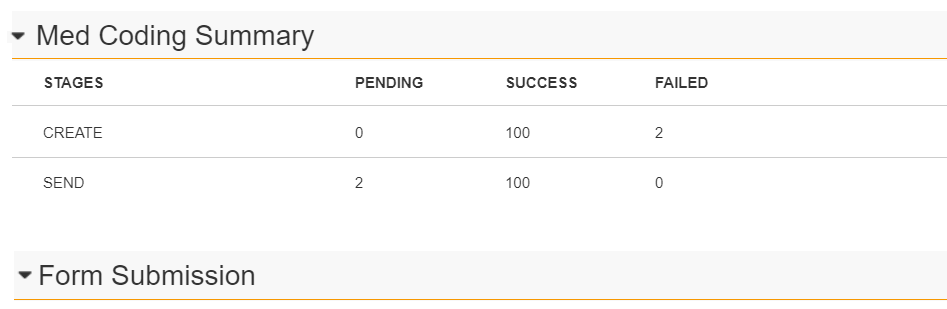
说明
我们修改了医疗编码摘要表,以将迁移过程的创建和发送阶段都显示出来。
创建阶段引用创建编码请求的时间点。发送阶段引用将迁移编码请求发送到 EDC 编码器的时间点。此阶段中的计数在创建阶段完全完成后立即填充。
启用和配置
这些更新将在常规版本中立即可用。
了解详情
对实验室数据的支持
用例
此功能支持向 CDMS 迁移研究中迁移实验室数据。
说明
现在,YAML 可用于将实验室标题数据映射到 Veeva 研究设计。迁移 Vault 将对这些映射的数据进行迁移。此外,如果实验室数据采用标准化(垂直)格式的结构,一条实验室结果为一行,也可以迁移到研究中。迁移后,系统将评估正常的实验室范围,并给超出范围的数据添加标记。
启用和配置
在迁移 Vault 中,此功能立即可用。
了解详情
YAML 生成器:Rave™ 插件支持
用例
此更新为 Rave 到 Veeva EDC 的研究迁移提供了支持。
说明
现在,迁移用户可以使用 YAML 生成器来为源自 Rave 的研究创建映射文件。
启用和配置
在迁移 Vault 中,此功能立即可用。
了解详情
YAML 生成器:Rave™ 对实验室数据迁移的支持
用例
此功能为 Rave 到 Veeva EDC 的研究迁移提供了完整的支持。
说明
迁移 Vault 现在可以自动对迁移自 Rave 的研究中的实验室数据进行 YAML 映射。YAML 生成器可以识别表单是否含有实验室数据,如果有,则相应地生成实验室 YAML 文件。
启用和配置
此功能自动可用。