标准 CDMS 报告模板
Veeva EDC 利用 Vault Platform 提供操作指标的报告功能。Veeva 提供标准的报告模板,可以通过复制并根据需要配置列和筛选器来创建报告。
如果从报告中打开了一个关联对象记录,Veeva EDC 会在 Veeva EDC 的相关区域打开该对象记录,而不是在对象记录的详细信息(Details)页面中。有关共享报告的信息,请参阅共享设置(Sharing Settings)。
可用性:与文档相关的报告功能在 Veeva EDC 中不可用。
Veeva 标准报告模板政策
标准报告模板展示了 Veeva EDC 如何显示操作指标。这些标准模板为客户在进行研究时可能需要的自定义报告提供了参考。所有用户的标准报告模板均为锁定状态。如果客户希望在研究执行中使用模板,必须创建该模板的副本。标准模板报告的版本在描述中可见。
标准报告模板不属于与 Veeva EDC 合同的一部分,并且可能会发生变化。因此,客户不应将其标准操作程序基于提供的模板。
标签和简短标签列:标签和简短标签列仅适用于填充 23R3 版本后创建的表单定义。对于已存在的表单定义,这些列将为空白。
可用模板
“事件操作摘要(Event Operational Summary)”对象的“事件日期(Event Date)”字段:25R1 版本发布后,事件操作摘要对象的事件日期字段不应再用于报告中。所有使用该字段的报告都应更新为从事件对象中提取事件日期。
以下是 Veeva EDC 中可用的标准报告模板:
| 模板 | 说明 | 报告类型 | 数据模型 V1 支持 | 数据模型 V2 支持 | 备注 |
|---|---|---|---|---|---|
| 研究中心效率 | |||||
| 标准模板:病例手册签名汇总 | 已签名的病例手册汇总 | 研究中心病例手册操作汇总 | 否(No) | 是(Yes) | 20R2 中的新增功能,适用于数据模型 V2 研究。 |
| 标准模板:病例手册签名汇总(V3) | 根据病例手册的签名状态生成的汇总矩阵报告。可能的值包括 Yes(表示病例手册已完全签名)和 No(表示病例手册未签名)。 | 研究中心病例手册操作汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:冻结病例手册汇总 | 冻结病例手册汇总 | 研究中心病例手册操作汇总 | 否(No) | 是(Yes) | 20R2 中的新增功能,适用于数据模型 V2 研究。 |
| 标准模板:冻结病例手册汇总(V3) | 根据病例手册的冻结状态生成的汇总矩阵报告。可能的值包括 Yes(表示病例手册已完全冻结)和 No(表示病例手册未冻结)。 | 研究中心病例手册操作汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:已锁定病例手册汇总 | 已锁定病例手册汇总 | 研究中心病例手册操作汇总 | 否(No) | 是(Yes) | 20R2 中的新增功能,适用于数据模型 V2 研究。 |
| 标准模板:已锁定病例手册汇总(V3) | 根据病例手册的锁定状态生成的汇总矩阵报告。可能的值包括 Yes(表示病例手册已完全锁定)和 No(表示病例手册未锁定)。 | 研究中心病例手册操作汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:事件状态 | 按照状态和研究中心汇总的总事件数。 | 模板:事件以及事件定义、研究、研究中心和受试者 | 是(Yes) | 否(No) | 对于数据模型 V2 研究:从事件操作汇总对象使用事件状态字段,而不是事件对象。 |
| 标准模板:事件状态(V3) | 按研究筛选的矩阵报告,提供按研究中心和状态分类的事件数量汇总。 | 模板:事件以及事件操作汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:事件签名汇总 | 已签名的事件汇总 | 模板:事件以及事件定义、研究、研究中心和受试者 | 否(No) | 是(Yes) | 20R2 中的新增功能,适用于数据模型 V2 研究。 |
| 标准模板:事件签名汇总(V3) | 对已提交事件的签名状态进行统计的汇总矩阵报告。可能的值包括:Yes 表示事件已签名,No 表示事件曾签名但已取消签名,None 表示事件从未签名。 | 事件以及研究中心和事件操作汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:表单周期时间汇总 | 表单周期时间指标汇总 | 模板:表单周期时间汇总 | 是(Yes) | 是(Yes) | |
| 标准模板:表单周期时间汇总(V3) | 按研究中心划分的表格式报告。周期时间包括:从访视到表单提交、表单提交到 SDV、DMR、签名、冻结和锁定 | 模板:表单周期时间汇总 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:表单 SDV 汇总 | 已验证源数据的表单汇总 | 模板:研究中心与表单 | 是(Yes) | 否(No) | 数据模型 V2 研究应使用此报告的 V2 版本。 |
| 标准模板:每周表单 SDV 监查活动 | 按研究中心汇总的每周表单 SDV 监查活动 | 模板:包含事件、研究中心和受试者的表单 | 是(Yes) | 否(No) | 数据模型 V2 研究应使用此报告的 V2 版本。 |
| 标准模板:表单签名汇总 | 已签名表单汇总 | 模板:研究中心与表单 | 是(Yes) | 否(No) | 数据模型 V2 研究应使用此报告的 V2 版本。 |
| 标准模板:表单签名汇总(v2) | 已签名表单汇总 | 模板:研究中心与表单 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用标准模板:表单签名汇总 |
| 标准模板:表单签名汇总(V3) | 对已提交表单的签名状态进行统计的汇总矩阵报告。可能的值包括:Yes 表示表单已签名,No 表示表单曾签名但已取消签名,None 表示表单从未签名。 | 表单以及研究中心和汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。 |
| 标准模板:表单状态 | 研究中心级别的表单状态汇总报告 | 模板:包含事件、研究中心和受试者的表单 | 是(Yes) | 是(Yes) | |
| 标准模板:表单状态(V3) | 所有表单状态的汇总矩阵报告,按研究中心和受试者分类。 | 模板:包含事件、研究中心和受试者的表单 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:冻结表单汇总 | 冻结表单汇总 | 模板:研究中心与表单 | 是(Yes) | 否(No) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:冻结表单汇总) |
| 标准模板:冻结表单汇总(v2) | 冻结表单汇总 | 模板:研究中心与表单 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本。 |
| 标准模板:冻结表单汇总(V3) | 对已提交表单的冻结状态进行统计的汇总矩阵报告。可能的值包括:Yes 表示表单已冻结,No 表示表单曾冻结但已取消冻结,None 表示表单从未冻结。 | 表单以及研究中心和汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:冻结事件汇总 | 冻结事件汇总 | 模板:事件以及事件定义、研究、研究中心和受试者 | 是(Yes) | 否(No) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:冻结事件汇总) |
| 标准模板:冻结事件汇总(v2) | 冻结事件汇总 | 模板:事件以及事件定义、研究、研究中心和受试者 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本。 |
| 标准模板:冻结事件汇总(V3) | 对已提交事件的冻结状态进行统计的汇总矩阵报告。可能的值包括:Yes 表示事件已冻结,No 表示事件曾冻结但已取消冻结,None 表示事件从未冻结。 | 事件以及研究中心和事件操作汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。数据模型 V1 研究应使用此报告的 V1 版本。 |
| 标准模板:已锁定表单汇总 | 已锁定表单汇总 | 模板:研究中心与表单 | 是(Yes) | 否(No) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:已锁定表单汇总) |
| 标准模板:已锁定表单汇总(v2) | 已锁定表单汇总 | 模板:研究中心与表单 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本。 |
| 标准模板:已锁定表单汇总(V3) | 对已提交表单的锁定状态进行统计的汇总矩阵报告。可能的值包括:Yes 表示表单已锁定,No 表示表单曾锁定但已取消锁定,None 表示表单从未锁定。 | 表单以及研究中心和汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。数据模型 V1 研究应使用此报告的 V1 版本。 |
| 标准模板:已锁定事件汇总 | 已锁定事件汇总 | 模板:事件以及事件定义、研究、研究中心和受试者 | 是(Yes) | 否(No) | 数据模型 V2 研究应使用此报告的 V2 版本。 |
| 标准模板:已锁定事件汇总(v2) | 已锁定事件汇总 | 模板:事件以及事件定义、研究、研究中心和受试者 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:已锁定事件汇总) |
| 标准模板:已锁定事件汇总(V3) | 对已提交事件的锁定状态进行统计的汇总矩阵报告。可能的值包括:Yes 表示事件已锁定,No 表示事件曾锁定但已取消锁定,None 表示事件从未锁定。 | 事件以及研究中心和事件操作汇总 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。数据模型 V1 研究应使用此报告的 V1 版本。 |
| 标准模板:各个研究中心的质疑时效 | 按研究中心和质疑时效(<1 天、1-3 天、3-5 天、5-7 天、>7 天)的质疑数量汇总 | 模板:质疑周期时间汇总 | 是(Yes) | 是(Yes) | |
| 标准模板:各个研究中心的质疑时效情况(V3) | 按质疑时效分组(1 周、2 周、3 周、4 周、>4 周以上)未解决和已回答质疑数量的汇总矩阵报告,按研究中心分组。 | 模板:质疑周期时间汇总 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:质疑周期时间汇总 | 质疑周期时间指标汇总,用于评估研究中心的响应能力和数据冲突解决情况 | 模板:质疑周期时间汇总 | 是(Yes) | 是(Yes) | |
| 标准模板:质疑周期时间汇总(V3) | 研究中所有质疑的表格式报告。周期时间包括质疑时效、首次响应时间以及从未解决到已解决的时间。 | 模板:质疑周期时间汇总 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:每个表单的质疑量 | 研究中针对特定表单设计(表单定义)执行的质疑次数 | 模板:带有表单定义和质疑绑定的表单 | 是(Yes) | 是(Yes) | |
| 标准模板:每个表单的质疑量(V3) | 按表单定义的质疑次数汇总的矩阵报告。 | 模板:带有表单定义和质疑绑定的表单 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:各个研究中心的每周质疑量 | 每周在研究中生成的质疑数量,按研究中心分组 | 模板:带有质疑绑定的研究中心 | 是(Yes) | 是(Yes) | |
| 标准模板:各个研究中心的每周质疑量(V3) | 每周创建质疑数量的汇总矩阵报告,按研究中心分组。 | 模板:带有质疑绑定的研究中心 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:研究中心质疑 | 研究中,按每个研究中心的质疑状态汇总质疑数量的报告 | 模板:带有质疑绑定的研究中心 | 是(Yes) | 是(Yes) | |
| 标准模板:研究中心质疑(V3) | 按质疑状态和研究中心分组的质疑数量的汇总矩阵报告。 | 模板:与研究中心关联的质疑绑定 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:每周累积受试者创建数量 | 每个研究中心在 EDC 系统中的累积受试者创建数量 | 模板:受试者 | 是(Yes) | 是(Yes) | |
| 标准模板:每周累积受试者创建数量(V3) | 每周创建受试者数量的汇总矩阵报告,按研究中心分组。 | 模板:受试者 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:受试者研究进度 | 受试者在研究中的进度汇总 | 模板:事件以及事件定义、研究、研究中心和受试者 | 是(Yes) | 否(No) | |
| 标准模板:受试者研究进度(V3) | 计划和已录入事件的表格式报告,按研究中心和受试者分组。 | 模板:事件操作汇总 | 否(No) | 是(Yes) | |
| 标准模板:受试者研究进度(V4) | 计划和已录入事件的表格式报告,按研究中心和受试者分组。 | 模板:事件以及事件操作汇总 | 否(No) | 是(Yes) | 25R1 中的新增功能。建议对数据模型 V2 研究使用此报告版本。 |
| 标准模板:受试者汇总 | 每个状态下的受试者数量 | 模板:受试者以及研究和研究中心 | 是(Yes) | 是(Yes) | |
| 标准模板:各个研究中心的受试者状态汇总(V3) | 每个状态下受试者数量的汇总矩阵报告,按研究中心分组。 | 模板:受试者以及研究和研究中心 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。此报告模板取代标准模板:受试者汇总。建议使用此报告版本。 |
| 标准模板:唯一 CRF(病例报告表)列表 | 按研究列出每位受试者的唯一表单(CRF) | 模板:表单定义 | 是(Yes) | 是(Yes) | |
| 标准模板:唯一 CRF 列表(V3) | 研究中唯一 CRF 定义的表格式报告。 | 模板:表单定义 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 研究收尾状态 | 按研究列出研究中心及研究中心收尾状态 | 模板:研究收尾 | 是(Yes) | 是(Yes) | |
| 研究收尾状态(V3) | 研究中每个研究中心收尾状态的表格式报告。 | 模板:研究收尾 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 可操作 | |||||
| 标准模板:详细缺失表单报告 | 每个研究中心和受试者缺失的表单列表 | 模板:包含事件、研究中心和受试者的表单 | 是(Yes) | 是(Yes) | |
| 标准模板:详细缺失表单报告(V3) | 逾期未提交表单的表格式报告。请注意,这仅包括已添加到计划中但尚未提交的表单。事件必须配置了“逾期天数”,以便标记该事件下的表单为逾期。 | 模板:带有事件、表单定义、研究中心和受试者的表单 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:表单 SDV 详细信息 | 表单 SDV 状态的详细列表 | 模板:包含事件、研究中心和受试者的表单 | 是(Yes) | 否(No) | 数据模型 V2 研究应使用此报告的 V2 版本。 |
| 标准模板:表单 DMR 汇总 | 各个研究中心的表单 DMR 状态汇总列表 | 模板:研究中心与表单 | 是(Yes) | 否(No) | 数据模型 V2 研究应使用此报告的 V2 版本。 |
| 标准模板:特意留空条目 | 受试者病例手册中数据录入用户标记为特意留空的条目列表 | 模板:具有条目历史记录的条目 | 是(Yes) | 否(No) | 使用 Item2 作为主要报告对象不受配置支持。 |
| 标准模板:特意留空条目(V3) | 标记为特意留空条目的表格式报告,按研究中心和受试者分组,可根据研究筛选。仅适用于数据模型 2 的研究。 | 模板:条目 2 | 否(No) | 是(Yes) | |
| 标准模板:各个研究中心和受试者的质疑详细信息 | 每个受试者的质疑详细列表 | 模板:与受试者、质疑绑定和质疑消息关联的质疑 | 是(Yes) | 是(Yes) | |
| 标准模板:各个研究中心和受试者的质疑详细信息(V3) | 质疑详细信息的表格式报告,按研究中心和受试者分组。 | 模板:与受试者、质疑绑定和质疑消息关联的质疑 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:综合表单汇总 | 各个研究中心和受试者的已提交表单和表单审查状态详细列表 | 模板:带有事件、研究中心和受试者的表单 | 是(Yes) | 否(No) | 数据模型 V2 研究应使用此报告的 V2 版本。 |
| 标准模板:综合表单汇总(v2) | 各个研究中心和受试者的已提交表单和表单审查状态详细列表 | 模板:带有事件、研究中心和受试者的表单 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:综合表单汇总) |
| 标准模板:综合表单汇总(V3) | 按研究中心和受试者分组的表格式报告,详细列出表单的 SDV、DMR、冻结、签名和锁定状态及其完成日期。 | 模板:带有事件、表单定义、研究中心、受试者和表单汇总的表单 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。数据模型 V1 研究应使用此报告的 V1 版本(标准模板:综合表单汇总) |
| 研究进度列表 | |||||
| 模板:事件进度列表 | 研究中所有事件及其进度列表 | 模板:事件进度列表 | 是(Yes) | 是(Yes) | 对于数据模型 V1 研究,某些列将为空 |
| 标准模板:事件进度列表(V2) | 带有表单级别操作数据的表格式报告,可根据研究筛选。仅当从 EDC 工具中调度事件进度列表作业时,报告才会填充数据。 | 事件进度列表以及列表的上次运行 | 是(Yes) | 是(Yes) | 对于数据模型 V1 研究,某些列将为空 |
| 模板:表单进度列表 | 研究中所有表单及其进度列表 | 模板:表单进度列表 | 是(Yes) | 是(Yes) | |
| 标准模板:表单进度列表(V2) | 带有表单级别操作数据的表格式报告,可根据研究筛选。仅当从 EDC 工具中调度表单进度列表作业时,报告才会填充数据。 | 表单进度列表以及列表的上次运行 | 是(Yes) | 是(Yes) | |
| 模板:质疑详细信息列表 | 研究中所有质疑的详细列表 | 模板:质疑详细信息列表 | 是(Yes) | 是(Yes) | |
| 标准模板:质疑详细信息列表(V2) | 带有表单级别操作数据的表格式报告,可根据研究筛选。仅当从 EDC 工具中调度质疑详细信息列表作业时,报告才会填充数据。 | 模板:质疑详细信息列表以及列表的上次运行 | 是(Yes) | 是(Yes) | |
| 模板:受试者进度列表 | 研究中所有受试者及其进度列表 | 模板:受试者进度列表 | 是(Yes) | 是(Yes) | |
| 标准模板:受试者进度列表(V2) | 带有表单级别操作数据的表格式报告,可根据研究筛选。仅当从 EDC 工具中调度受试者进度列表作业时,报告才会填充数据。 | 模板:受试者进度列表以及列表的上次运行 | 是(Yes) | 是(Yes) | |
| 编码器 | |||||
| WHODrug 编码报告 | 基于 WHODrug 的表单的临床编码请求和已分配编码(如果已分配) | 模板:临床编码 | 是(Yes) | 是(Yes) | 在 23R3 之前创建的 Vault 上 |
| 标准模板:WHODrug 编码报告(V3) | 基于 WHODrug 的表单的临床编码请求和已分配编码(如果已分配);标准报告由 Veeva 进行更新 | 模板:临床编码 | 是(Yes) | 是(Yes) | |
| 标准模板:WHODrug 编码报告(V4) | 基于 WHODrug 的表单的临床编码请求和已分配编码(如果已分配)。包含编码备注和质疑。 | 模板:带有备注和质疑的临床编码 | 是(Yes) | 是(Yes) | |
| 标准模板:JDrug 编码报告(V3) | 基于 JDrug 的表单的临床编码请求和已分配编码(如果已分配);标准报告由 Veeva 进行更新 | 模板:临床编码 | 是(Yes) | 是(Yes) | |
| 标准模板:JDrug 编码报告(V4) | 基于 JDrug 的表单的临床编码请求和已分配编码(如果已分配)。包含编码备注和质疑。 | 是(Yes) | 是(Yes) | ||
| MedDRA 编码报告 | 基于 MedDRA 的表单的临床编码请求和已分配编码(如果已分配) | 模板:临床编码 | 是(Yes) | 是(Yes) | 在 23R3 之前创建的 Vault 上 |
| 标准模板:MedDRA 编码报告(V3) | 基于 MedDRA 和 MedDRAJ 的表单的临床编码请求和已分配编码(如果已分配);标准报告由 Veeva 进行更新 | 模板:临床编码 | 是(Yes) | 是(Yes) | |
| 标准模板:MedDRA 编码报告(V4) | 基于 MedDRA 和 MedDRAJ 的表单的临床编码请求和已分配编码(如果已分配)。包含编码备注和质疑。 | 模板:带有备注和质疑的临床编码 | 是(Yes) | 是(Yes) | |
| 可操作 | |||||
| 标准模板:每个事件的逾期表单输入 | 包含逾期数据录入任务的事件汇总,包括预计的表单工作量 | 模板:事件以及事件操作汇总 | 是(Yes) | 否(No) | 数据模型 V2 研究:从事件操作汇总对象使用事件状态字段,而不是事件对象 |
| 标准模板:每个事件的逾期表单输入(V3) | 空白和进行中事件的表格式报告,按研究中心和受试者分组。包括每个事件的预期表单数量和数据录入逾期的天数。此报告仅包括配置了逾期天数值的事件。 | 模板:事件以及事件定义和事件汇总 | 是(Yes) | 否(No) | 23R3 中的新增功能。建议使用此报告版本。对于数据模型 V2 研究:从事件操作汇总对象使用事件状态字段,而不是事件对象 |
| 标准模板:时间表偏差报告 | 各个研究方案下研究中心和受试者遵循计划访视时间表的汇总 | 模板:事件操作汇总 | 是(Yes) | 是(Yes) | |
| 标准模板:时间表偏差报告(V3) | 按研究中心和受试者分组的事件表格式报告,显示遵循计划访视时间表的情况。 | 模板:事件操作汇总以及事件定义 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:导致数据更改的质疑 | 系统生成的导致数据更改的质疑的汇总列表 | 质疑操作汇总以及质疑 | 是(Yes) | 是(Yes) | |
| 标准模板:导致数据值更改的质疑(V3) | 按研究和质疑规则分组的导致条目值更改的系统质疑的表格式报告。 | 质疑操作汇总以及质疑 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。此报告取代标准模板:导致数据更改的质疑。建议使用此报告版本。 |
| 研究设计 | |||||
| 标准模板:表单更改原因报告 | 提交后表单更改原因的汇总计数 | 模板:具有条目历史记录的条目 | 是(Yes) | 否(No) | 使用 Item2 作为主要报告对象不受配置支持。 |
| 标准模板:条目更改原因报告(V3) | 每个更新了具体更改原因的研究中心的条目计数矩阵汇总报告,可根据研究筛选。显示该条目的最新更改原因。不包括任何系统管理的更改原因。仅适用于数据模型 2 的研究。 | 模板:条目 2 | 否(No) | 是(Yes) | |
| 标准模板:各个规则定义下的质疑量 | 每个规则定义下的质疑执行数量 | 模板:规则定义以及研究和质疑绑定 | 是(Yes) | 是(Yes) | |
| 标准模板:各个规则定义下的质疑量(V3) | 每个规则定义下的质疑数量的汇总矩阵报告,按研究中心分组。 | 模板:规则定义以及研究和质疑绑定 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 标准模板:唯一规则定义列表 | 研究中的唯一规则列表 | 模板:规则定义以及研究和质疑绑定 | 是(Yes) | 是(Yes) | |
| 标准模板:唯一规则定义列表(V3) | 唯一规则定义的表格式报告。 | 模板:规则定义以及研究和质疑绑定 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 审查(适用于在 19R3 版本之后创建的研究) | |||||
| 标准模板:每周表单 SDV 监查活动(v2) | 按研究中心汇总的每周表单 SDV 监查活动 | 模板:表单以及事件、研究中心、受试者和表单汇总 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:每周表单 SDV 监查活动) |
| 标准模板:每周表单 SDV 监查活动(V3) | 每周标记为 SDV 完成的表单数量的汇总矩阵报告。仅当至少一个表单标记为 SDV 完成时才包括研究中心。 | 模板:表单操作汇总以及表单和研究中心 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。数据模型 V1 研究应使用此报告的 V1 版本(标准模板:每周表单 SDV 监查活动) |
| 标准模板:每周表单 DMR 监查活动(v2) | 按研究中心汇总的每周表单 DMR 监查活动 | 模板:表单以及事件、研究中心、受试者和表单汇总 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:每周表单 DMR 监查活动) |
| 标准模板:每周表单 DMR 监查活动(V3) | 每周标记为 DMR 完成的表单数量的汇总矩阵报告。仅当至少一个表单标记为 DMR 完成时才包括研究中心。 | 模板:表单操作汇总以及表单和研究中心 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。数据模型 V1 研究应使用此报告的 V1 版本(标准模板:每周表单 DMR 监查活动) |
| 标准模板:表单 SDV 汇总(v2) | 表单 SDV 状态的汇总列表 | 模板:表单以及研究中心和汇总 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:表单 SDV 汇总) |
| 标准模板:表单 SDV 汇总(V3) | 表单级别 SDV 状态的汇总矩阵报告。仅包括需要 SDV 的表单。可能的值:Yes 表示表单中所有必填条目均为 SDV 完成,No 表示并非所有必填条目均为 SDV 完成 | 模板:表单操作汇总以及表单和研究中心 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:表单 SDV 汇总) |
| 标准模板:表单 DMR 汇总(v2) | 表单 DMR 状态的汇总列表 | 模板:表单以及研究中心和汇总 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:表单 DMR 汇总) |
| 标准模板:表单 DMR 汇总(V3) | 表单级别 DMR 状态的汇总矩阵报告。仅包括需要 DMR 的表单。可能的值:Yes 表示表单中所有必填条目均为 DMR 完成,No 表示并非所有必填条目均为 DMR 完成。 | 模板:表单操作汇总以及表单和研究中心 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:表单 DMR 汇总) |
| 标准模板:表单 SDV 详细信息(v2) | 各个研究中心的表单 SDV 状态详细列表 | 模板:表单以及事件、研究中心、受试者和表单汇总 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:表单 SDV 详细信息) |
| 标准模板:表单 SDV 详细信息(V3) | 需要 SDV 表单的 SDV 状态表格式报告,按研究中心和受试者分组。可能的值:Yes 表示表单中所有必填条目均为 SDV 完成,No 表示并非所有必填条目均为 SDV 完成。 | 模板:事件操作汇总以及事件和表单定义 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。数据模型 V1 研究应使用此报告的 V1 版本(标准模板:表单 SDV 详细信息) |
| 标准模板:表单 DMR 详细信息(v2) | 各个研究中心的表单 DMR 状态详细列表 | 模板:表单以及事件、研究中心、受试者和表单汇总 | 否(No) | 是(Yes) | 数据模型 V1 研究应使用此报告的 V1 版本(标准模板:表单 DMR 详细信息) |
| 标准模板:表单 DMR 详细信息(V3) | 需要 DMR 表单的 DMR 状态表格式报告,按研究中心和受试者分组。可能的值:Yes 表示表单中所有必填条目均为 DMR 完成,No 表示并非所有必填条目均为 DMR 完成。 | 模板:事件操作汇总以及事件和表单定义 | 否(No) | 是(Yes) | 23R3 中的新增功能。建议对数据模型 V2 研究使用此报告版本。数据模型 V1 研究应使用此报告的 V1 版本(标准模板:表单 DMR 详细信息) |
| 安全 | |||||
| 安全病例 | 安全病例列表 | 模板:安全 | 是(Yes) | 是(Yes) | |
| 标准模板:安全病例(V3) | 研究中安全病例的表格式报告。 | 模板:安全 | 是(Yes) | 是(Yes) | 23R3 中的新增功能。建议使用此报告版本。 |
| 安全消息 | 安全消息列表 | 模板:安全 | 是(Yes) | 是(Yes) | |
| 个人信息板 * 这些报告用于支持个人信息板。 |
|||||
| 信息板:超出范围事件总数 | 超出范围事件的数量 | 模板:事件以及事件操作汇总 | 是(Yes) | 否(No) | 数据模型 V2 研究:从事件操作汇总对象使用事件状态字段,而不是事件对象 |
| 信息板:入组受试者人数 | 各个研究的入组受试者人数 | 模板:受试者以及研究和研究中心 | 是(Yes) | 是(Yes) | |
| 信息板:未解决质疑 | 未解决质疑的数量 | 模板:质疑周期时间汇总 | 是(Yes) | 是(Yes) | |
| 信息板:已回答质疑 | 已回答质疑的数量 | 模板:质疑周期时间汇总 | 是(Yes) | 是(Yes) | |
| 信息板:表单状态(未完成) | 状态为未完成的表单数量 | 模板:包含事件、研究中心和受试者的表单 | 是(Yes) | 是(Yes) | |
| 信息板:各个表单的质疑量 | 按表单质疑的数量 | 模板:带有表单定义和质疑绑定的表单 | 是(Yes) | 是(Yes) | |
| 实验室 | |||||
| 标准模板:带有实验室位置的研究中心实验室 | 显示实验室位置和使用这些位置的研究中心 | 模板:带有实验室位置的研究中心实验室 | 是(Yes) | 是(Yes) | |
| 标准模板:实验室参考范围 | 显示实验室位置及其使用的正常范围 | 模板:带有实验室参考范围的实验室位置 | 是(Yes) | 是(Yes) | |
| 标准模板:实验室条目和分析物定义 | 显示研究中使用的实验室条目定义和分析物定义。 | 模板:带有分析物定义的条目定义 | 是(Yes) | 是(Yes) | |
| 随机化 | |||||
| 紧急揭盲报告 | 显示为研究执行的所有紧急揭盲操作的列表 | 随机化操作历史记录 | 是(Yes) | 是(Yes) | |
| 许可证密钥 | |||||
| 标准模板:EDC 工具中的研究主程序和许可证密钥 | 列出在 EDC 工具中输入的所有研究主程序和任何许可证密钥值 | 模板:带有研究主程序 - 许可证的研究主程序 | 此报告中的数据对 Vault 所有者可见。 | ||
可用报告类型模板
以下是 Veeva EDC 中可用的标准报告类型模板。
| 名称 | 说明 | 主要报告对象 | 相关对象 | 应用程序 |
|---|---|---|---|---|
| 模板:事件操作汇总 | 此报告类型可以跟踪预期表单的数量、事件中表单的逾期天数、事件日期以及事件日期超出事件窗的天数。 | 事件操作汇总 | 不适用 | EDC |
| 模板:事件进度列表 | 此报告类型在 EDC 工具 > 作业时间表(EDC Tools > Job Schedule)中的事件进度列表作业创建。 | 事件进度列表 | 事件进度列表 | EDC |
| 模板:事件进度列表以及列表的上次运行 | 此报告类型在 EDC 工具 > 作业时间表(EDC Tools > Job Schedule)中的事件进度列表作业创建。 | 事件进度列表 | 事件进度列表 | EDC |
| 模板:事件以及事件定义、研究、研究中心和受试者 | 此报告类型可以显示事件信息,这些事件引用了事件设计、研究、研究中心和与事件相关受试者的信息。 | 事件 |
|
EDC |
| 模板:事件以及事件操作汇总 | 此报告类型可以显示事件操作汇总以及事件详细信息,如审查状态、创建日期和计划日期。 | 事件 | 事件操作汇总 | EDC |
| 模板:表单周期时间汇总 | 此报告类型可以列出每个表单完成/提交所需的平均时间。 | 表单操作汇总 | 不适用 | EDC |
| 模板:表单定义 | 此报告类型可以显示表单定义。 | 表单定义 | 不适用 | EDC |
| 模板:表单进度列表 | 此报告类型在 EDC 工具 > 作业时间表中的表单进度列表作业创建。 | 表单进度列表 | 表单进度列表 | EDC |
| 模板:表单进度列表以及列表的上次运行 | 此报告类型在 EDC 工具 > 作业时间表中的表单进度列表作业创建。 | 表单进度列表 | 表单进度列表 | EDC |
| 模板:包含事件、研究中心和受试者的表单 | 此报告类型可以显示表单信息,这些表单引用了有关 SDV 详细信息和状态的信息 | 表单 |
|
EDC |
| 模板:条目 2 | 此报告类型可以列出特意留空条目和条目更改原因的信息。 | 条目 | 不适用 | EDC |
| 模板:质疑周期时间汇总 | 此报告类型可以列出每个质疑被回答或解决所需的平均时间 | 质疑操作汇总 | 不适用 | EDC |
| 模板:质疑详细信息列表 | 此报告类型在 EDC 工具>作业时间表中的质疑详细信息列表作业创建。 | 质疑详细信息列表 | 质疑详细信息列表 | EDC |
| 模板:质疑详细信息列表以及列表的上次运行 | 此报告类型在 EDC 工具>作业时间表中的质疑详细信息列表作业创建。 | 质疑详细信息列表 | 质疑详细信息列表 | EDC |
| 模板:与受试者、质疑绑定和质疑消息关联的质疑 | 此报告类型可以列出受试者、研究中心以及有关质疑和质疑绑定及消息的信息。 | 质疑 |
|
EDC |
| 模板:规则定义以及研究和质疑绑定 | 此报告类型可以列出规则定义以及有关名称、质疑绑定和研究中心的信息 | 规则定义 |
|
EDC |
| 模板:研究中心与表单 | 此报告类型可以列出有关研究中心名称和相应表单的引用信息。 | 研究中心 | 表单 | EDC |
| 模板:带有质疑绑定的研究中心 | 此报告类型可以列出有关研究中心和相应质疑的信息。 | 研究中心 | 质疑绑定 | EDC |
| 模板:受试者 | 此报告类型可以提供有关受试者的信息。 | 受试者 | 不适用 | EDC |
| 模板:受试者进度列表 | 此报告类型在 EDC 工具 > 作业时间表中的受试者进度列表作业创建。 | 受试者进度列表 | 受试者进度列表 | EDC |
| 模板:受试者进度列表以及列表的上次运行 | 此报告类型在 EDC 工具 > 作业时间表中的受试者进度列表作业创建。 | 受试者进度列表 | 受试者进度列表 | EDC |
| 模板:受试者以及研究和研究中心 | 此报告类型可以列出有关受试者状态和研究中心的信息。 | 受试者 |
|
EDC |
| 模板:安全 | 此报告类型可以列出有关安全病例和安全消息的信息,包含来自安全病例表单的上下文。 | 安全病例 |
|
EDC、安全 |
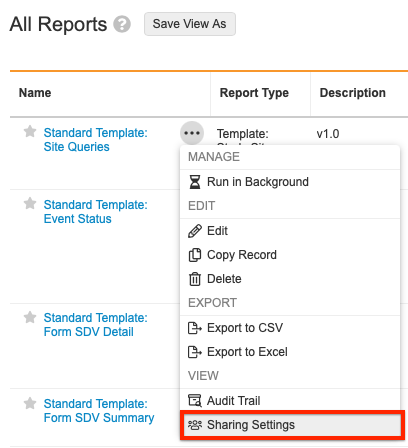
共享设置
必须为每个新报告版本添加适当的用户到报告共享设置中。
要访问报告共享设置,请在报告(Reports)选项卡中单击想要更新的报告旁边的操作(Actions)按钮。
相关权限
在默认情况下,报告功能对以下标准研究角色的用户可用:
- CDMS Clinical Coder(CDMS 临床编码员)
- CDMS Clinical Coder Administrator(CDMS 临床编码器管理员)
- CDMS Clinical Research Associate(CDMS 临床试验监查员)
- CDMS Data Manager(CDMS 数据管理员)
- CDMS Lead Data Manager(CDMS 首席数据管理员)
- CDMS Study Designer(CDMS 研究设计者)
- CDMS User Administrator(CDMS 用户管理员)
如果贵组织使用自定义研究角色,必须拥有报告信息板(Reports Dashboards)选项卡和计划报告权限才能使用所有报告功能。
单个报告必须与研究角色或自定义组共享。