임상시험계획서 위반 모니터링
의뢰자는 Vault 내에서 스터디의 임상시험계획서 위반을 추적할 수 있습니다. 검토(Review) > 임상시험계획서 위반(Protocol Deviations) 탭에서 임상시험계획서 위반을 수동으로 생성하거나 시스템에서 규칙을 통해 프로그래밍 방식으로 임상시험계획서 위반을 생성할 수 있습니다. 수동 및 프로그래밍 가능한 임상시험계획서 위반은 모두 대상자, 이벤트, 폼 또는 아이템에 연결되며 각 임상시험계획서 위반은 다음 세부 정보를 캡처합니다.
- 요약
- 범주(Category)
- 하위 범주
- Severity
- 설명
- 위반 날짜
- 확인된 날짜
필수 구성 요소
임상시험계획서 위반(Protocol Deviations) 기능은 스터디 설계자가 스터디에 대해 활성화해야 합니다.
스터디 설계자는 임상시험계획서 위반을 생성할 때 참조할 수 있도록 범주, 하위 범주 및 심각도를 생성해야 합니다.
표준 CDMS Clinical Research Associate(CDMS 모니터), CDMS Data Manager(CDMS 데이터 매니저) 및 CDMS Lead Data Manager(CDMS 책임 데이터 매니저) 스터디 역할을 보유한 사용자는 기본적으로 아래에 설명된 작업을 수행할 수 있습니다. 조직에서 커스텀 스터디 역할을 사용하는 경우 역할에서 다음 권한을 부여해야 합니다.
| 유형(Type) | 권한 레이블 | 제어 |
|---|---|---|
| 표준 탭 | 검토(Review) 탭 | 검토 탭에 접근할 수 있는 기능 |
| 표준 탭 | 임상시험계획서 위반(Protocol Deviations) 탭 | 임상시험계획서 위반 탭에 접근할 수 있는 기능 |
| 기능적 권한 | 임상시험계획서 위반 보기 | 임상시험계획서 위반을 볼 수 있는 기능 |
| 기능적 권한 | 임상시험계획서 위반 편집 | 임상시험계획서 위반을 편집할 수 있는 기능 |
| 기능적 권한 | 임상시험계획서 위반 생성 | 임상시험계획서 위반을 생성할 수 있는 기능 |
스터디에 제한된 데이터가 포함되어 있는 경우 제한된 데이터 접근 권한이 있어야 해당 데이터를 볼 수 있습니다.
스터디 역할에 대해 자세히 알아보십시오.
임상시험계획서 위반 보기
Vault에는 연결된 임상시험계획서 위반이 있는 대상자, 이벤트, 폼 또는 아이템에 대해 임상시험계획서 위반 표시기()가 표시됩니다.
표시기를 클릭하여 임상시험계획서 위반에 대한 요약을 표시할 수 있으며, 여기에는 임상시험계획서 위반(Protocol Deviations) 탭에서 임상시험계획서 위반의 전체 보기를 열 수 있는 링크가 포함되어 있습니다.
모든 임상시험계획서 위반 목록을 보려면 검토(Review) > 임상시험계획서 위반(Protocol Deviations)으로 이동합니다.
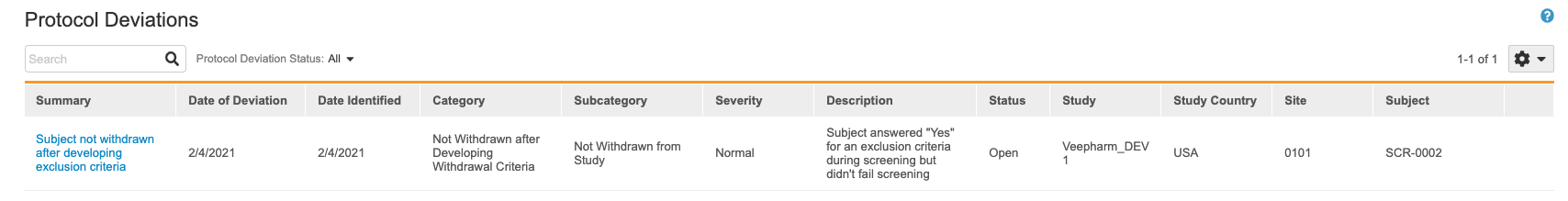
그러면 임상시험계획서 위반(Protocol Deviations) 리스팅이 열립니다.
검색 및 필터링
개별 임상시험계획서 위반을 검색할 수 있습니다. 특정 상태의 임상시험계획서 위반만 표시하도록 리스팅을 필터링할 수도 있습니다.
임상시험계획서 위반 상태별로 필터링하는 방법은 다음과 같습니다.
- 검토(Review) > 임상시험계획서 위반(Protocol Deviations)으로 이동합니다.
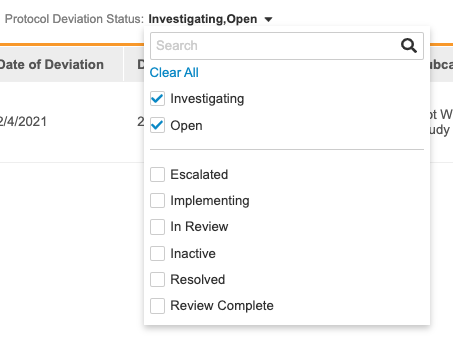
- 모두(All)를 클릭하여 임상시험계획서 위반 상태(Protocol Deviation Status) 필터 목록을 엽니다.
- 페이지의 아무 곳이나 클릭하여 필터 목록을 종료합니다.
- 필터를 다시 열고 모두 지우기(Clear All)를 클릭하거나 개별 상태 확인란의 선택을 취소하여 필터를 제거합니다.
수동 임상시험계획서 위반 생성
Vault에서 자동으로 생성하는 프로그래밍 위반 외에도 임상시험계획서 위반을 수동으로 생성할 수 있습니다. 잠긴 사이트에서는 새로운 임상시험계획서 위반을 생성할 수 없습니다.
대상자
대상자에 대한 임상시험계획서 위반을 생성하는 방법은 다음과 같습니다.
- 검토(Review) 탭에서 대상자로 이동합니다.
- 기타 작업(More Actions) 메뉴에서 임상시험계획서 위반 생성(Create Protocol Deviation)을 선택합니다.
- 임상시험계획서 위반 생성(Create Protocol Deviation) 대화 상자에서 필수 필드를 채웁니다.
- 저장을 클릭합니다.
이벤트
이벤트에 대한 임상시험계획서 위반을 생성하는 방법은 다음과 같습니다.
- 검토(Review) 탭에서 이벤트로 이동합니다.
- 기타 작업(More Actions) 메뉴에서 임상시험계획서 위반 생성(Create Protocol Deviation)을 선택합니다.
- 임상시험계획서 위반 생성(Create Protocol Deviation) 대화 상자에서 필수 필드를 채웁니다.
- 저장을 클릭합니다.
폼
폼에 대한 임상시험계획서 위반을 생성하는 방법은 다음과 같습니다.
- 검토(Review) 탭에서 폼으로 이동합니다.
- 기타 작업(More Actions) 메뉴에서 임상시험계획서 위반 생성(Create Protocol Deviation)을 선택합니다.
- 임상시험계획서 위반 생성(Create Protocol Deviation) 대화 상자에서 필수 필드를 채웁니다.
- 저장을 클릭합니다.
아이템
아이템에 대한 임상시험계획서 위반을 생성하는 방법은 다음과 같습니다.
- 검토(Review) 탭에서 아이템으로 이동합니다.
- 기타 작업(More Actions) 메뉴에서 임상시험계획서 위반 생성(Create Protocol Deviation)을 선택합니다.
- 임상시험계획서 위반 생성(Create Protocol Deviation) 대화 상자에서 필수 필드를 채웁니다.
- 저장을 클릭합니다.
수동 임상시험계획서 위반 생성
마지막 업데이트: 23R1
이 비디오에서는 검토(Review) 탭에서 새 수동 임상시험계획서 위반을 생성하는 방법에 대해 설명합니다.
시스템 생성 임상시험계획서 위반
시스템 생성 임상시험계획서 위반은 사용자가 입력한 데이터가 적격할 때 자동으로 생성됩니다. 이 위반은 스터디 디자인의 일부인 임상시험계획서 위반 생성 규칙 작업에 따라 제어됩니다. Vault에서 규칙 구성에 따라 요약, 범주, 하위 범주, 심각도, 설명을 자동으로 설정합니다.
수동으로 생성된 임상시험계획서 위반과 상호 작용하는 것과 동일한 방식으로 해당 임상시험계획서 위반에 응답하고 이와 상호 작용할 수 있습니다.
해당 임상시험계획서 위반은 "시스템"에서 생성된 것으로 표시됩니다. 미결 상태에서 자동으로 생성됩니다. 사이트 사용자가 나중에 폼을 편집하고 결과 데이터가 더 이상 임상시험계획서 위반으로 적격하지 않은 경우 Vault에서 임상시험계획서 위반을 비활성으로 설정합니다. 또 다른 편집으로 인해 데이터가 한 번 더 적격해지면 Vault에서 기존 임상시험계획서 위반을 활성화하는 대신 새 임상시험계획서 위반을 생성합니다.
임상시험계획서 위반 업데이트
임상시험계획서 위반 세부 사항(Protocol Deviation Details) 페이지의 의뢰자 검토(Sponsor Review) 섹션에서 상태(Status), 심각도(Severity) 및 해결(Resolution) 필드를 변경하여 임상시험계획서 위반을 업데이트할 수 있습니다. 해당 필드에 입력하는 내용은 조직에서 임상시험계획서 위반을 처리하기 위해 정의한 워크플로에 따라 달라집니다.
임상시험계획서 위반을 업데이트하는 방법은 다음과 같습니다.
- 검토(Review) > 임상시험계획서 위반(Protocol Deviations)으로 이동합니다.
- 요약(Summary)을 클릭하여 임상시험계획서 위반을 엽니다.
- 편집을 클릭합니다.
-
응답에 따라 상태(Status), 심각도(Severity) 및 해결(Resolution) 필드를 업데이트합니다.
- 저장을 클릭합니다.
- 변경 이유를 선택합니다.
임상시험계획서 위반 검토
마지막 업데이트: 24R1
이 비디오에서는 검토(Review) 탭에서 임상시험계획서 위반을 검토하는 방법에 대해 설명합니다.
임상시험계획서 위반 내보내기
모든 임상시험계획서 위반 목록을 CSV 또는 Excel™ 파일로 내보낼 수 있습니다. 리스팅에 적용하는 필터는 내보내기에 적용되지 않습니다.
임상시험계획서 위반을 내보내는 방법은 다음과 같습니다.
- 검토(Review) > 임상시험계획서 위반(Protocol Deviations)으로 이동합니다.
- Vault에서 파일 생성이 시작됩니다. 완료되면 Vault에서 파일을 다운로드할 수 있는 링크가 포함된 이메일을 보냅니다.
해당 오딧트레일 보기
임상시험계획서 위반 세부 사항(Protocol Deviation Details) 페이지에서 개별 임상시험계획서 위반에 대한 오딧트레일을 볼 수 있습니다. 작업(Actions) 메뉴에서 오딧트레일(Audit Trail)을 선택합니다.